Clear Sky Science · fr
Effets thérapeutiques de l’IGF-2 sur le NMOSD en inhibant l’apoptose des astrocytes via la modulation de la voie de signalisation IGF-1R/PI3K/AKT
Protéger le cerveau dans une maladie auto-immune peu connue
Le trouble du spectre de la neuromyélite optique, ou NMOSD, est une maladie auto-immune rare mais dévastatrice qui attaque les nerfs optiques et la moelle épinière, laissant souvent les patients aveugles, paralysés ou avec des troubles cognitifs importants. Les traitements actuels visent principalement à calmer le système immunitaire, sont coûteux et ne protègent pas directement les cellules cérébrales contre les lésions. Cette étude examine si une molécule naturelle liée à la croissance présente dans le sang, appelée IGF‑2, pourrait aider à protéger les cellules cérébrales des dommages dans le NMOSD et offrir une nouvelle voie thérapeutique.
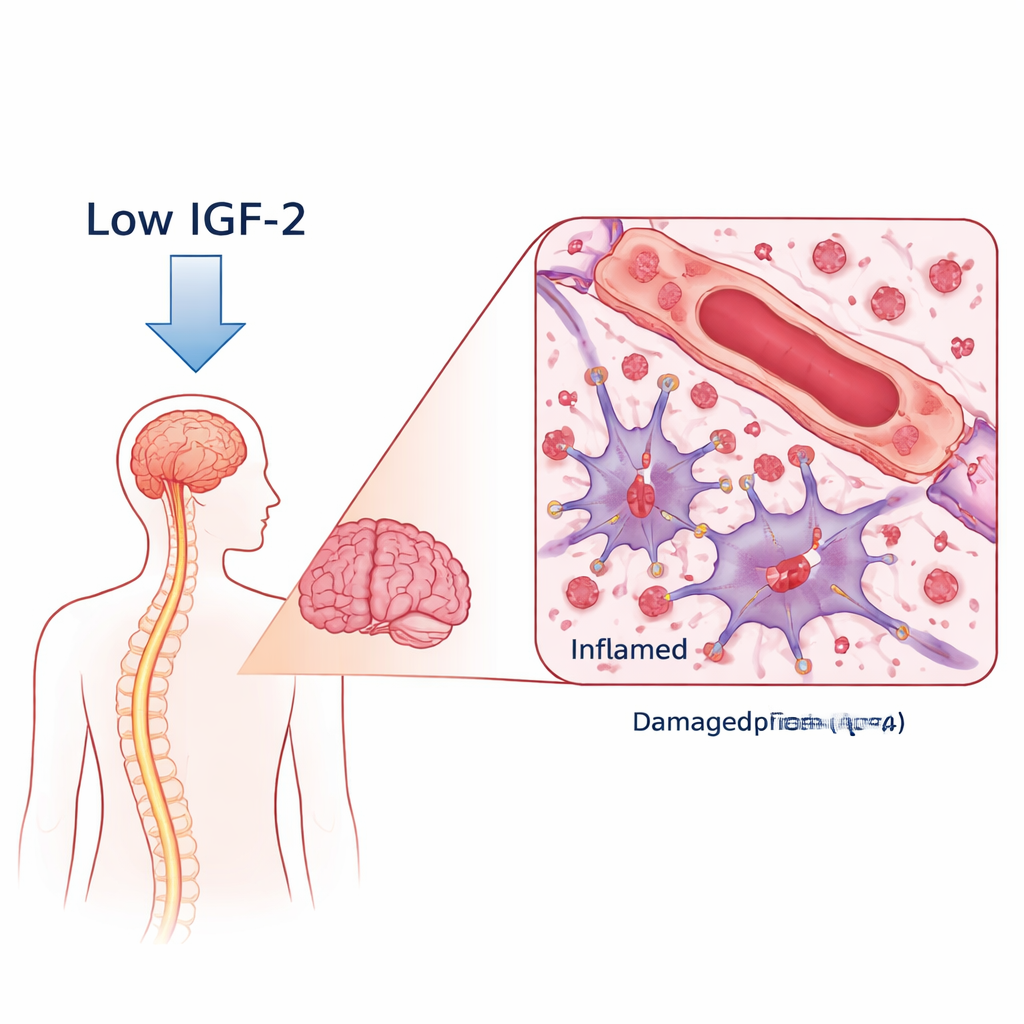
Un anticorps néfaste et un protecteur manquant
Dans le NMOSD, l’organisme produit des anticorps dirigés contre une protéine canal d’eau appelée AQP4, située à la surface des cellules de soutien étoilées du cerveau, les astrocytes. Lorsque ces anticorps se lient, ils déclenchent des attaques immunitaires qui endommagent les astrocytes, enlèvent la myéline (la gaine isolante des nerfs) et peuvent nuire aux neurones. Les chercheurs ont comparé le sang de femmes atteintes de NMOSD positifs pour les anticorps anti-AQP4 à celui de volontaires sains. Grâce à un large relevé protéique, ils ont constaté que les niveaux d’IGF‑2 étaient fortement diminués chez les patients NMOSD, tandis que deux protéines de liaison à l’IGF pouvant piéger l’IGF‑2 étaient plus élevées. Fait important, les patients ayant les taux d’IGF‑2 les plus bas avaient tendance à présenter un handicap plus sévère et de moins bons scores aux tests de mémoire et de fonctions cognitives, reliant cette molécule à la gravité de la maladie et à la santé cognitive.
Le traitement standard favorise la restauration de l’IGF-2
De nombreux patients NMOSD reçoivent du rituximab, un médicament qui élimine les cellules B productrices d’anticorps. L’équipe a mesuré les protéines sanguines avant et après le traitement par rituximab. Après la thérapie, les niveaux d’IGF‑2 ont augmenté et les protéines de liaison ont diminué, se rapprochant du profil observé chez les personnes saines. Cela suggère que maîtriser le système immunitaire peut permettre à l’organisme de restaurer certains de ses facteurs protecteurs. Bien que le rituximab ne soit pas conçu pour agir sur l’IGF‑2, cette évolution de la molécule laisse entendre qu’elle peut faire partie de la réponse de récupération de l’organisme, et que la surveillance de l’IGF‑2 pourrait aider à suivre l’évolution des patients au fil du temps.
Tester l’IGF-2 dans un modèle murin de la maladie
Pour déterminer si l’IGF‑2 peut faire plus que refléter la gravité de la maladie, les scientifiques ont utilisé un modèle murin. Ils ont injecté des anticorps humains anti-AQP4 et du complément humain dans le cerveau de souris, reproduisant des caractéristiques clés du NMOSD : perte d’AQP4 sur les astrocytes, inflammation, dégradation de la myéline et faiblesse des membres. Un autre groupe de souris a d’abord reçu un virus inoffensif qui faisait produire aux cellules cérébrales une quantité supplémentaire d’IGF‑2. Ces souris à IGF‑2 augmenté ont moins perdu de poids, présenté des troubles moteurs plus légers et montré moins de perte de myéline et d’inflammation dans le tissu cérébral et médullaire. Le traitement standard par rituximab a également été bénéfique, mais la surexpression d’IGF‑2 a semblé protéger plus directement le tissu cérébral, suggérant un rôle neuroprotecteur plutôt que seulement immunosuppresseur.
Comment l’IGF-2 freine la mort cellulaire et l’inflammation
L’équipe a ensuite examiné des astrocytes en culture exposés aux anticorps du NMOSD. Normalement, ces anticorps réduisaient les niveaux d’un récepteur clé appelé IGF‑1R et désactivaient une voie de protection en aval connue sous le nom PI3K/AKT, tout en activant des protéines « d’autodestruction » et des signaux inflammatoires. Lorsque les chercheurs ont contraint les astrocytes à produire davantage d’IGF‑2, cette voie protectrice s’est réactivée, les marqueurs de mort cellulaire ont diminué et les cellules ont libéré moins de molécules inflammatoires telles que IL‑1β, IL‑6 et TNF‑α. Le blocage du récepteur IGF‑1R a partiellement annulé ces bénéfices, montrant que l’IGF‑2 agit principalement en activant la chaîne IGF‑1R/PI3K/AKT à l’intérieur des astrocytes. Chez les souris vivantes, l’augmentation d’IGF‑2 a également réduit l’activation des microglies, les sentinelles immunitaires du cerveau, et abaissé les signaux inflammatoires dans la circulation sanguine.
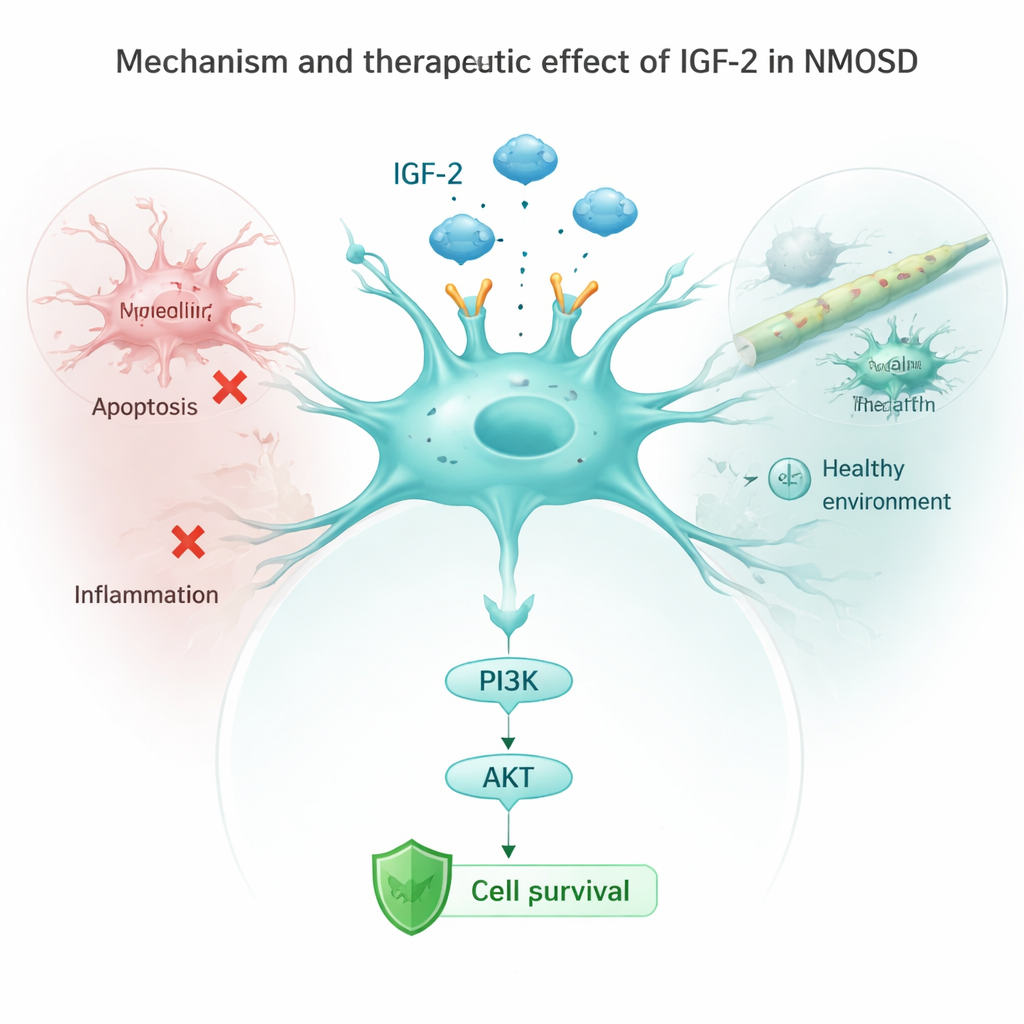
Ce que cela pourrait signifier pour les patients
Pris ensemble, ces résultats suggèrent que des taux faibles d’IGF‑2 constituent à la fois un signe d’alerte et une opportunité manquée dans le NMOSD. Les patients ayant moins d’IGF‑2 ont tendance à être plus handicapés et à présenter des capacités cognitives réduites, tandis que restaurer ou augmenter l’IGF‑2 dans des modèles expérimentaux aide les astrocytes à survivre, réduit l’inflammation cérébrale et diminue les lésions nerveuses. Bien que ces travaux soient encore préliminaires, basés sur un petit nombre de patients et sur des études animales, ils désignent l’IGF‑2 comme une cible prometteuse pour des traitements futurs qui, outre l’atténuation de l’attaque immunitaire, protégeraient directement les cellules cérébrales vulnérables.
Citation: Zhang, Y., Xu, N., Yu, K. et al. Therapeutic effects of IGF-2 on NMOSD by inhibiting astrocyte apoptosis through modulation of the IGF-1R/PI3K/AKT signaling pathway. Sci Rep 16, 6312 (2026). https://doi.org/10.1038/s41598-026-37456-4
Mots-clés: neuromyélite optique, astrocytes, IGF-2, neuroinflammation, neuroprotection