Clear Sky Science · fr
Intégration de la toxicologie en réseau, de l’apprentissage automatique et des simulations de dynamique moléculaire pour révéler les mécanismes doubles de la tanshinone IIA dans le TNBC et la cardiotoxicité induite par la doxorubicine
Pourquoi cette recherche importe pour les patients
La doxorubicine est un médicament essentiel contre le cancer du sein, mais elle comporte un inconvénient sérieux : elle peut endommager le cœur, parfois des années après la fin du traitement. Parallèlement, le cancer du sein triple négatif — une forme difficile à traiter qui ne présente pas les cibles hormonales et de facteurs de croissance habituelles — nécessite encore de meilleures thérapies. Cette étude explore si la tanshinone IIA, un composé extrait de la plante médicinale chinoise Salvia miltiorrhiza, pourrait à la fois protéger le cœur de la toxicité de la doxorubicine et aider à attaquer les tumeurs mammaires agressives, rendant potentiellement la chimiothérapie plus sûre et plus efficace.
Un composé, deux grands problèmes
La doxorubicine a sauvé d’innombrables vies, mais ses bénéfices sont limités par une cardiotoxicité dépendant de la dose : au‑delà d’une certaine dose cumulée, le risque d’insuffisance cardiaque augmente nettement. Les cliniciens font souvent face à un choix douloureux entre contrôler le cancer et protéger le cœur. Des travaux précliniques antérieurs suggéraient que la tanshinone IIA peut renforcer les défenses antioxydantes des cellules cardiaques et tuer directement les cellules cancéreuses, mais les raisons moléculaires sous‑jacentes restaient floues. Les auteurs se sont donc donné pour objectif de cartographier, de manière systématique, comment ce composé unique pourrait atténuer les lésions cardiaques tout en frappant le cancer du sein triple négatif, établissant un pont entre la médecine traditionnelle et l’oncologie de précision moderne. 
Exploiter de grandes données biologiques pour la protection cardiaque
Pour comprendre la protection cardiaque, l’équipe a d’abord rassemblé des milliers de gènes liés à la cardiotoxicité à partir de plusieurs grandes bases de données et les a combinés aux cibles protéiques connues de la doxorubicine et de la tanshinone IIA. Treize cibles « chevauchantes » sont apparues — des protéines associées aux lésions cardiaques, interagissant avec la doxorubicine et potentiellement modulables par la tanshinone IIA. À l’aide de cartes d’interactions protéine–protéine, les chercheurs ont réduit cette liste à six acteurs centraux, dont CCND1 (un régulateur du cycle cellulaire), APAF1 (un déclencheur de la mort cellulaire programmée), AR (récepteur des androgènes), TERT (essentiel pour le maintien des extrémités chromosomiques), MMP2 (une enzyme de remodelage tissulaire) et NQO1 (une enzyme antioxydante). Le docking informatique et les simulations de dynamique moléculaire ont suggéré que la doxorubicine et la tanshinone IIA peuvent se lier fortement à ces protéines, mais que les complexes protéine–tanshinone IIA sont souvent plus stables et énergétiquement favorables, ce qui laisse entendre que le composé végétal pourrait détourner ou atténuer les signaux nocifs de la doxorubicine dans le cœur.
Dévoiler comment il cible les tumeurs agressives
Côté cancer, les chercheurs se sont concentrés sur des jeux de données d’expression génique du cancer du sein triple négatif. Ils ont comparé des échantillons tumoraux à du tissu mammaire normal pour identifier des centaines de gènes anormalement activés ou réprimés. Ils ont ensuite utilisé une technique appelée analyse de réseau de co‑expression génique pondérée pour repérer les groupes de gènes les plus étroitement liés au phénotype triple négatif. En croisant ces gènes tumoraux avec les cibles prédites de la tanshinone IIA, ils ont distillé une petite liste de candidats et appliqué trois méthodes d’apprentissage automatique indépendantes pour déterminer quels gènes distinguaient le mieux la tumeur du tissu normal et avaient le plus de chances d’être cliniquement pertinents. Les preuves convergentes ont mis en avant une cible remarquable : EZH2, un gène impliqué dans le compactage de l’ADN et souvent hyperactif dans les cancers agressifs.
Relier la biologie tumorale et le système immunitaire
Pour comprendre pourquoi EZH2 compte chez de véritables patients, l’équipe a examiné de grandes bases de données tumorales. Ils ont constaté que EZH2 est nettement plus exprimé dans les tumeurs mammaires invasives que dans le tissu mammaire normal. Si son expression n’était pas clairement corrélée à la survie globale sur l’ensemble des cas de cancer du sein, elle était fortement liée à des caractéristiques du microenvironnement immunitaire tumoral. Des niveaux plus élevés d’EZH2 corrélaient avec une infiltration accrue de plusieurs types cellulaires immunitaires — comme les lymphocytes B et T — et avec une expression plus importante de molécules qui stimulent ou inhibent les réponses immunitaires, y compris des points de contrôle immunitaires bien connus comme CTLA‑4 et LAG‑3. Ces schémas suggèrent qu’EZH2 se situe à l’intersection de la croissance tumorale et du contrôle immunitaire, et qu’un médicament comme la tanshinone IIA, en influençant EZH2, pourrait aider à remodeler la façon dont le système immunitaire reconnaît et attaque le cancer du sein triple négatif. 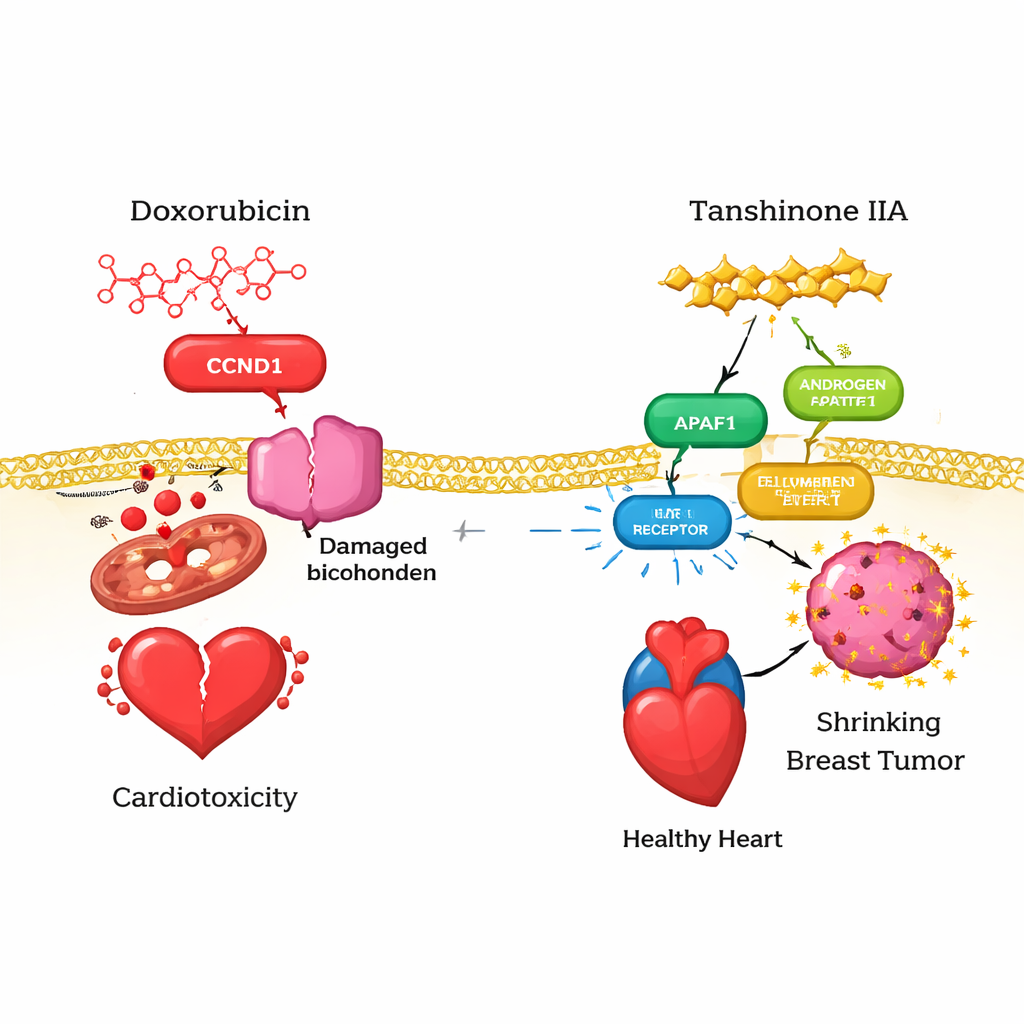
Ce que cela pourrait signifier pour les traitements futurs
En termes simples, ce travail propose que la tanshinone IIA puisse jouer un double rôle dans la prise en charge du cancer du sein : agir comme une sorte de « bouclier chimique » réduisant les lésions cardiaques liées à la doxorubicine en stabilisant des protéines clés protectrices du cœur, et servir en même temps d’arme ciblée contre le cancer du sein triple négatif via son action sur EZH2 et les voies immunitaires associées. Les résultats reposent sur des analyses computationnelles et statistiques plutôt que sur des essais animaux ou humains, ils constituent donc un plan préliminaire plutôt qu’une thérapie prête à l’emploi. Néanmoins, ils offrent une feuille de route moléculaire détaillée pour concevoir des traitements combinés qui préservent le pouvoir vital de la doxorubicine tout en en limitant les risques à long terme — et pour traduire un composant d’une plante traditionnelle en un adjuvant anticancéreux moderne guidé par les mécanismes.
Citation: Wu, B., Lan, Xh., Chen, Xq. et al. Integrating network toxicology, machine learning, and molecular dynamics simulations to reveal tanshinone iia’s dual mechanisms in TNBC and doxorubicin-induced cardiotoxicity. Sci Rep 16, 6861 (2026). https://doi.org/10.1038/s41598-026-37428-8
Mots-clés: tanshinone IIA, cardiotoxicité liée à la doxorubicine, cancer du sein triple négatif, EZH2, pharmacologie de réseau