Clear Sky Science · fr
L’évaluation métabolomique révèle un épuisement des acides aminés et des métabolites énergétiques dans le muscle squelettique après une insuffisance rénale aiguë ischémique chez la souris
Pourquoi des reins endommagés peuvent vous priver de force
Les personnes souffrant d’une insuffisance rénale aiguë remarquent souvent quelque chose qui semble sans lien avec les analyses d’urine ou de sang : leurs muscles sont faibles et la convalescence est lente. Cette étude pose une question simple mais importante — lorsque les reins sont soudainement endommagés, que se passe‑t‑il réellement à l’intérieur des réserves d’énergie et des éléments constitutifs des muscles ? À partir d’un inventaire chimique détaillé des muscles de souris, les chercheurs montrent que l’insuffisance rénale aiguë déclenche un prélèvement à l’échelle du corps sur des nutriments clés et des molécules énergétiques, laissant le muscle squelettique dans un état appauvri et pauvre en énergie.
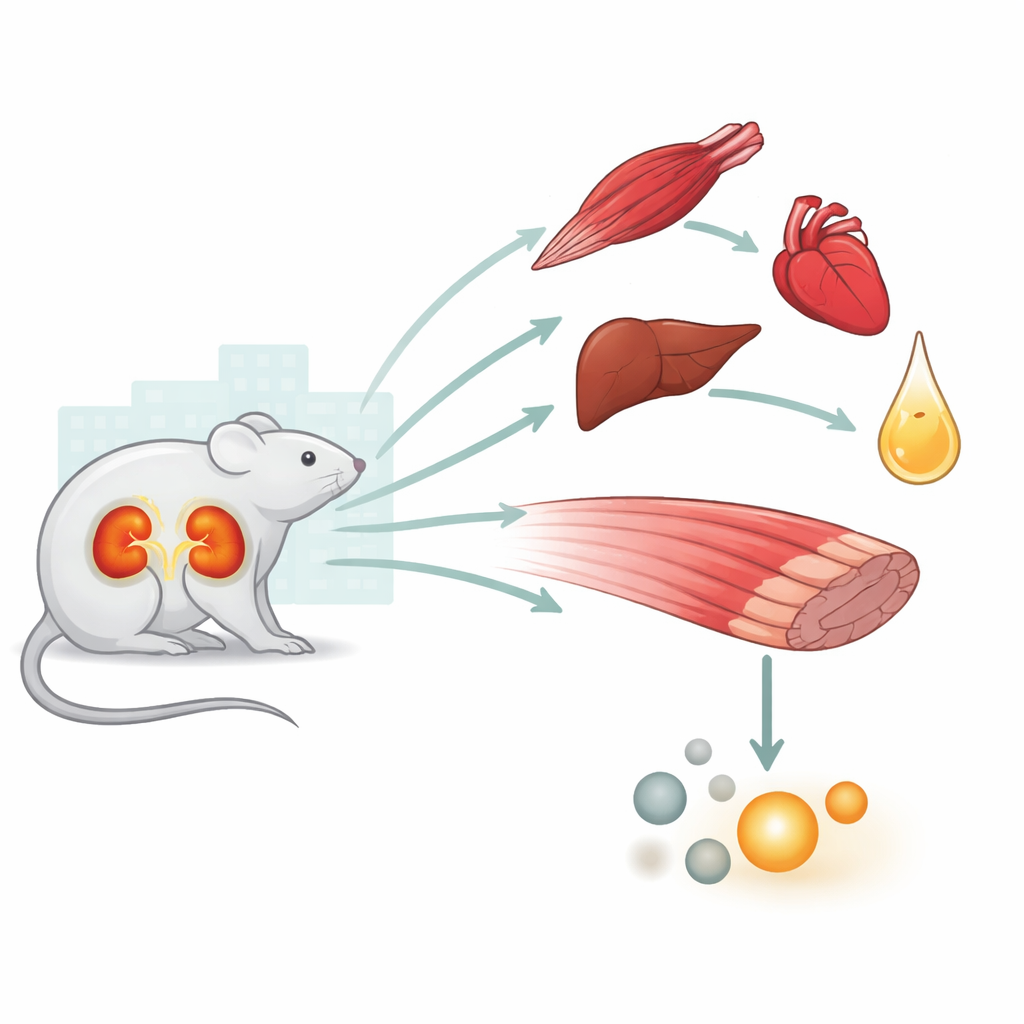
Une crise corporelle, pas seulement un problème rénal
L’insuffisance rénale aiguë (IRA) est fréquente chez les patients hospitalisés et en soins intensifs et est fortement associée à un risque de décès accru. Les cliniciens observent depuis longtemps que l’IRA se comporte comme un état de stress systémique, affectant le cœur, les poumons, le foie, le cerveau et les muscles. Des travaux antérieurs de ce groupe ont montré qu’après une perte temporaire du flux sanguin vers les reins chez la souris, le cœur, le foie, les poumons et les reins eux‑mêmes présentaient des signes chimiques de faible énergie et de stress oxydatif. Sur cette base, l’étude actuelle se concentre sur le muscle squelettique, un important réservoir de glucides et d’acides aminés que l’organisme peut mobiliser en cas de stress sévère.
Comment l’étude a été réalisée chez la souris
Les chercheurs ont induit une IRA ischémique chez des souris mâles jeunes adultes en clampant brièvement l’apport sanguin des deux reins, puis en restaurant la circulation. Ils ont comparé ces animaux à des souris soumises à une chirurgie factice (sham) et à des témoins non opérés. À 24 et 72 heures, ils ont prélevé un muscle clé de la jambe (le gastrocnémien) et utilisé une approche métabolomique non ciblée — un balayage chimique ultra‑sensible — pour mesurer 175 petites molécules, dont des acides aminés, des antioxydants et des composés liés à l’énergie. Des méthodes statistiques et de reconnaissance de motifs ont été employées pour déterminer quelles molécules changeaient le plus et comment la chimie musculaire différait entre les groupes.
Carburant musculaire et antioxydants en baisse
Les changements les plus marquants sont apparus 24 heures après la lésion rénale. Environ deux cinquièmes des métabolites détectés étaient modifiés, et le schéma global était clair : de nombreux composés clés dans le muscle étaient appauvris par rapport à la chirurgie factice. Des acides aminés essentiels et non essentiels tels que l’alanine, la valine, la lysine, la méthionine et la tyrosine ont diminué, tout comme plusieurs molécules du cycle de l’urée (arginine, citrulline, ornithine, argininosuccinate) qui participent à la gestion des déchets azotés et soutiennent la production de créatine. L’antioxydant cellulaire principal, le glutathion, et ses précurseurs (y compris la méthionine et un dipeptide cystéine‑glycine) étaient également réduits, ce qui indique un stress oxydatif accru. Les molécules liées à l’énergie, y compris la créatine et des intermédiaires des voies énergétiques centrales, ont également tendance à diminuer, suggérant que le muscle sacrifie ses propres réserves pour soutenir le reste de l’organisme.
Relier le muscle aux autres organes
Pour voir la situation à plus grande échelle, l’équipe a comparé les données musculaires avec des profils métabolomiques préalablement recueillis dans le rein, le foie, le cœur et le plasma sanguin au même point de 24 heures. À travers tous ces sites, certains thèmes se répétaient : appauvrissement généralisé du glutathion et de ses précurseurs, diminution de l’alanine et perturbation constante de la chimie liée à l’arginine et au cycle de l’urée. Parallèlement, certains produits de dégradation, comme l’allantoïne (un marqueur de stress oxydatif), augmentaient dans plusieurs organes et dans le sang. La créatine et sa forme riche en énergie, la phosphocréatine, étaient relativement augmentées dans le foie, le rein et le sang, alors que l’arginine et les acides aminés chutaient dans le muscle et le plasma, ce qui suggère que le muscle squelettique pourrait exporter des substrats pour permettre aux autres organes — et en particulier aux reins endommagés — de continuer à produire de l’énergie en situation de stress.
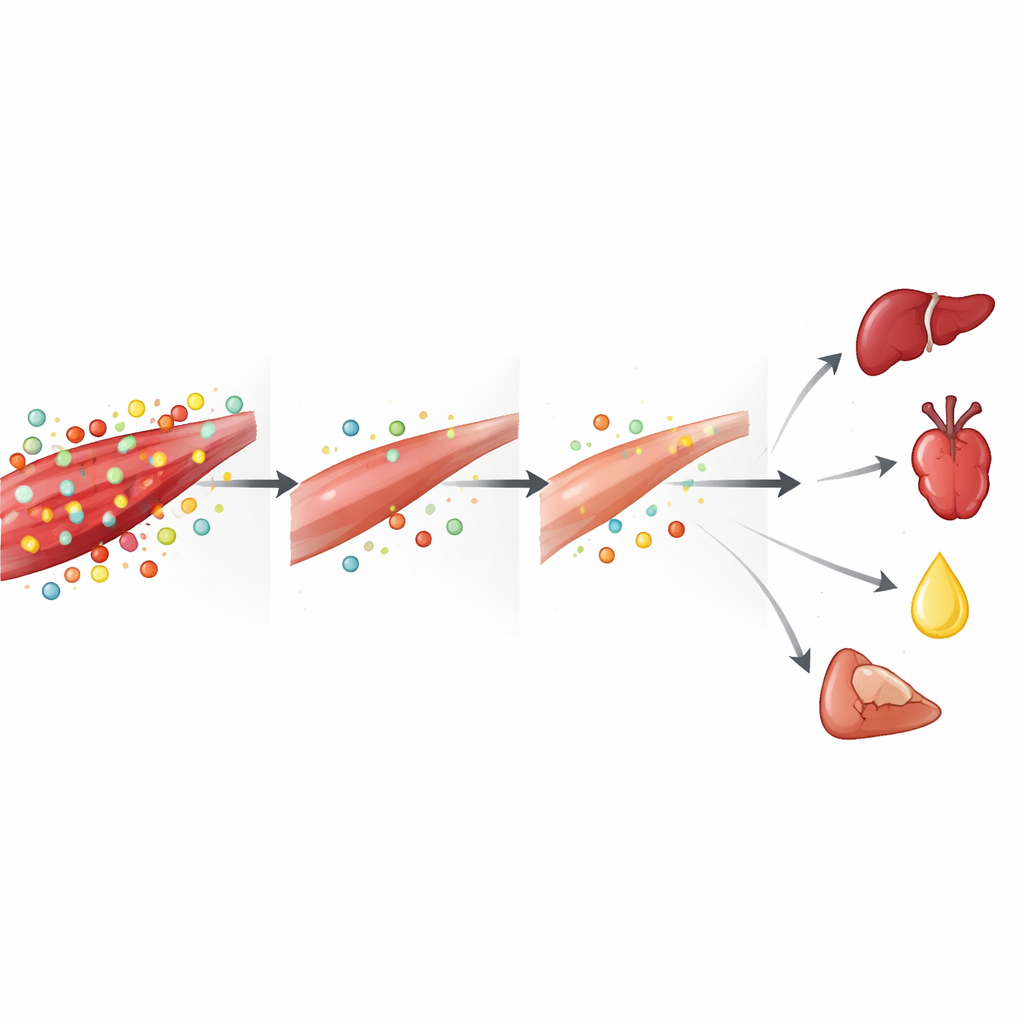
Implications pour les patients et les thérapies futures
Exprimée en termes courants, l’étude décrit l’IRA comme un événement métabolique de « vidage » pour l’organisme : le muscle squelettique dégrade ses réserves de protéines et d’antioxydants pour aider à alimenter et protéger les organes vitaux, laissant les muscles eux‑mêmes à court de carburant et de défenses. Cela aide à expliquer pourquoi les personnes ayant une atteinte rénale sévère sont sujettes à la fonte musculaire, à la faiblesse et à une récupération fonctionnelle médiocre. Cela ouvre aussi la possibilité qu’un soutien nutritionnel ciblé — en particulier des acides aminés et des composés qui renforcent les systèmes glutathion et créatine‑phosphocréatine — puisse un jour aider à protéger à la fois les reins et les muscles lors d’une maladie aiguë. Bien que ces résultats proviennent de souris et reposent sur des instantanés chimiques plutôt que sur des traçages directs des flux, ils fournissent une cartographie détaillée de la façon dont la chimie musculaire est perturbée par la lésion rénale et orientent vers de nouvelles stratégies pour préserver la force et améliorer les résultats lorsque les reins font défaut soudainement.
Citation: Li, A.S., Baker, P.R., Park, S. et al. Metabolomic assessment reveals depletion of amino acids and energy metabolites in skeletal muscle after ischemic acute kidney injury in mice. Sci Rep 16, 8823 (2026). https://doi.org/10.1038/s41598-026-37424-y
Mots-clés: insuffisance rénale aiguë, métabolisme du muscle squelettique, épuisement des acides aminés, stress oxydatif, métabolomique