Clear Sky Science · fr
Analyse de la fonction cardiaque systolique chez des souris dépourvues de PERM1 à partir de cohortes animales importantes
Pourquoi les petits cœurs de souris comptent pour la santé humaine
L’insuffisance cardiaque est souvent décrite comme une pompe fatiguée, mais ce qui affaiblit réellement un cœur est étonnamment complexe. Dans cette étude, des scientifiques ont utilisé un groupe de souris exceptionnellement large pour poser une question ciblée : l’inactivation d’un gène unique appelé PERM1, connu pour aider les cellules cardiaques à produire de l’énergie, modifie-t-elle aussi la force de contraction du cœur ? En scannant soigneusement le cœur de plus de 170 souris, ils montrent que ce gène modifie subtilement la morphologie cardiaque et réduit sa force d’éjection, alors que les animaux restent en grande partie apparemment sains. Leurs résultats contribuent à trancher un débat dans le domaine et fournissent une feuille de route pour concevoir de meilleures expériences cardiaques à l’avenir.
Un gène qui relie l’utilisation du carburant à la contraction
PERM1 a été identifié initialement comme un interrupteur augmentant la production d’énergie dans les cellules musculaires, y compris cardiaques. Des travaux antérieurs ont montré que les niveaux de PERM1 diminuent dans les cœurs en insuffisance, chez la souris comme chez l’humain, ce qui suggère que de faibles niveaux de PERM1 pourraient contribuer à des battements plus faibles. Mais les études utilisant des souris knock-out pour PERM1 — des animaux génétiquement dépourvus de ce gène — ont donné des réponses contradictoires quant à savoir si leurs cœurs pompaient réellement moins efficacement. Parce que PERM1 est envisagé comme une cible possible pour de nouvelles thérapies de l’insuffisance cardiaque, les auteurs ont cherché à tester son impact sur la fonction cardiaque avec suffisamment d’animaux et des statistiques rigoureuses pour obtenir une réponse claire oui/non.
Un regard à grand effectif sur de petits cœurs
L’équipe a rassemblé des données d’échocardiogramme — la même technique par ultrasons utilisée en cardiologie clinique — pour chaque souris knock-out PERM1 et son compagnon de portée sain utilisé dans leur laboratoire sur une période rétrospective de 18 mois. Cette collecte a produit 84 animaux normaux (type sauvage) et 88 knock-out, un effectif bien plus important que ce qui est habituel dans les études cardiaques sur souris. À partir des images échographiques, ils ont mesuré des indicateurs standards du fonctionnement du ventricule gauche, la principale chambre de pompage. Le chiffre clé était la fraction d’éjection, le pourcentage de sang expulsé à chaque battement, ainsi que des mesures connexes telles que l’amplitude de réduction du diamètre ventriculaire à la contraction, l’épaisseur des parois et le volume total de sang éjecté par minute.
Contraction plus faible, chambre plus grande, débit similaire
Les résultats montrent un schéma cohérent. En moyenne, la fraction d’éjection est passée d’environ 65 % chez les souris normales à 54 % chez les knock-out PERM1, une différence d’ampleur cliniquement significative chez l’humain et soutenue par des statistiques très robustes. D’autres mesures de contraction, comme le raccourcissement fractionnel et l’épaississement pariétal, ont également diminué. Parallèlement, les ventricules gauches des knock-out étaient visiblement plus volumineux, surtout en fin de contraction, ce qui indique qu’un volume sanguin plus important restait dans la chambre. Malgré cette contraction plus faible, le volume total de sang pompé par minute a chuté seulement légèrement — d’environ 6 % — car les chambres agrandies pouvaient contenir plus de sang au départ. Autrement dit, le cœur compense partiellement une mauvaise contraction en étirant sa chambre principale.
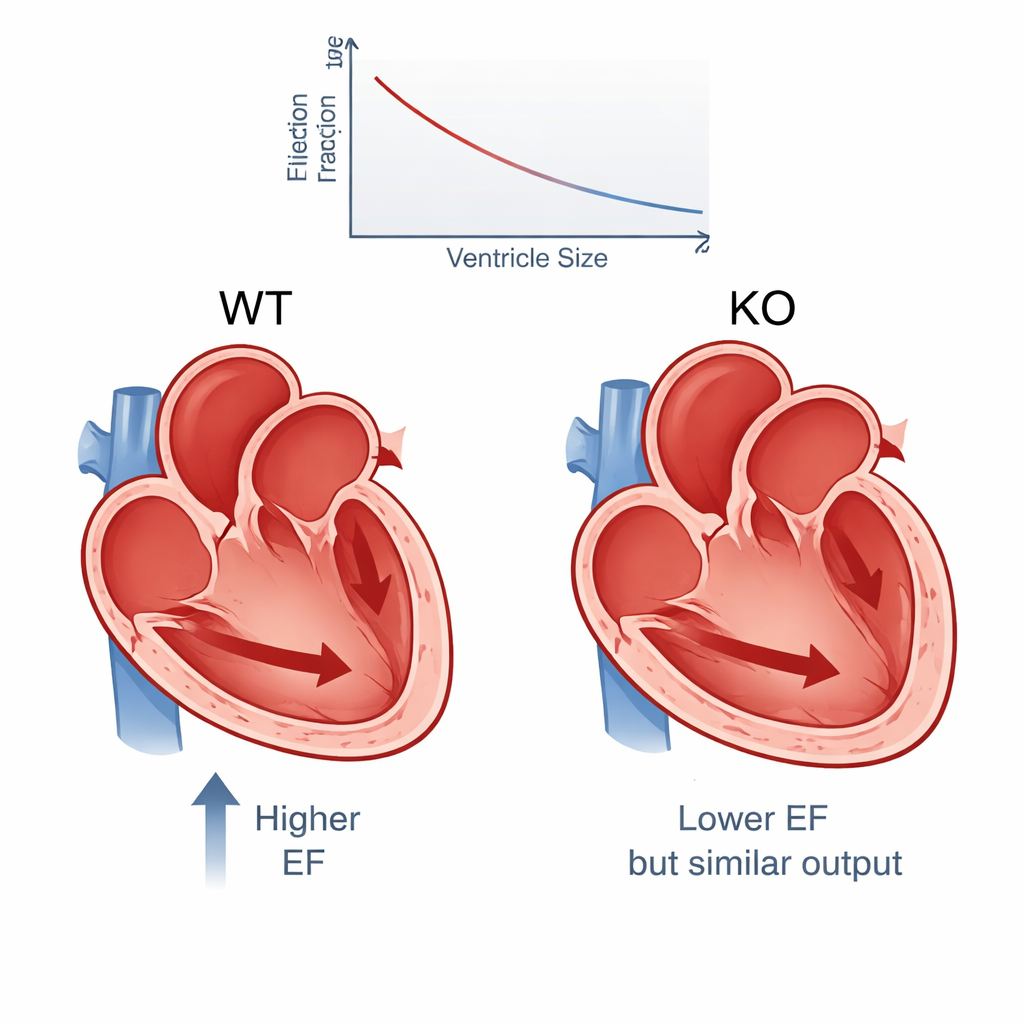
Diversité cachée au sein de cœurs « identiques »
Parce que l’étude comprenait tant d’animaux, les chercheurs ont pu aller au-delà des moyennes et étudier la variation entre cœurs individuels. Même chez des souris saines génétiquement identiques, ils ont observé une répartition étonnamment large de la fraction d’éjection. La suppression de PERM1 a déplacé l’ensemble de la distribution vers le bas — davantage de cœurs avec une force d’éjection plus faible — mais n’a pas élargi la dispersion elle-même. Environ 7 % des souris knock-out avaient des fractions d’éjection inférieures à 40 %, un niveau qui correspondrait à une insuffisance cardiaque avec fraction d’éjection réduite chez l’humain, et pourtant ces souris conservaient un débit sanguin proche de la normale. Les analyses statistiques ont montré que le sexe, l’âge et le poids corporel n’expliquaient qu’une petite partie de la variabilité ; la plupart des différences proviennent probablement de facteurs biologiques plus difficiles à mesurer, comme des influences environnementales subtiles ou des changements épigénétiques.
Ce que cela signifie pour la recherche cardiaque future
Pour aider d’autres scientifiques à concevoir de meilleures expériences, les auteurs ont utilisé leur large jeu de données pour calculer combien d’animaux sont généralement nécessaires pour détecter des changements significatifs pour chaque paramètre cardiaque. Ils ont trouvé que les tailles d’échantillon modestes couramment utilisées dans le domaine risquent de manquer des effets réels mais modérés, en particulier pour des mesures subtiles comme le volume d’éjection systolique ou le débit cardiaque. Dans l’ensemble, l’étude plaide fortement en faveur du fait que la perte de PERM1 provoque un remodelage spécifique du cœur — chambres plus grandes, contraction plus faible — plutôt qu’une défaillance franche, et que ce remodelage est partiellement compensé par des modifications structurelles qui aident à préserver le flux sanguin. Pour les non-spécialistes, la conclusion est qu’un seul gène régulateur de l’énergie peut pousser le cœur vers un nouveau mode de fonctionnement, qui paraît sain à l’extérieur mais comporte des changements discrets dans la structure de la pompe et son effort de travail.
Citation: Zaitsev, A.V., Sreedevi, K., Goode, B. et al. Analysis of systolic cardiac function in PERM1-knockout mice using large cohorts of animals. Sci Rep 16, 7705 (2026). https://doi.org/10.1038/s41598-026-37420-2
Mots-clés: insuffisance cardiaque, contractilité cardiaque, énergétique mitochondriale, modèles murins, échocardiographie