Clear Sky Science · fr
Identification et caractérisation des biomarqueurs liés aux fibroblastes et des sous-populations pro-inflammatoires dans la parodontite par analyse transcriptomique intégrée et analyse unicellulaire
Pourquoi vos gencives comptent au-delà de votre sourire
Des gencives qui saignent et des dents mobiles peuvent sembler des problèmes mineurs, mais la maladie gingivale chronique — appelée parodontite — peut endommager l’os de la mâchoire, provoquer une perte dentaire et est associée à des affections comme les maladies cardiaques et le diabète. Cette étude examine de près un groupe de cellules souvent négligé dans les gencives, les fibroblastes, pour comprendre comment elles favorisent ou apaisent l’inflammation. En combinant de larges jeux de données génétiques et l’analyse unicellulaire, les chercheurs mettent au jour de nouveaux signaux d’alerte et des types cellulaires qui pourraient améliorer le diagnostic et le traitement de la maladie parodontale.
Acteurs cachés des gencives douloureuses
Les fibroblastes sont les cellules ouvrières qui construisent et entretiennent le tissu conjonctif qui maintient les dents en place. Pendant des années, on les a surtout considérés comme un « échafaudage » structurel. Cette recherche montre qu’ils sont bien plus : les fibroblastes peuvent fonctionner comme des centres de contrôle miniatures de l’inflammation. Lorsque les bactéries perturbent l’équilibre microbien normal de la bouche, les fibroblastes réagissent en libérant des messagers chimiques qui attirent les cellules immunitaires et peuvent soit aider à réparer les tissus, soit intensifier les lésions. Les auteurs se sont concentrés sur l’identification de signes génétiques liés aux fibroblastes qui diffèrent entre gencives saines et parodontite, et sur la détection de sous-groupes de fibroblastes devenant particulièrement inflammatoires dans les tissus malades.
Examiner le tissu gingival cellule par cellule
Pour cela, l’équipe a exploité plusieurs grands jeux de données d’expression génique provenant de patients ayant des gencives saines ou une parodontite, ainsi qu’un jeu de données unicellulaire moderne profilant des milliers de cellules individuelles. Ils ont d’abord cartographié les principaux types cellulaires du tissu gingival — comme les cellules immunitaires, les cellules des vaisseaux sanguins et les fibroblastes — et confirmé que le nombre et l’activité des fibroblastes étaient plus élevés dans les gencives malades. Ils ont ensuite recherché des gènes qui étaient à la fois altérés dans la parodontite et spécifiquement associés aux fibroblastes. En utilisant une méthode statistique qui réduit aux caractéristiques les plus informatives, ils ont identifié six gènes clés liés aux fibroblastes dont le profil d’activité combiné distinguait de manière fiable la parodontite de la santé à travers plusieurs cohortes de patients.
Schémas de risque et « personnalités » immunitaires de la maladie gingivale
Avec ces six gènes, les chercheurs ont construit un modèle diagnostique performant pour séparer les échantillons malades des sains, et l’ont traduit en un graphique de score simple — appelé nomogramme — qui pourrait, en principe, estimer le risque individuel. En regroupant les patients selon l’intensité d’expression de ces gènes fibroblastiques, trois formes distinctes de parodontite sont apparues. Une forme présentait un paysage immunitaire fortement inflammatoire, riche en lymphocytes T agressifs et en macrophages en « mode attaque ». Une seconde forme était dominée par des cellules qui atténuent les réponses immunitaires, suggérant un environnement plus suppressif. Une troisième forme se situait entre les deux, avec un mélange plus équilibré ou au repos de cellules immunitaires. Ces schémas suggèrent que la maladie gingivale n’est pas uniforme — et que les fibroblastes participent à façonner ces différentes « personnalités » inflammatoires.
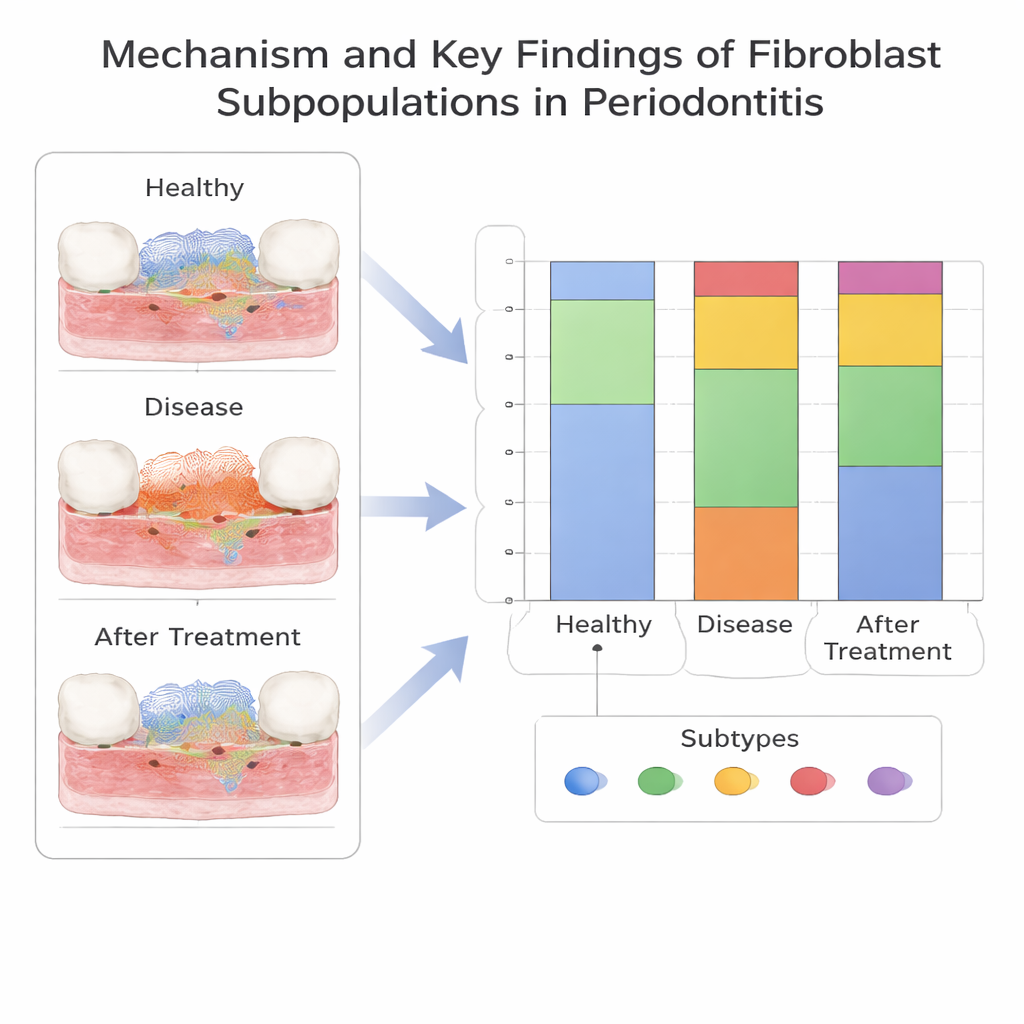
Un nouveau sous-type de fibroblaste pro-inflammatoire
En approfondissant l’analyse unicellulaire, l’équipe a divisé les fibroblastes en cinq sous-types selon leur activité génétique. Un sous-type, marqué par un gène appelé CXCL13, s’est démarqué car il était beaucoup plus fréquent dans la parodontite que dans les gencives saines. Ce groupe de fibroblastes CXCL13-positifs apparaissait tôt le long d’un parcours développemental et était lié à des signaux attirant les cellules immunitaires et remodelant la matrice tissulaire — des caractéristiques cohérentes avec un rôle pro-inflammatoire marqué. En revanche, un autre sous-type de fibroblastes était enrichi dans les tissus sains et pourrait contribuer à maintenir la stabilité de l’environnement gingival. Les auteurs ont confirmé dans des échantillons de patients que certains gènes liés aux fibroblastes, en particulier SELL, et les fibroblastes CXCL13-positifs eux-mêmes, étaient effectivement plus élevés dans les gencives malades, renforçant ainsi les résultats computationnels.
Ce que cela signifie pour les soins gingivaux futurs
Concrètement, l’étude révèle que certains fibroblastes de vos gencives agissent comme des accélérateurs de l’inflammation, tandis que d’autres jouent plutôt le rôle de freins ou d’équipes de réparation. En identifiant des marqueurs génétiques précis et un sous-groupe de fibroblastes pro-inflammatoires distinct, ce travail ouvre la voie à des tests plus précis permettant de détecter la parodontite plus tôt et de façon plus fiable. Il suggère également que de futurs traitements pourraient cibler ces voies spécifiques pilotées par les fibroblastes — en réduisant les sous-ensembles dommageables comme les fibroblastes CXCL13-positifs ou en renforçant les sous-types protecteurs — pour mieux maîtriser l’inflammation gingivale et potentiellement en limiter l’impact sur la santé globale.
Citation: Huang, M., Lin, Y., Wu, Z. et al. Identification and characterization of fibroblast-related biomarkers and pro-inflammatory subpopulations in periodontitis by integrated transcriptomic and single-cell analysis. Sci Rep 16, 6223 (2026). https://doi.org/10.1038/s41598-026-37385-2
Mots-clés: parodontite, fibroblastes, inflammation des gencives, séquençage ARN unicellulaire, biomarqueurs