Clear Sky Science · fr
Modèles généralisés de vaisseaux sanguins pour l’oncologie par nanoparticules magnétiques : propriétés géométriques et microfluidiques
Guider de minuscules aimants dans le corps
Imaginez pouvoir attirer des médicaments anticancéreux directement dans une tumeur à l’aide d’un aimant, épargnant ainsi le reste du corps des effets secondaires agressifs. Cette étude examine comment de minuscules particules magnétiques circulent dans des réseaux ressemblant à des vaisseaux sanguins et pose une question apparemment simple : dans des conditions d’écoulement réalistes, les aimants peuvent-ils réellement diriger ces particules là où les médecins le souhaitent ?
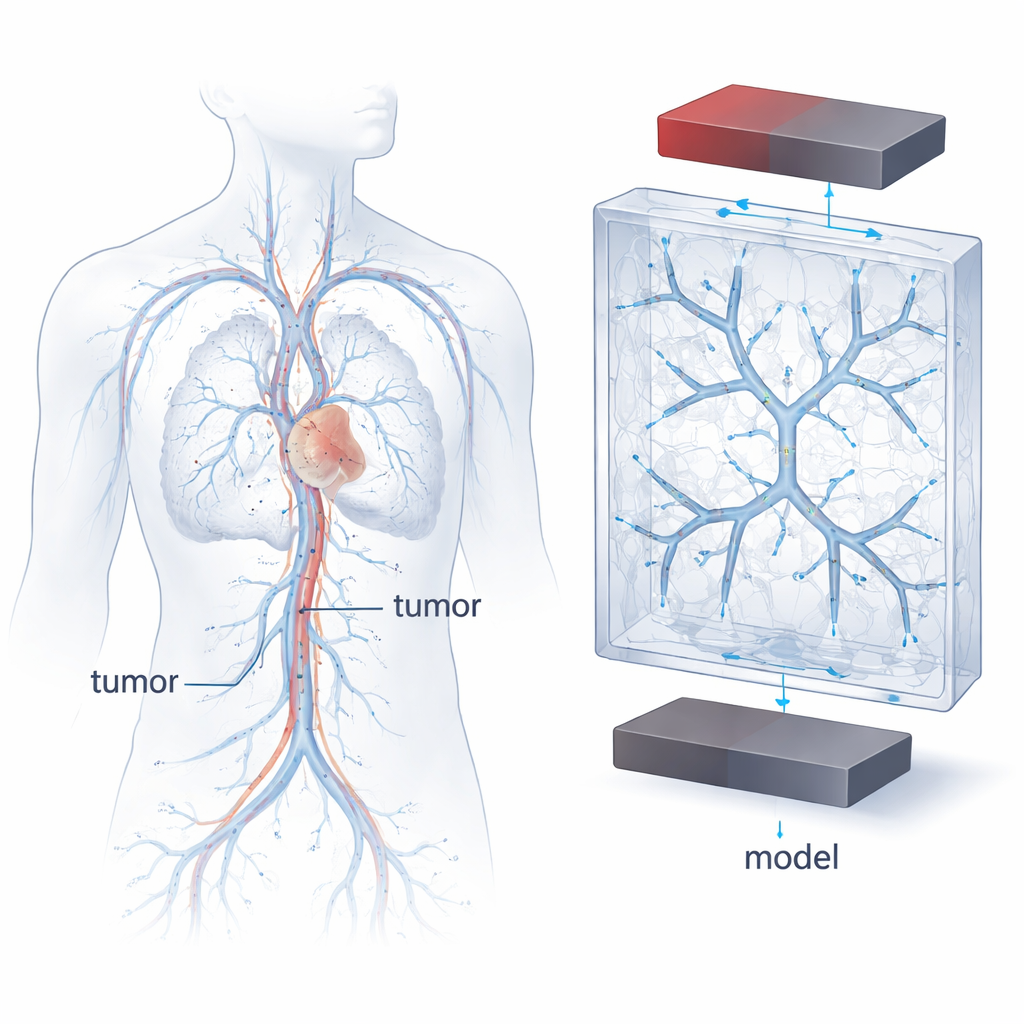
Pourquoi la géométrie des vaisseaux et l’écoulement importent
Les thérapies magnétiques contre le cancer reposent sur des nanoparticules d’oxyde de fer superparamagnétiques — SPIONs — que l’on peut attirer avec un champ magnétique pendant qu’elles transportent des médicaments dans le sang. Mais les vaisseaux sanguins ne sont pas de simples tubes droits : ils se ramifient, se rétrécissent, se courbent et se divisent, et la vitesse du sang augmente ou diminue en conséquence. Ces variations de forme et de vitesse affectent le mouvement des particules, leur zone de concentration et la durée pendant laquelle elles restent en contact avec la paroi, condition nécessaire pour y adhérer. Les vaisseaux sanguins réels des patients sont extrêmement variables, ce qui rend difficile la comparaison des expériences ou la prédiction du comportement d’une nouvelle thérapie. Les auteurs ont donc cherché à construire une « vascularisation modèle » hautement contrôlée et reproductible qui capture néanmoins les caractéristiques essentielles des vaisseaux alimentant les tumeurs.
Construire des réseaux sanguins tumoraux idéalisés
Pour concevoir ces vaisseaux modèles, l’équipe s’est appuyée sur des règles classiques décrivant la manière dont les artères réelles se ramifient. L’une de ces règles, la loi de Murray, relie les diamètres des vaisseaux parents et fils dans un réseau économe en énergie. En utilisant des mesures cliniques issues de tumeurs mammaires et ces lois d’échelle, les chercheurs ont généré mathématiquement des arbres ramifiés imitant la réduction progressive des vaisseaux alimentant la tumeur jusqu’au lit capillaire. Ils ont ensuite utilisé l’impression 3D haute résolution pour intégrer des réseaux de canaux creux comportant deux, trois ou quatre niveaux de branchement à l’intérieur de blocs plastiques transparents. Les canaux suivaient un schéma de branchement symétrique et s’étendaient en trois dimensions, offrant un paysage simplifié mais inspiré de la physiologie pour étudier le mouvement des particules.
Observer les particules magnétiques en action
À travers ces réseaux imprimés, l’équipe a fait circuler de l’eau comme substitut du sang, puis injecté en amont un fluide contenant des SPIONs et appliqué un champ magnétique statique autour du modèle. Des images à grande vitesse ont fourni un enregistrement quasi cinématographique des nuages de particules sombres traversant les différentes branches, tandis qu’une analyse informatique a converti les changements de luminosité en signaux temporels reflétant la présence locale de particules. En faisant varier le débit d’écoulement, la concentration en particules, la complexité du branchement et la présence ou non d’un aimant, les chercheurs ont pu dissocier l’impact de chaque facteur sur la distribution des particules, leur temps de résidence et leur dépôt éventuel sur les parois des canaux.
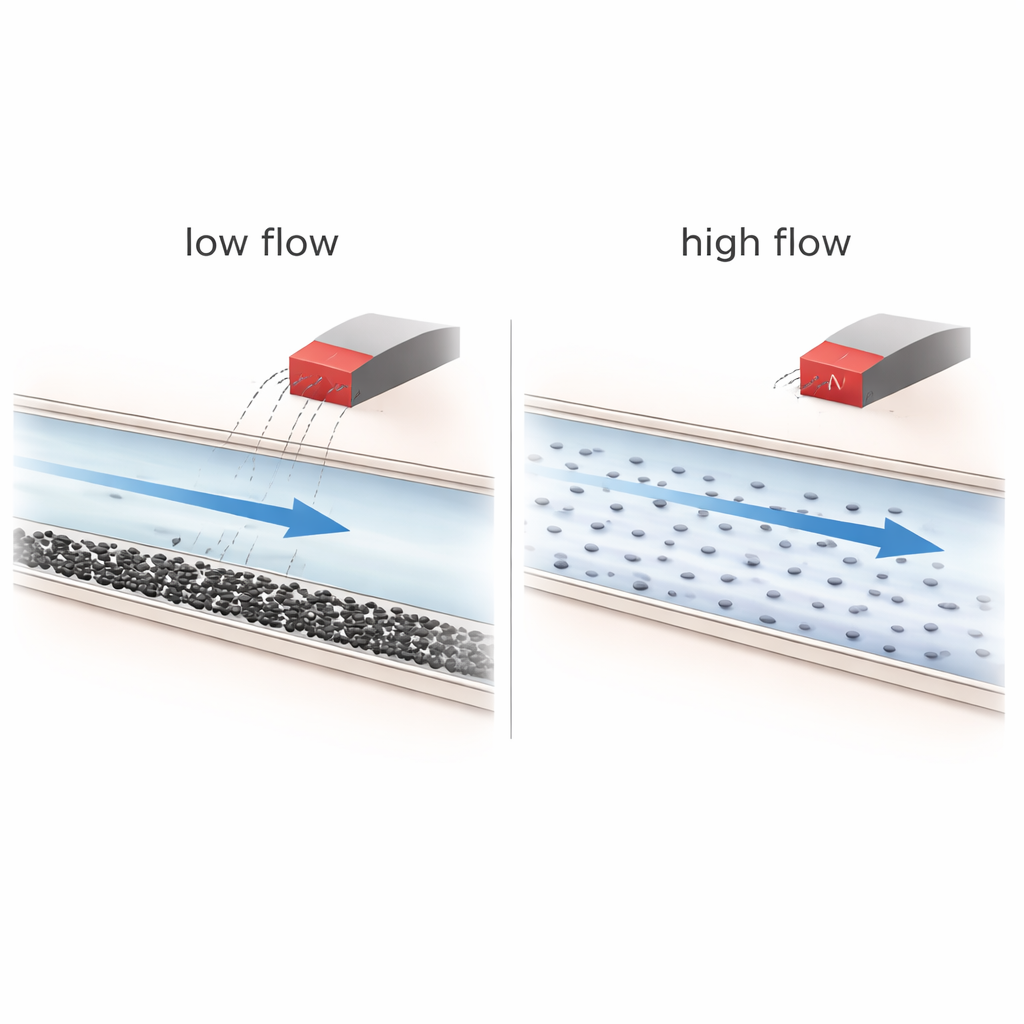
Quand les aimants aident — et quand ils ne le font pas
Les expériences montrent que ce sont les conditions d’écoulement qui dominent. À des débits plus élevés, le fluide est bien mélangé et les nanoparticules circulent rapidement ; dans ces conditions, le champ magnétique a presque aucune influence et les particules suivent simplement les lignes de courant à travers le réseau. À faible débit, cependant, la gravité et les effets de concentration provoquent un dépôt des particules vers le bas des canaux, formant des couches stratifiées et parfois des agrégats lâches. Dans cette situation déjà inégale, l’aimant peut orienter davantage de particules vers certaines branches et prolonger légèrement leur temps de résidence, en particulier dans des réseaux plus complexes et fortement ramifiés. Pourtant, les calculs montrent que la force magnétique sur une seule particule de 40 nanomètres est de beaucoup d’ordres de grandeur inférieure à la traînée visqueuse exercée par le liquide en écoulement, rendant le « guidage » d’une particule isolée physiquement irréaliste dans les conditions testées.
Ce que cela signifie pour les thérapies anticancer futures
Pour un non-spécialiste, la conclusion principale est que les aimants seuls ne peuvent pas de manière fiable extraire des nanoparticules en suspension libre d’un courant sanguin rapide. Des effets magnétiques remarquables n’apparaissent que lorsque les particules ont déjà ralenti, se sont déposées ou ont formé des agrégats — des situations qui amplifient effectivement leur réponse magnétique. Les modèles de vaisseaux généralisés imprimés en 3D présentés ici offrent une façon standardisée d’explorer ces effets à travers différentes géométries de réseau et régimes d’écoulement. Pour le ciblage magnétique des médicaments à l’avenir, ce travail suggère que des stratégies réussies devront probablement exploiter des comportements collectifs — tels que l’agrégation contrôlée ou des systèmes vecteurs — plutôt que de s’appuyer sur le guidage d’un seul nanoparticule à travers de grands vaisseaux fortement perfusés.
Citation: Fleischhauer, D., Schlicht, S. & Drummer, D. Generalized blood vessel models for magnetic nanoparticle-based oncology: geometric and microfluidic properties. Sci Rep 16, 3701 (2026). https://doi.org/10.1038/s41598-026-37348-7
Mots-clés: ciblage magnétique de médicaments, nanoparticules, vasculature tumorale, modèles microfluidiques, administration de médicaments