Clear Sky Science · fr
Cibler l’axe Akt–EphA2 et l’adhésion cellule–cellule augmente la sensibilité à l’anoïkis des cellules cancéreuses
Pourquoi les cellules cancéreuses en suspension comptent
Lorsque des cellules cancéreuses se détachent d’une tumeur et circulent dans le sang, elles devraient normalement mourir parce qu’elles perdent l’ancrage au tissu environnant. Ce mécanisme de sécurité intégré, appelé mort cellulaire induite par le détachement, empêche normalement des tissus de se développer là où ils ne devraient pas. Les cellules métastatiques, cependant, apprennent souvent à ignorer ce signal et restent viables en suspension, ce qui facilite leur capacité à former de nouvelles tumeurs. Cette étude pose une question apparemment simple : si l’on restaure un « sens du toucher » mécanique clé chez des cellules de cancer du sein agressives, peut‑on forcer ces cellules errantes à mourir, et si ce n’est pas le cas, quels subterfuges de secours utilisent‑elles pour survivre ?
Réanimer un sens du toucher perdu
Les cellules évaluent en permanence la rigidité de leur environnement en tirant sur les structures qui les ancrent. Dans un tissu sain, la perte de contact ou l’atterrissage sur une surface très molle déclenche souvent l’autodestruction. La tropomyosine 2.1 (Tpm2.1) est une composante importante de cette machinerie de tension interne et fait souvent défaut ou est diminuée dans les cellules cancéreuses. Les chercheurs ont utilisé une lignée cellulaire de cancer du sein métastatique largement étudiée et l’ont modifiée afin d’exprimer davantage de Tpm2.1, restaurant ainsi une grande partie de cette détection de rigidité. Lorsque ces cellules modifiées ont été contraintes de pousser dans des boîtes spéciales anti‑adhésives qui les empêchent de s’attacher, elles ont effectivement manifesté plus de mortalité cellulaire, une croissance plus lente et une mobilité réduite par rapport aux cellules non modifiées. Pourtant, même après plusieurs jours en suspension, environ 70 % des cellules exprimant Tpm2.1 étaient encore vivantes, ce qui suggère que la restauration seule du sens du toucher ne résout pas complètement le problème.
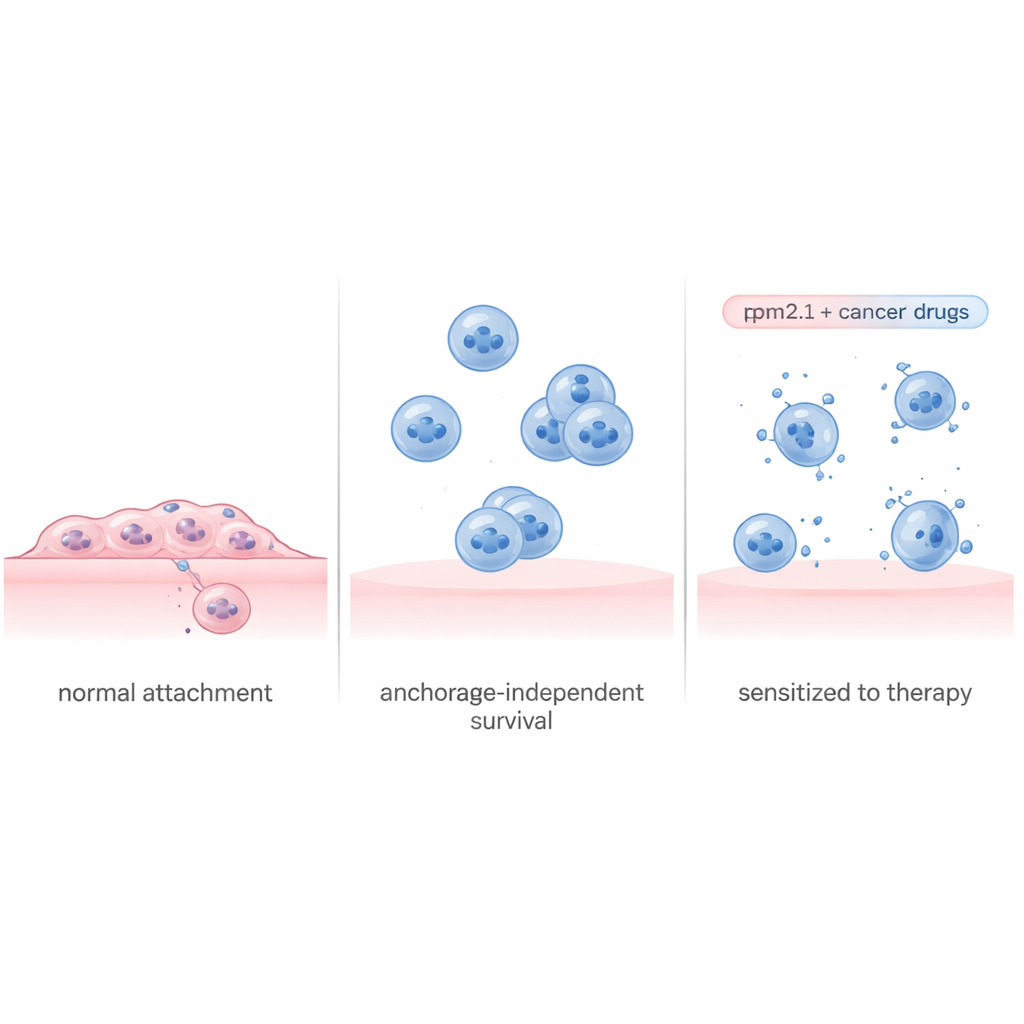
Lire le manuel de survie des cellules cancéreuses
Pour comprendre pourquoi certaines cellules mouraient tandis que d’autres survivaient, l’équipe a séparé les cellules Tpm2.1 en suspension en deux groupes : celles montrant des signes précoces de mort cellulaire et celles paraissant saines. Ils ont ensuite mesuré les gènes activés ou réprimés dans chaque groupe sur quatre jours. Les cellules en train de mourir montraient une vaste mise hors service des programmes impliqués dans la division cellulaire, la réparation de l’ADN et l’adhésion, accompagnée de signaux de stress ressemblant à une voie à sens unique vers l’autodestruction. En revanche, les cellules survivantes ont lancé un plan de survie coordonné. Peu après le détachement, elles ont activé des voies inflammatoires et liées à l’immunité, puis ont intensifié des circuits majeurs de croissance et de survie, y compris une voie bien connue centrée sur la protéine Akt. Simultanément, elles ont fortement augmenté l’expression des gènes favorisant l’adhésion cellule–cellule, ce qui leur permet de former des amas protecteurs même sans s’accrocher à la matrice environnante.
La force du nombre : comment les amas cellulaires résistent à la mort
Parce que les données transcriptomiques indiquaient une augmentation de l’adhésion cellule–cellule, les chercheurs ont testé si un simple regroupement pouvait aider les cellules à survivre en suspension. Lorsque les cellules exprimant Tpm2.1 étaient cultivées à forte densité, facilitant la formation d’amas, beaucoup moins de cellules mouraient que lorsqu’elles étaient maintenues clairsemées. Une molécule d’adhésion, ICAM1, s’est particulièrement distinguée par son élévation chez les cellules survivantes et est déjà connue pour favoriser la formation et l’accrochage d’amas de cellules tumorales circulantes dans des tissus distants. Bloquer ICAM1 avec un inhibiteur de petite molécule a augmenté la mortalité des cellules exprimant Tpm2.1 en suspension, tout en ayant peu d’effet sur les cultures classiques en position adhérente. Ces résultats soutiennent l’idée que, une fois leur mécanique interne partiellement restaurée, les cellules cancéreuses peuvent encore échapper à la mort en se tenant littéralement les unes aux autres plutôt qu’à leur environnement.
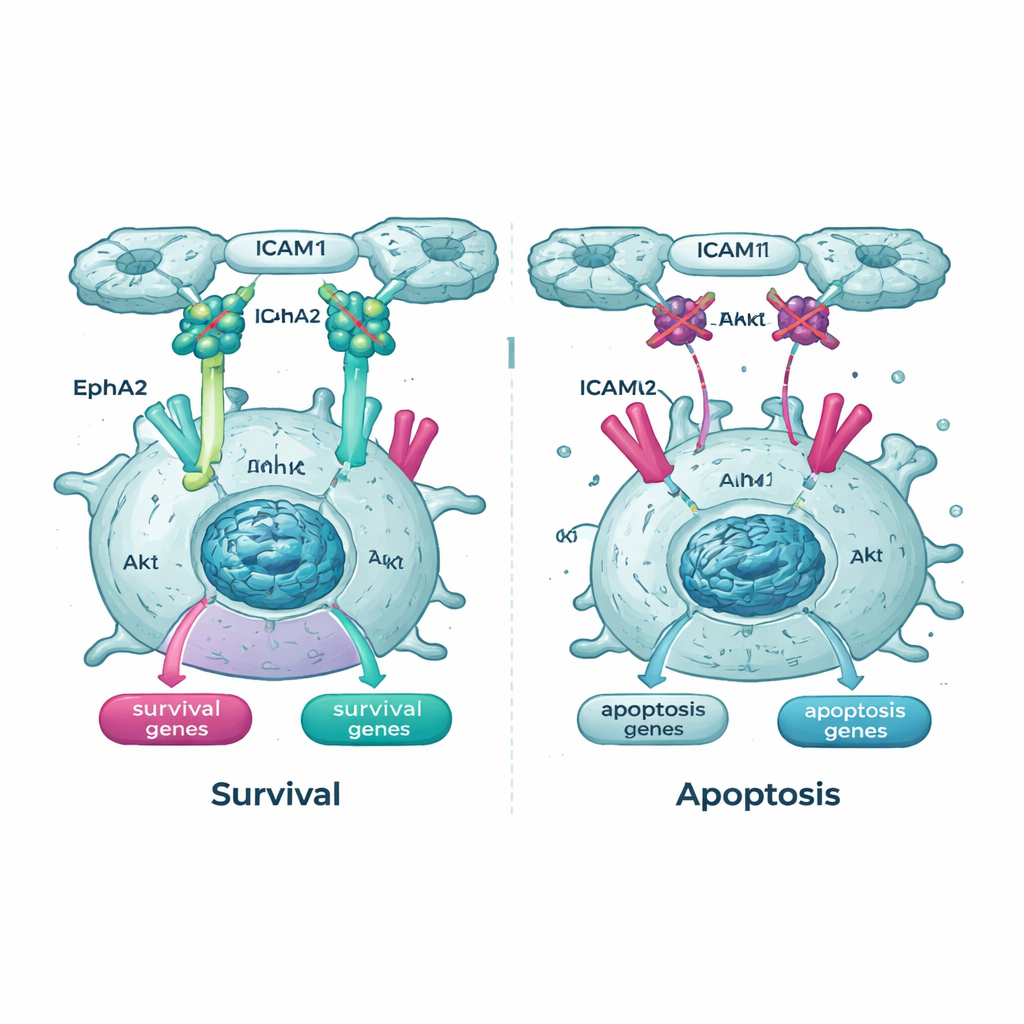
Sectionner des lignes de vie clés à l’intérieur de la cellule
Les analyses génétiques ont également mis en lumière la voie Akt et l’un de ses partenaires, un récepteur appelé EphA2, comme des lignes de vie importantes pour les cellules cancéreuses en suspension. Dans les cellules exprimant Tpm2.1, la forme active et phosphorylée d’Akt était plus faible en suspension que dans les cellules témoins, et les niveaux et l’activité d’EphA2 étaient également réduits. Lorsque l’équipe a traité les cellules avec des médicaments bloquant Akt ou EphA2, tant les cellules normales que celles exprimant Tpm2.1 sont devenues beaucoup plus susceptibles de mourir en suspension. Il est notable que les cellules dont la détection de rigidité avait été restaurée étaient particulièrement sensibles à ces médicaments au fil du temps, ce qui suggère qu’une fois leurs contrôles mécaniques partiellement réengagés, elles dépendent davantage des signaux de survie restants.
Transformer un état prédisposé en une faiblesse létale
Pour un non‑spécialiste, le message principal est que réparer un interrupteur de sécurité défaillant chez les cellules cancéreuses — leur capacité à sentir et répondre à la perte de contact — est nécessaire mais insuffisant pour les pousser à l’autodestruction. Les cellules qui survivent le font en s’unissant et en réorientant leurs connexions internes via des voies alternatives de croissance et de survie. Ce travail montre que la restauration de la détection de rigidité par Tpm2.1 place les cellules métastatiques du sein dans un état « prédisposé » où elles sont plus proches de la mort mais pas encore engagées. En bloquant alors la voie Akt–EphA2 et en perturbant l’adhésion cellule–cellule via ICAM1, les chercheurs peuvent pousser ces cellules prédisposées au‑delà du seuil et augmenter fortement la mort induite par le détachement. En termes pratiques, l’étude propose une stratégie pour de futures thérapies combinées visant à éliminer les cellules tumorales en suspension avant qu’elles ne puissent former de nouvelles métastases.
Citation: Vivante, A.G., Dwivedi, N., Sheetz, M.P. et al. Targeting the Akt–EphA2 axis and cell–cell adhesion enhances anoikis sensitivity in cancer cells. Sci Rep 16, 6197 (2026). https://doi.org/10.1038/s41598-026-37327-y
Mots-clés: métastase du cancer du sein, adhésion cellulaire, anoïkis, signalisation Akt, détection de rigidité