Clear Sky Science · fr
La lumière LED violette et la glycérine brute améliorent de façon synergétique la production d’astaxanthine chez Aurantiochytrium limacinum
Pourquoi des microbes lumineux pourraient vous concerner
Des composés colorés venus du monde microscopique transforment discrètement notre façon de produire des compléments nutritionnels, des cosmétiques et même de l’alimentation pour poissons. Cette étude examine comment un minuscule organisme marin, Aurantiochytrium limacinum, peut être stimulé par une lumière LED violette et des sous‑produits industriels bon marché pour fabriquer des molécules de grande valeur comme l’astaxanthine — un puissant antioxydant rouge que l’on trouve aussi dans le saumon et les crevettes — en parallèle d’huiles oméga‑3 bénéfiques telles que le DHA. Ce travail ouvre la voie à des méthodes de production plus durables et moins coûteuses pour ces ingrédients, sans dépendre des poissons sauvages ni d’usines chimiques énergivores.
Une toute petite usine venue de la mer
Aurantiochytrium limacinum est un protiste marin microscopique qui prospère dans l’obscurité et se nourrit de carbone organique plutôt que de lumière solaire. Il intéresse l’industrie parce qu’il peut produire simultanément deux produits de valeur : le DHA, un acide gras oméga‑3 important pour le cerveau et le cœur, et des caroténoïdes, les pigments responsables des couleurs jaunes, orange et rouges chez de nombreuses plantes et animaux. Parmi ces caroténoïdes, l’astaxanthine se distingue par ses fortes propriétés antioxydantes et anti‑inflammatoires, ce qui a suscité une demande croissante dans les compléments, les aliments fonctionnels et les soins de la peau. Jusqu’à présent, la majorité de l’astaxanthine provenait soit de l’huile de poisson, soit d’une synthèse chimique énergivore, deux voies qui posent des problèmes de durabilité et de sécurité.
Choisir la bonne couleur de lumière
Les chercheurs ont étudié comment différentes couleurs de lumière — obscurité, lumière blanche standard et LED violettes à bande étroite (410–420 nm) — influencent la production de ce microbe. Ils ont cultivé des cultures avec soit du glucose (un sucre simple) soit de la glycérine comme source principale de carbone, puis mesuré la croissance cellulaire, le stockage des lipides et les niveaux de caroténoïdes. Les cellules ont poussé tout aussi bien sous toutes les couleurs de lumière et leur teneur globale en lipides est restée à peu près la même. Ce qui a changé de façon spectaculaire, c’est le mélange de pigments : la lumière violette a conduit aux niveaux les plus élevés de caroténoïdes, suivie de la lumière blanche, l’obscurité produisant le moins. La β‑carotène et la canthaxanthine, pigments orange en amont de la voie de l’astaxanthine, ont fortement augmenté sous lumière violette, en particulier lorsque la glycérine était utilisée comme source de carbone. L’astaxanthine elle‑même était toutefois la plus abondante dans les cultures alimentées au glucose, montrant que la couleur de la lumière et le type d’aliment orientent subtilement jusqu’où la cellule va dans la voie de synthèse des pigments.
Transformer des déchets en couleur et en huile
Un défi majeur pour la commercialisation de ce microbe est le coût de son alimentation. Le glucose est relativement onéreux à l’échelle industrielle, tandis que la production de biodiesel génère de grands volumes de glycérine brute, un sous‑produit de faible valeur parfois difficile à éliminer. Les auteurs ont testé si cette glycérine impure pouvait être suffisamment nettoyée pour servir de matière première utile. Après des traitements simples — dilution, acidification pour éliminer savons et sels, et dans certains cas une étape supplémentaire de polissage sur charbon actif — la glycérine brute a soutenu une croissance microbienne comparable à celle obtenue avec du glucose ou de la glycérine pure. Sous LED violette, les cultures cultivées sur glycérine brute traitée ont produit de hauts niveaux de β‑carotène et de canthaxanthine, puis ont atteint des quantités d’astaxanthine similaires à celles obtenues sur milieux standard, tout en maintenant la production de lipides neutres (huiles).
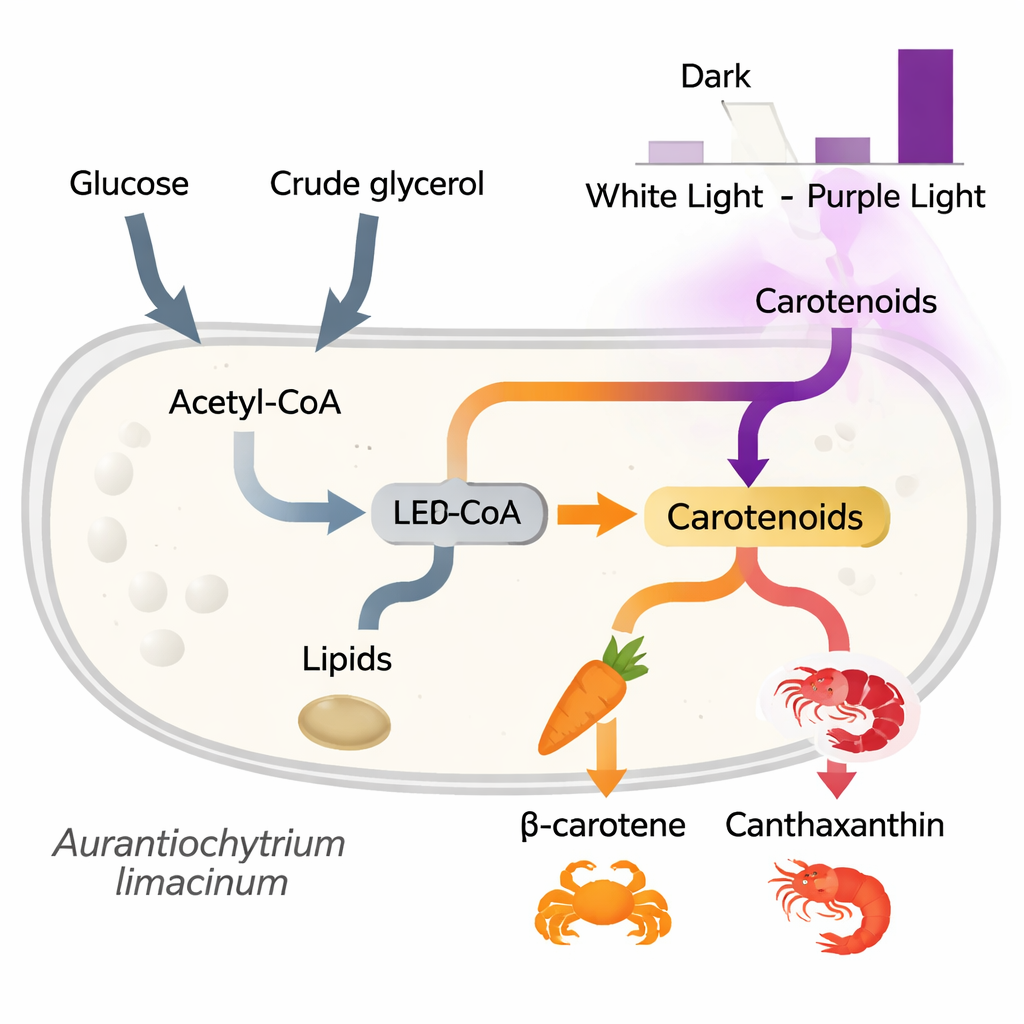
Regarder sous le capot de la cellule
Pour comprendre comment la lumière et le type d’aliment reconfigurent le métabolisme, l’équipe a également examiné quels gènes étaient activés ou réprimés selon les conditions à l’aide du séquençage d’ARN. Ils ont constaté que les gènes impliqués dans l’importation et le traitement de la glycérine étaient fortement activés lorsque la glycérine était la source d’alimentation, confirmant que les cellules peuvent efficacement diriger ce carbone dérivé de déchets vers le métabolisme central. De façon surprenante, de nombreux gènes liés à la synthèse des lipides et des caroténoïdes étaient moins actifs sous lumière violette à un premier point temporel, même si les niveaux de pigments étaient plus élevés par la suite. Ce schéma suggère que les cellules peuvent d’abord atténuer certains processus sous stress lumineux puis augmenter la production de pigments plus tard comme réponse protectrice, utilisant les caroténoïdes comme de véritables « écrans solaires » et antioxydants naturels.
Ce que cela signifie pour les produits futurs
Pour les non‑spécialistes, l’essentiel est que l’ajustement fin à la fois de l’éclairage et de l’alimentation peut transformer un microbe marin en une usine flexible et peu coûteuse d’ingrédients liés à la santé. La lumière LED violette stimule des pigments colorés et protecteurs sans compromettre la production d’huiles bénéfiques, tandis que la glycérine brute modestement purifiée — essentiellement un flux de déchets industriels — peut remplacer des sucres plus coûteux comme source principale d’alimentation. Ensemble, ces stratégies ouvrent la voie à une production d’astaxanthine et de DHA plus verte et plus économique, réduisant la pression sur les pêcheries sauvages et la chimie fossile tout en exploitant la puissance discrète de la biotechnologie microbienne.
Citation: Yamakawa, K., Kawano, K., Kato, S. et al. Purple LED light and crude glycerol synergistically enhance astaxanthin production in Aurantiochytrium limacinum. Sci Rep 16, 6623 (2026). https://doi.org/10.1038/s41598-026-37313-4
Mots-clés: astaxanthine, Aurantiochytrium, lumière LED violette, glycérine brute, bioproduits microbiens