Clear Sky Science · fr
TRMT6 atténue la susceptibilité et la progression de la colite induite par DSS de manière multifacette via une régulation translationnelle
Pourquoi cette étude sur l’intestin est importante
Les maladies inflammatoires de l’intestin (MII) – qui comprennent la maladie de Crohn et la rectocolite hémorragique – touchent des millions de personnes dans le monde et peuvent provoquer des douleurs chroniques, des saignements, une perte de poids et de la fatigue. Au cœur de ces affections se trouve un revêtement intestinal fragile, d’une seule cellule d’épaisseur, qui doit se réparer en permanence tout en retenant des trillions de microbes. Cette étude révèle un “gardien” moléculaire jusque-là sous‑estimé, une protéine nommée TRMT6, qui aide les cellules intestinales à croître, à cicatriser et à gérer leur métabolisme. Comprendre le rôle de TRMT6 pourrait ouvrir la voie à des traitements pour les MII plus ciblés et mieux tolérés.
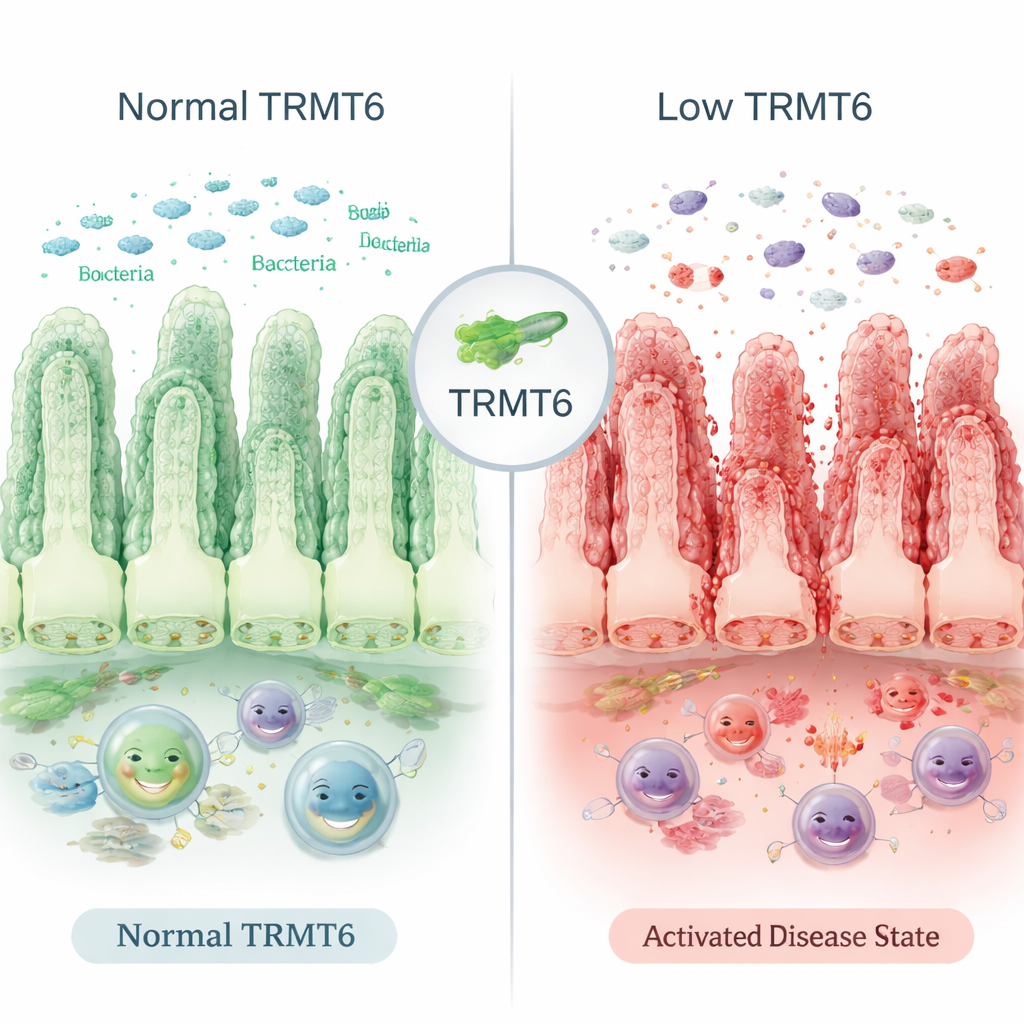
Un gardien microscopique de la paroi intestinale
La surface interne de l’intestin est recouverte d’une seule couche de cellules qui se renouvelle tous les quelques jours. Ce tapis vivant joue le rôle de barrière, séparant les bactéries intestinales des tissus internes de l’organisme. Les chercheurs ont constaté que TRMT6, une enzyme présente dans ces cellules intestinales, est diminuée dans des échantillons de tissus provenant de personnes atteintes de MII active et chez des souris atteintes de colite induite chimiquement. TRMT6 ne modifie pas la séquence d’ADN ; elle modifie subtilement l’ARN — les copies de travail de l’information génétique qui orientent la production des protéines — de façons qui influent sur l’efficacité de la traduction protéique. Quand les niveaux de TRMT6 baissent, ce processus de fabrication des protéines se détériore et la muqueuse intestinale devient plus vulnérable aux dommages.
Que se passe-t-il quand TRMT6 est désactivée
Pour évaluer l’importance de TRMT6, l’équipe a créé des souris chez lesquelles TRMT6 a été supprimée spécifiquement dans les cellules de l’intestin grêle. Dans des conditions normales, ces animaux semblaient en bonne santé et leurs intestins paraissaient en grande partie normaux au microscope. Cependant, lorsque les souris ont été exposées à un produit chimique (DSS) qui irrite l’intestin et est largement utilisé comme modèle de colite, le tableau a changé de façon spectaculaire. Par rapport à leurs congénères normaux, les souris déficientes en TRMT6 ont perdu davantage de poids, avaient des côlons plus courts et plus gonflés et présentaient des lésions plus profondes au niveau de l’intestin grêle. Un second modèle génétique supprimant TRMT6 uniquement dans les cellules souches intestinales — les cellules qui renouvellent en continu l’épithélium — a entraîné une maladie tout aussi sévère, confirmant que l’enzyme est particulièrement critique dans ce compartiment en renouvellement.
Réparation ralentie, métabolisme perturbé et microbiote déréglé
Un examen plus approfondi des tissus intestinaux a révélé pourquoi l’absence de TRMT6 est si délétère pendant la colite. Dans l’intestin lésé, on observait davantage de cellules en apoptose et moins de cellules en prolifération, comme le montrent les colorations histologiques standard. Un régulateur clé de la croissance, la protéine MYC, était nettement réduite au niveau protéique, alors que son message ARN n’avait diminué que modérément. Ce décalage suggère que TRMT6 aide les cellules intestinales à traduire efficacement l’ARN de MYC en protéine, ce qui permet une réparation rapide de la muqueuse. Pour aller plus loin, les chercheurs ont combiné des mesures à grande échelle de l’ARN, des protéines, des petites molécules (métabolites) et de l’ADN bactérien. Ces analyses « multi‑omiques » ont montré que la perte de TRMT6 perturbe des protéines impliquées dans le traitement des lipides et l’absorption des nutriments, modifie les niveaux de nombreuses molécules lipidiques et d’acides organiques dans l’intestin et le sang, et déplace l’équilibre du microbiote intestinal en réduisant plusieurs groupes bénéfiques au profit d’espèces plus associées à l’inflammation.
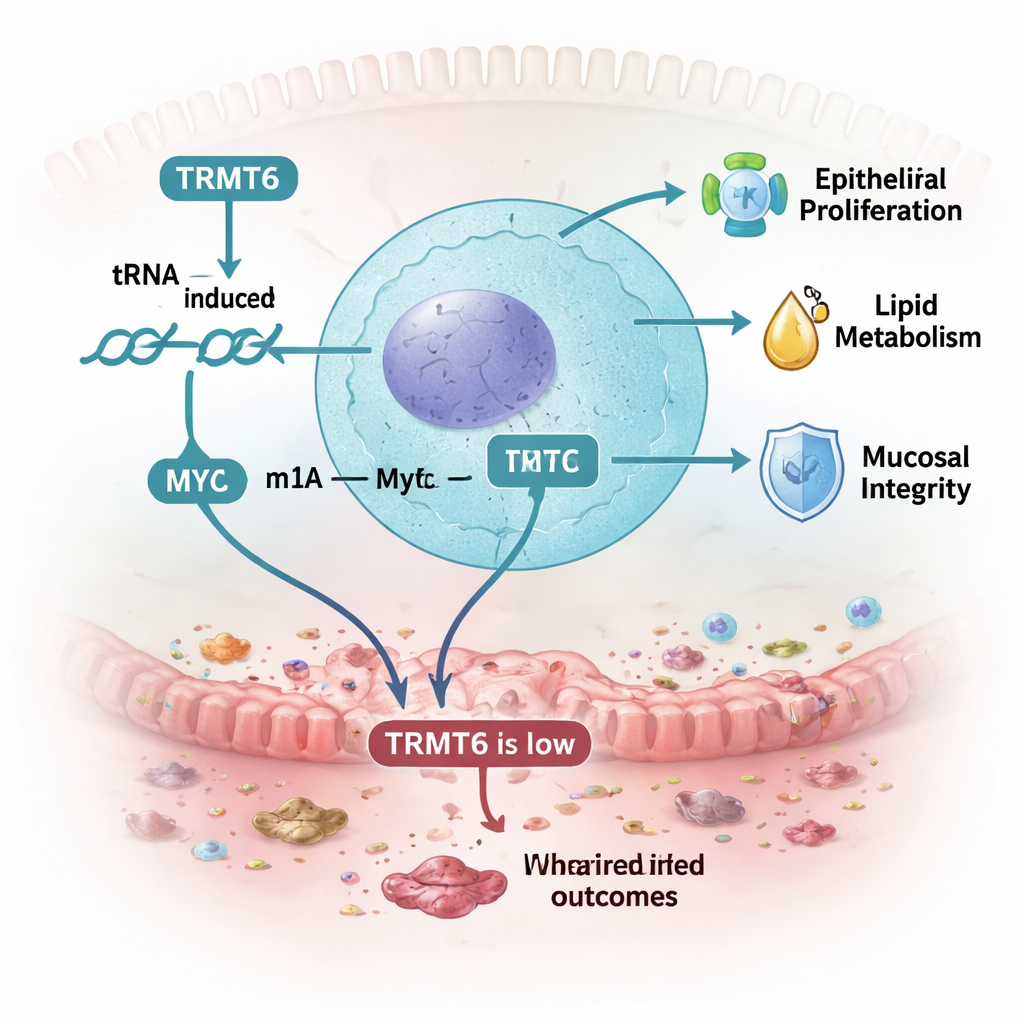
Un carrefour moléculaire reliant barrière, métabolisme et inflammation
Pris ensemble, ces résultats présentent TRMT6 comme un nœud central qui aide la muqueuse intestinale à faire face au stress. En ajustant finement une marque chimique spécifique sur l’ARN de transfert, TRMT6 soutient la production de MYC et d’autres protéines qui stimulent le renouvellement cellulaire, régulent le traitement des lipides et maintiennent l’étanchéité entre l’organisme et ses microbes résidents. Quand TRMT6 fait défaut ou est réduit, la paroi intestinale se répare plus lentement, absorbe moins bien les nutriments et crée des conditions favorisant une communauté microbienne plus nocive. Sous la pression supplémentaire d’un déclencheur inflammatoire, ces faiblesses se traduisent par une colite plus sévère chez la souris, ce qui reflète la diminution de TRMT6 observée dans les tissus humains atteints de MII.
Ce que cela pourrait signifier pour les traitements futurs
Pour les non‑spécialistes, le message clé est que les MII ne relèvent pas seulement d’un problème immunitaire ; elles résultent également d’échecs dans l’entretien quotidien des cellules intestinales. TRMT6 apparaît comme l’un des outils cellulaires qui maintiennent l’équilibre entre production protéique, métabolisme et réparation de la barrière. Bien que ces travaux soient encore à un stade préclinique précoce, ils suggèrent que stimuler doucement l’activité de TRMT6, ou imiter ses effets sur la traduction de l’ARN et la synthèse protéique, pourrait un jour contribuer à renforcer la muqueuse intestinale et à calmer l’inflammation chez les personnes atteintes de MII. Des études plus larges, dans d’autres modèles pathologiques et sur des échantillons de patients, seront nécessaires, mais ce travail pointe vers un angle nouveau et plus précis pour s’attaquer à l’inflammation intestinale chronique.
Citation: Zhang, X., Du, Y., Ye, Y. et al. TRMT6 mitigates susceptibility and progression of DSS-induced colitis multifacetedly via translational regulation. Sci Rep 16, 6809 (2026). https://doi.org/10.1038/s41598-026-37299-z
Mots-clés: maladie inflammatoire de l’intestin, barrière intestinale, modification de l’ARN, microbiote intestinal, métabolisme intestinal