Clear Sky Science · fr
Impact du microbiote Oligo‑MM12 défini sur la colonisation intestinale et la dissémination de Listeria monocytogenes
Pourquoi les microbes de votre intestin comptent
Beaucoup connaissent Listeria monocytogenes comme un germe alimentaire dangereux lié à des aliments prêts à consommer contaminés et à des maladies graves chez les personnes vulnérables. Ce qui est moins évident, c’est que la capacité de cette bactérie à s’implanter dans l’organisme dépend non seulement de notre système immunitaire, mais aussi de la communauté foisonnante de microbes déjà présents dans nos intestins. Cette étude utilise des modèles murins spécialement conçus et un « côlon artificiel » miniature pour poser une question simple mais importante : comment la complexité du microbiome intestinal influence‑t‑elle la capacité de Listeria à coloniser l’intestin et à se disséminer dans l’organisme ?
Le récit de deux quartiers microbiens
Pour répondre à cette question, les chercheurs ont comparé deux types de souris. Un groupe, appelé souris SPF, portait un mélange riche et naturel de bactéries intestinales semblable à celui trouvé chez de nombreux animaux de laboratoire. L’autre groupe, les souris Oligo‑MM12, hébergeait une communauté beaucoup plus simple composée de seulement 12 souches bactériennes bien caractérisées. Parce que chaque membre de cette communauté est connu et stable d’une génération à l’autre, les souris Oligo‑MM12 sont un outil puissant pour disséquer quelles bactéries aident à bloquer les envahisseurs et lesquelles peuvent laisser des lacunes dans nos défenses. En contrastant ces souris, l’équipe a pu tester en quoi un écosystème intestinal dense et divers diffère d’un système épuré et minimaliste lorsqu’il s’agit de faire face à un défi infectieux.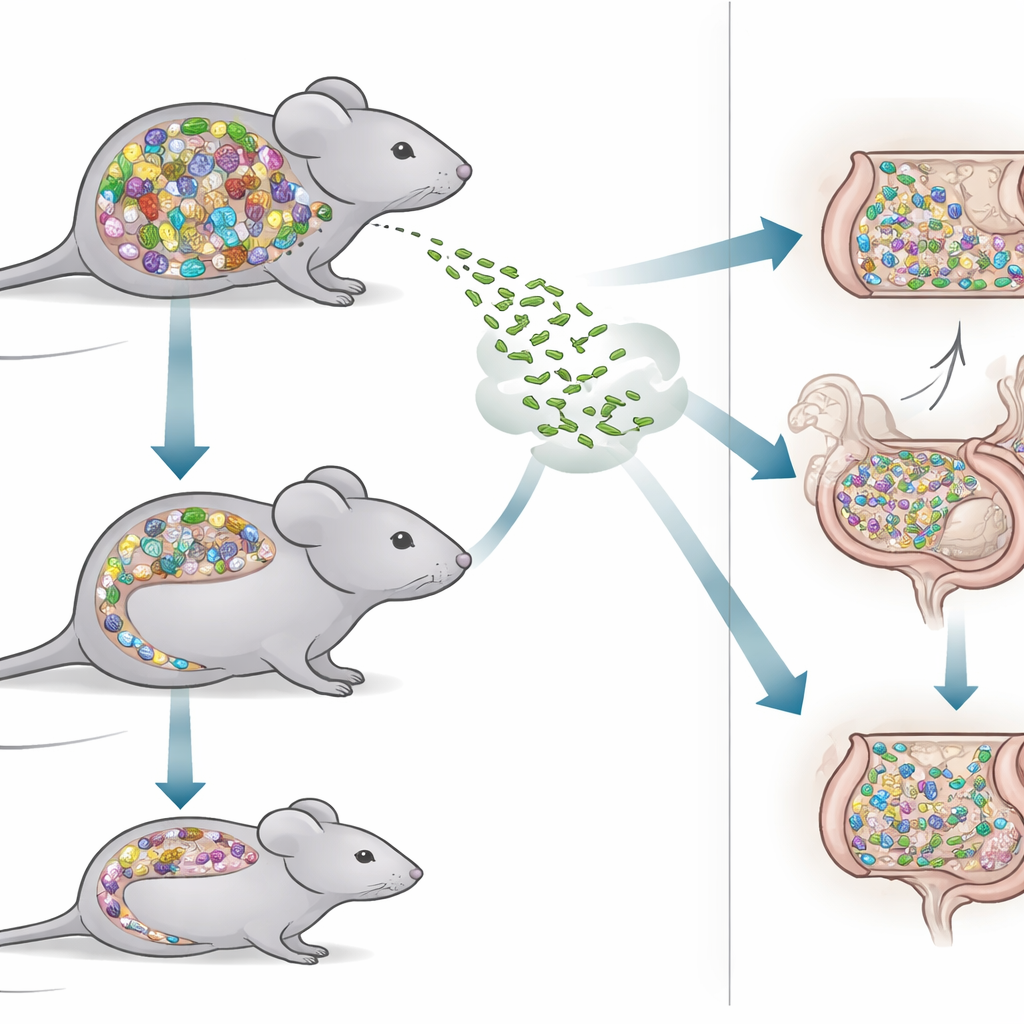
Suivre Listeria dans l’intestin et au‑delà
Les scientifiques ont infecté les deux types de souris avec la même dose orale de Listeria et ont suivi le nombre de bactéries présentes dans les fèces et les organes internes sur trois jours. De manière intéressante, la communauté plus simple Oligo‑MM12 semblait initialement mieux contenir Listeria : le premier jour après l’infection, ces souris excrétaient moins de cellules de Listeria dans leurs selles que les souris SPF. Cependant, cet avantage précoce s’est estompé. Au troisième jour, les souris Oligo‑MM12 excrétaient davantage de Listeria, tandis que les souris SPF avaient progressivement réduit les niveaux. Malgré ces différences claires dans l’intestin, les quantités de Listeria dans des organes internes tels que le foie, la rate et les ganglions lymphatiques étaient similaires entre les deux modèles murins, ce qui suggère que, une fois que Listeria atteint les tissus profonds, la complexité du microbiome joue un rôle moindre.
Simuler le côlon dans une boîte contrôlée
Pour séparer les effets des tissus hôtes et de l’immunité du comportement des microbes eux‑mêmes, l’équipe a également mené une expérience ex vivo en utilisant un dispositif appelé bioréacteur micro‑Matrix. Ils ont préparé des bouillies fécales à partir de chaque type de souris, les ont ajoutées à un milieu nutritif dans des puits scellés et anaérobies, et ont introduit Listeria dans certaines de ces cultures miniatures tout en laissant d’autres en témoins. Sur cinq jours, ils ont mesuré les nombres de Listeria et séquencé l’ADN bactérien pour suivre l’évolution des communautés. Dans ce côlon artificiel, Listeria a atteint des niveaux similaires qu’elle fasse face au microbiote SPF complexe ou à la communauté plus simple Oligo‑MM12, et sa présence n’a provoqué que des changements modestes dans la composition globale de la communauté. Ce contraste avec les animaux vivants souligne à quel point le système immunitaire, la muqueuse intestinale et les flux de bile et de mucus façonnent l’infection dans l’intestin réel.
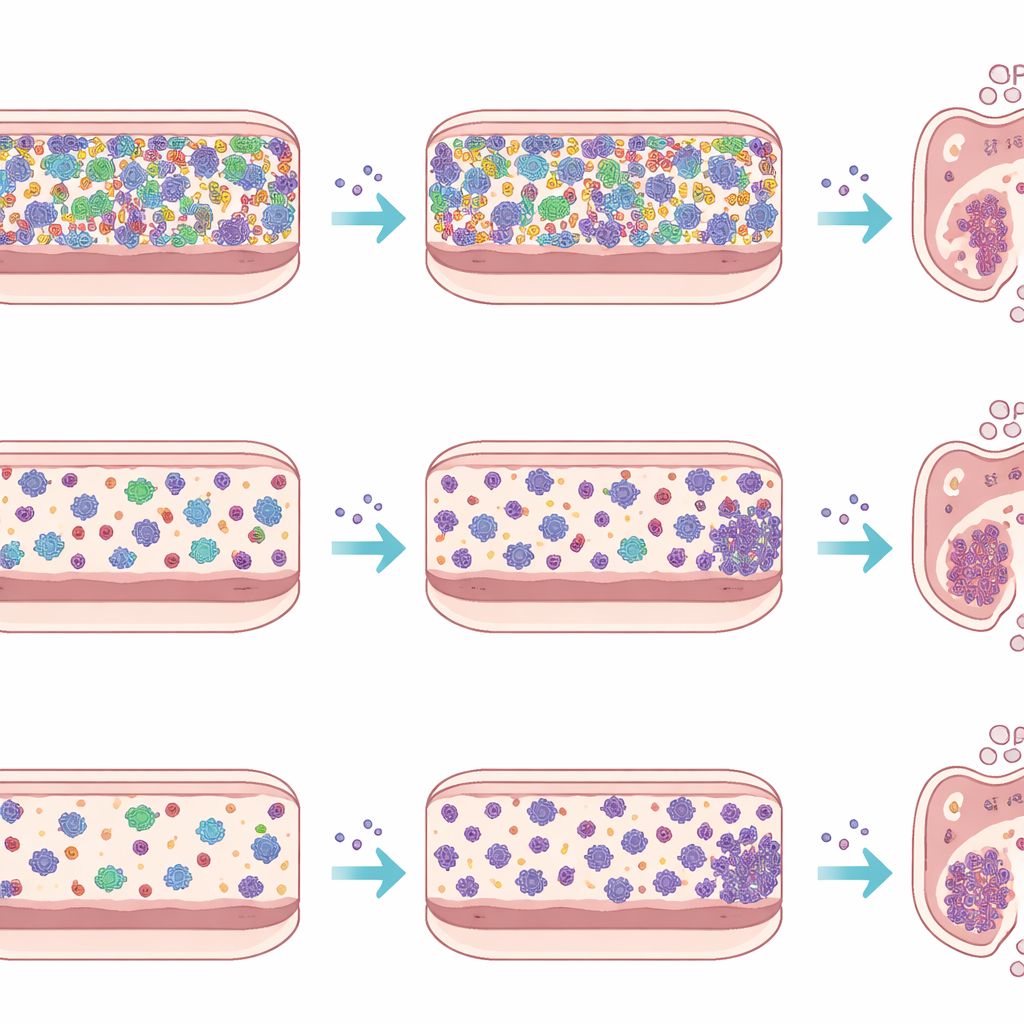
Principaux gagnants, perdants et spectateurs microbiens
En observant quels groupes bactériens augmentaient ou diminuaient pendant l’infection, l’étude identifie des candidats susceptibles d’influencer le succès de Listeria. Chez les souris Oligo‑MM12, les niveaux d’Akkermansia, une bactérie associée au mucus souvent liée à la santé intestinale, ont chuté le deuxième jour puis ont fortement rebondi au troisième jour. Chez les souris SPF, plusieurs genres connus pour produire des métabolites bénéfiques ou soutenir l’intégrité de la barrière, comme Blautia et Bacteroides, ont diminué durant l’infection, tandis que certaines bactéries de type Prevotella ont montré des hausses et des baisses complexes qui peuvent refléter une attaque directe par des composés antimicrobiens de Listeria. Ex vivo, ces schémas étaient pour l’essentiel atténués, renforçant l’idée que nombre des changements observés résultent d’interactions à trois entre le pathogène, les microbes résidents et l’environnement de l’hôte plutôt que d’une simple compétition microbe‑microbe.
Ce que cela signifie pour la protection des personnes
Pour les non‑spécialistes, le message central est que tous les microbiomes d’apparence saine ne protègent pas de la même manière contre les infections, et que « plus de diversité » n’est pas toujours meilleur à tout moment. La communauté simplifiée Oligo‑MM12 a fourni une forte résistance précoce à Listeria dans l’intestin, mais avec le temps le microbiome SPF plus complexe a mieux réussi à éliminer l’envahisseur. Ce travail montre que des modèles de microbiote de faible complexité soigneusement conçus, combinés à des systèmes ex vivo contrôlables, peuvent révéler quels groupes bactériens et facteurs environnementaux sont cruciaux pour bloquer des agents pathogènes alimentaires dangereux. En définitive, ces connaissances pourraient orienter des probiotiques ciblés ou des thérapies basées sur le microbiome pour renforcer les bons alliés microbiens au bon moment afin de prévenir les infections graves à Listeria chez les patients à risque.
Citation: Cazzaniga, M., Bra, K.K., Herzog, M.K.M. et al. Impact of the defined Oligo-MM12 microbiota on intestinal colonisation and dissemination of Listeria monocytogenes. Sci Rep 16, 8434 (2026). https://doi.org/10.1038/s41598-026-37294-4
Mots-clés: infection à Listeria, microbiote intestinal, résistance à la colonisation, modèle murin, probiotiques