Clear Sky Science · fr
L’amide de N-acétyl cystéine atténue le stress oxydatif et l’apoptose dans un modèle de rat d’ischémie‑reperfusion rénale
Pourquoi protéger nos reins est important
Chaque jour, nos reins filtrent silencieusement le sang, éliminent les déchets et maintiennent l’équilibre de l’organisme. Mais lors d’une chirurgie majeure, d’une infection sévère ou d’une transplantation, l’apport sanguin aux reins peut momentanément cesser puis reprendre, provoquant une vague de lésions connue sous le nom d’ischémie–reperfusion. Cette étude examine si une forme plus puissante d’un supplément antioxydant familier peut aider à protéger les reins contre ce type de stress — réduisant potentiellement le risque d’insuffisance rénale aiguë chez les patients soumis à des interventions à haut risque.
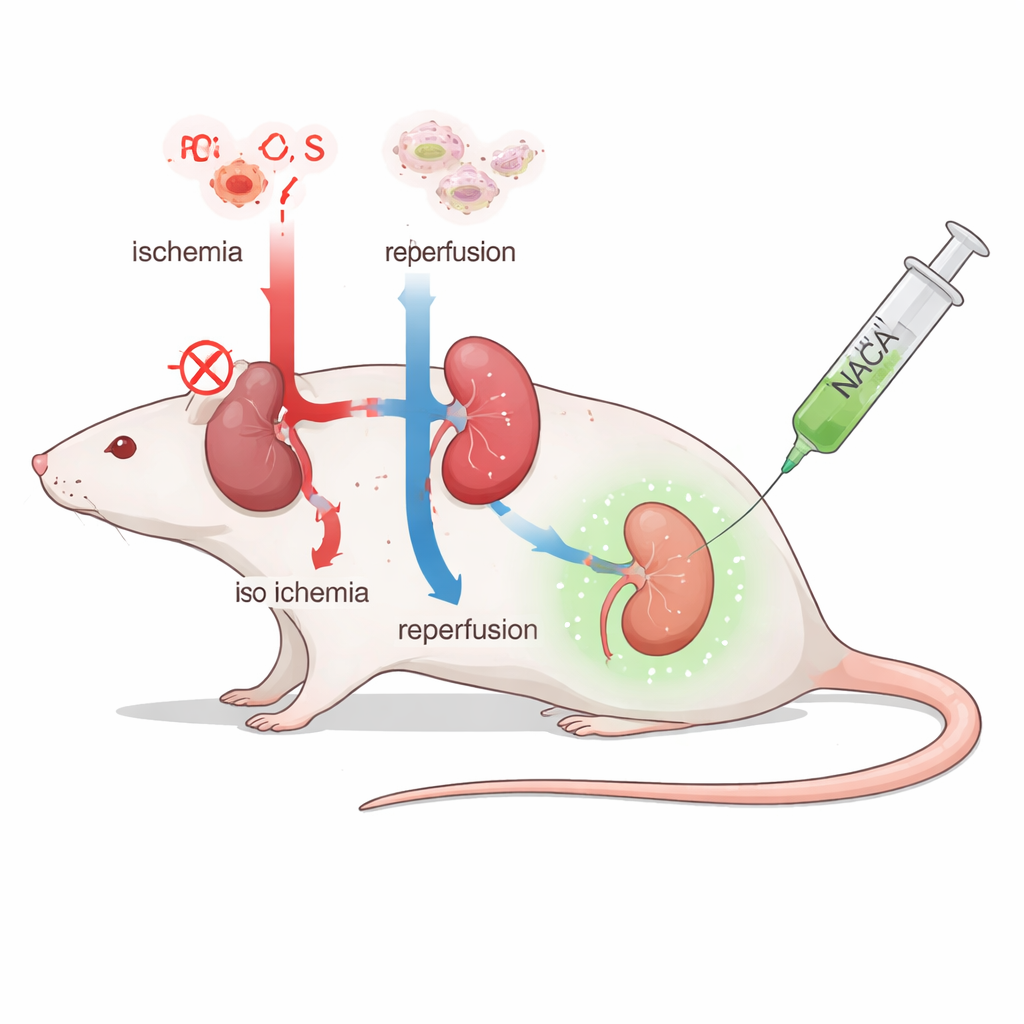
Une brève interruption aux conséquences durables
Lorsque l’apport sanguin aux reins est interrompu puis rétabli, le retour soudain d’oxygène peut paradoxalement endommager les tissus. Les cellules libèrent de grandes quantités d’espèces réactives de l’oxygène — des molécules très réactives qui détériorent les lipides, les protéines et l’ADN. Ce « stress oxydatif » déclenche inflammation et mort cellulaire programmée (apoptose), qui ensemble peuvent altérer sévèrement la fonction rénale. Les médecins disposent actuellement de moyens limités pour prévenir ce type de lésion ; les chercheurs utilisent donc des modèles animaux pour tester de nouvelles stratégies protectrices avant de les proposer aux humains.
Une variante plus performante d’un antioxydant courant
La N‑acétylcystéine (NAC) est un antioxydant bien connu utilisé en clinique, par exemple pour traiter les intoxications au paracétamol. Cependant, dans les études sur la protection rénale, ses bénéfices ont été variables, en partie parce qu’elle pénètre mal dans les cellules et les mitochondries. L’équipe de cette étude s’est intéressée à l’amide de N‑acétyl cystéine (NACA), une forme modifiée de la NAC plus liposoluble et capable de traverser plus facilement les membranes cellulaires. Ils ont posé deux questions principales chez le rat : la NACA réduit‑t‑elle les lésions rénales après ischémie–reperfusion, et le moment de l’administration — avant versus après l’arrêt du flux sanguin — influence‑t‑il son efficacité ?
Tester la NACA chez le rat
Les chercheurs ont utilisé quatre groupes de rats. Un groupe servait de témoin, tandis qu’un second était soumis à une ischémie–reperfusion rénale sans traitement. Deux groupes supplémentaires ont reçu la NACA à la même dose : l’un a obtenu le médicament une demi‑heure avant l’arrêt du flux sanguin, l’autre l’a reçu juste après la période ischémique, juste avant la reperfusion. Les scientifiques ont ensuite mesuré des marqueurs sanguins de la fonction rénale, des signes chimiques de stress oxydatif dans le tissu rénal, des lésions microscopiques des structures rénales et les niveaux d’une protéine clé de la mort cellulaire, la caspase‑3. Cette combinaison de tests leur a permis d’évaluer non seulement l’apparence générale des reins, mais aussi si les voies centrales de la lésion étaient atténuées.
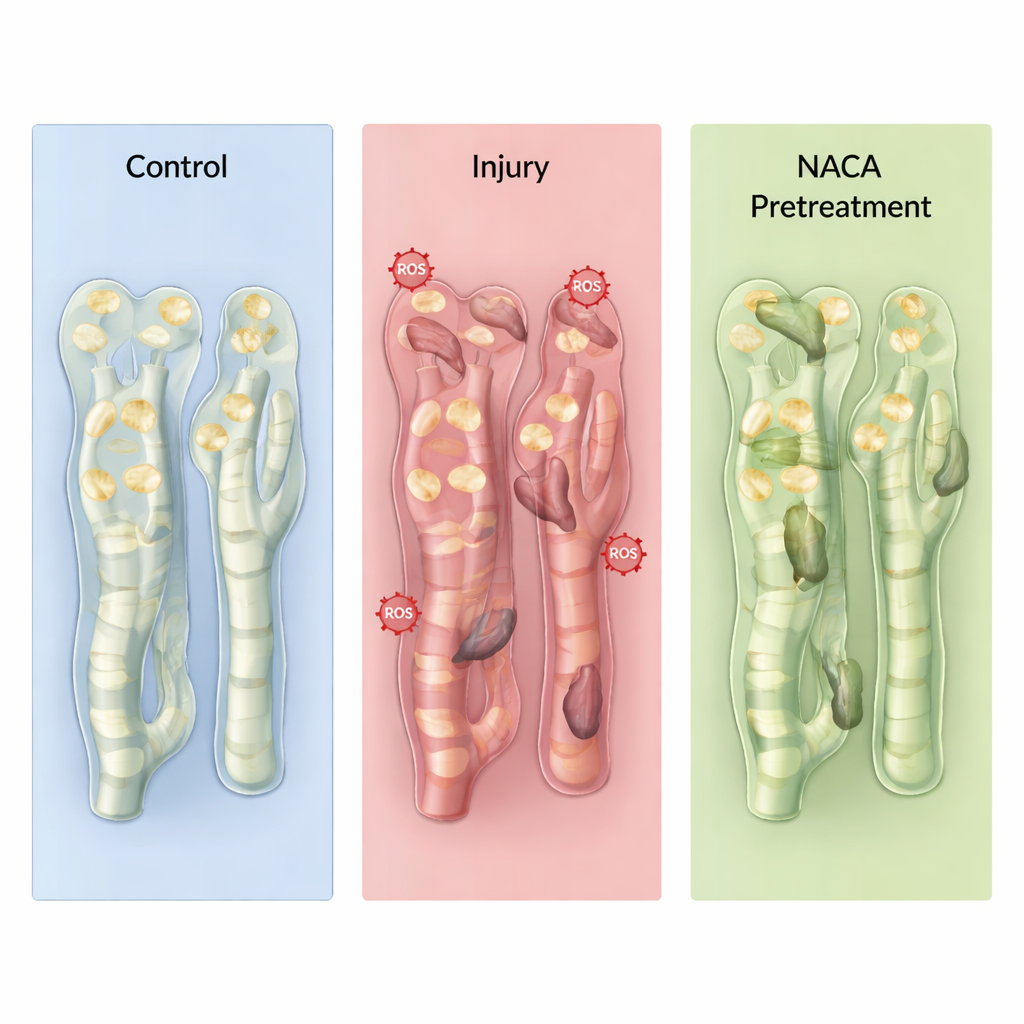
Protection partielle — et pourquoi le timing importe
Comme prévu, les rats soumis à l’ischémie–reperfusion sans NACA présentaient des signes évidents d’insuffisance rénale aiguë : les déchets tels que l’urée et la créatinine augmentaient, les marqueurs chimiques de l’atteinte lipidique étaient accrus, et l’examen microscopique révélait des tubules dilatés, des « cylindres » de débris et un tissu inflammatoire. Lorsque la NACA était administrée avant l’ischémie, plusieurs de ces altérations étaient atténuées. Les marqueurs de dommage lipidique diminuaient, les principales enzymes antioxydantes se rapprochaient de la normale, l’infiltration de cellules inflammatoires était réduite et l’activité de la caspase‑3 — indicatrice d’entrée des cellules dans la mort programmée — chutait notablement. Administrer la NACA seulement après la période ischémique apportait moins d’avantage ; au moment de son arrivée, de nombreuses réactions dommageables avaient déjà été déclenchées, si bien que l’apoptose et l’inflammation n’étaient pas réduites dans la même mesure.
Ce que cela pourrait signifier pour les patients
L’étude montre que la NACA ne peut pas complètement prévenir les lésions rénales, mais qu’elle offre une « rinoprotection » partielle significative en réduisant le stress oxydatif et en ralentissant la mort cellulaire précoce, notamment lorsqu’elle est présente dans le tissu avant le rétablissement du flux sanguin. Pour le grand public, cela suggère qu’un antioxydant mieux conçu, administré au bon moment, pourrait un jour aider à protéger les reins vulnérables lors d’événements tels que la transplantation ou les chirurgies complexes. Les travaux restent au stade animal et une seule dose et fenêtre temporelle ont été testées, si bien qu’un bénéfice chez l’humain n’est pas encore prouvé. Néanmoins, ces résultats renforcent l’idée qu’anticiper le stress rénal et pré‑armer l’organe avec des antioxydants ciblés comme la NACA pourrait devenir une composante importante des stratégies futures pour réduire le risque d’insuffisance rénale aiguë.
Citation: Ozhan, O., Ekici, C., Ates, B. et al. N-acetyl cysteine amide mitigates oxidative stress and apoptosis in a rat model of renal ischemia-reperfusion injury. Sci Rep 16, 6323 (2026). https://doi.org/10.1038/s41598-026-37274-8
Mots-clés: insuffisance rénale aiguë, stress oxydatif, ischémie reperfusion, thérapie antioxydante, amide de N-acétyl cystéine