Clear Sky Science · fr
Analyse intégrée des régulateurs globaux et des gènes d’efflux associés à l’inversion de la résistance aux antimicrobiens chez Klebsiella pneumoniae multirésistante
Pourquoi ces germes hospitaliers sont si difficiles à tuer
Dans les hôpitaux du monde entier, certaines souches de la bactérie Klebsiella pneumoniae sont devenues notoirement difficiles à traiter. Elles résistent à plusieurs antibiotiques qui fonctionnaient autrefois de façon fiable, transformant des infections courantes en urgences potentiellement mortelles. Cette étude explore le fonctionnement interne de ces microbes pour comprendre un stratagème important : de minuscules pompes qui expulsent les antibiotiques hors de la cellule, et les interrupteurs génétiques qui semblent augmenter ou diminuer l’activité de ces pompes.
Super‑bactéries et leurs sorties moléculaires
La Klebsiella pneumoniae multirésistante est désormais rencontrée dans de nombreux hôpitaux, y compris le centre médical irakien où cette recherche a été réalisée. Ces bactéries peuvent survivre à plusieurs grandes familles d’antibiotiques à la fois, telles que les fluoroquinolones, les aminoglycosides et les céphalosporines de troisième génération. L’un des moyens qu’elles utilisent consiste à installer de puissantes « pompes d’efflux » dans leur enveloppe cellulaire. Parmi les plus importantes figure un système appelé AcrAB‑TolC, qui traverse les membranes bactériennes et fonctionne comme une minuscule pompe de relevage, saisissant les molécules d’antibiotique à l’intérieur de la cellule et les rejetant à l’extérieur avant que les médicaments ne puissent causer des dégâts sérieux. Lorsque ces pompes sont très actives, la concentration d’antibiotique à l’intérieur de la bactérie n’atteint jamais un niveau létal.
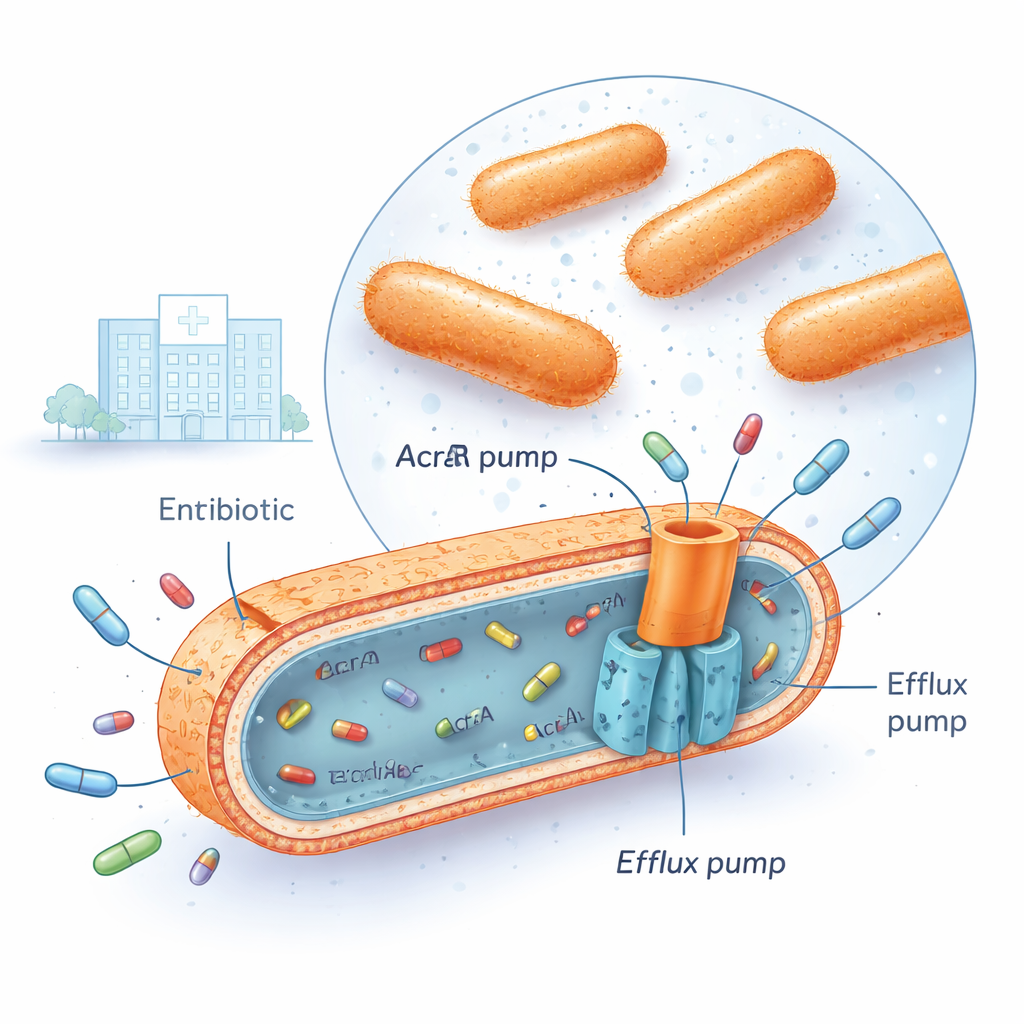
Interrupteurs génétiques associés à la suractivité des pompes
Les chercheurs ont collecté 30 isolats cliniques multirésistants de Klebsiella pneumoniae et les ont comparés à 10 isolats sensibles aux antibiotiques ainsi qu’à une souche de référence standard. À l’aide d’une technique appelée PCR quantitative en temps réel, ils ont mesuré le niveau d’expression de certains gènes. Ils se sont concentrés sur trois « régulateurs globaux » — des gènes nommés marA, soxS et rob — ainsi que sur les trois composants de la pompe AcrAB‑TolC (acrA, acrB et tolC). Dans les souches résistantes, deux régulateurs, marA et soxS, étaient généralement surexprimés d’environ quatre à cinq fois par rapport aux bactéries sensibles, tandis que acrB, un composant central de la pompe, était stimulé d’à près de huit fois. L’analyse statistique a montré que lorsque les niveaux de marA et de soxS étaient élevés, les niveaux de acrB l’étaient généralement aussi, et ces souches supportaient des doses beaucoup plus élevées d’antibiotiques fluoroquinolones comme la ciprofloxacine. Un troisième régulateur, rob, variait peu et n’était pas corrélé à l’activité de la pompe, ce qui suggère qu’il joue un rôle moindre dans les conditions testées.
Désactiver les pompes pour affaiblir la résistance
Montrer que les gènes de la pompe et des régulateurs sont actifs en même temps est suggestif mais pas suffisant pour prouver qu’ils causent réellement la résistance. Pour tester si les pompes avaient une importance fonctionnelle, l’équipe a utilisé un outil chimique appelé PAβN. Ce composé n’est pas employé comme médicament chez les patients, mais au laboratoire il peut obstruer des pompes de type AcrAB‑TolC et les empêcher d’expulser les antibiotiques. Les scientifiques ont choisi dix isolats résistants présentant des niveaux particulièrement élevés du gène acrB et ont mesuré la quantité de ciprofloxacine nécessaire pour arrêter leur croissance, avec et sans PAβN. Dans huit de ces dix souches, le blocage de la pompe a réduit au moins par quatre la dose de ciprofloxacine requise, et parfois jusqu’à seize fois. Cette diminution montre que, chez nombre de ces super‑bactéries, les pompes d’efflux actives constituent effectivement une cause majeure de leur tolérance à des doses élevées d’antibiotiques.
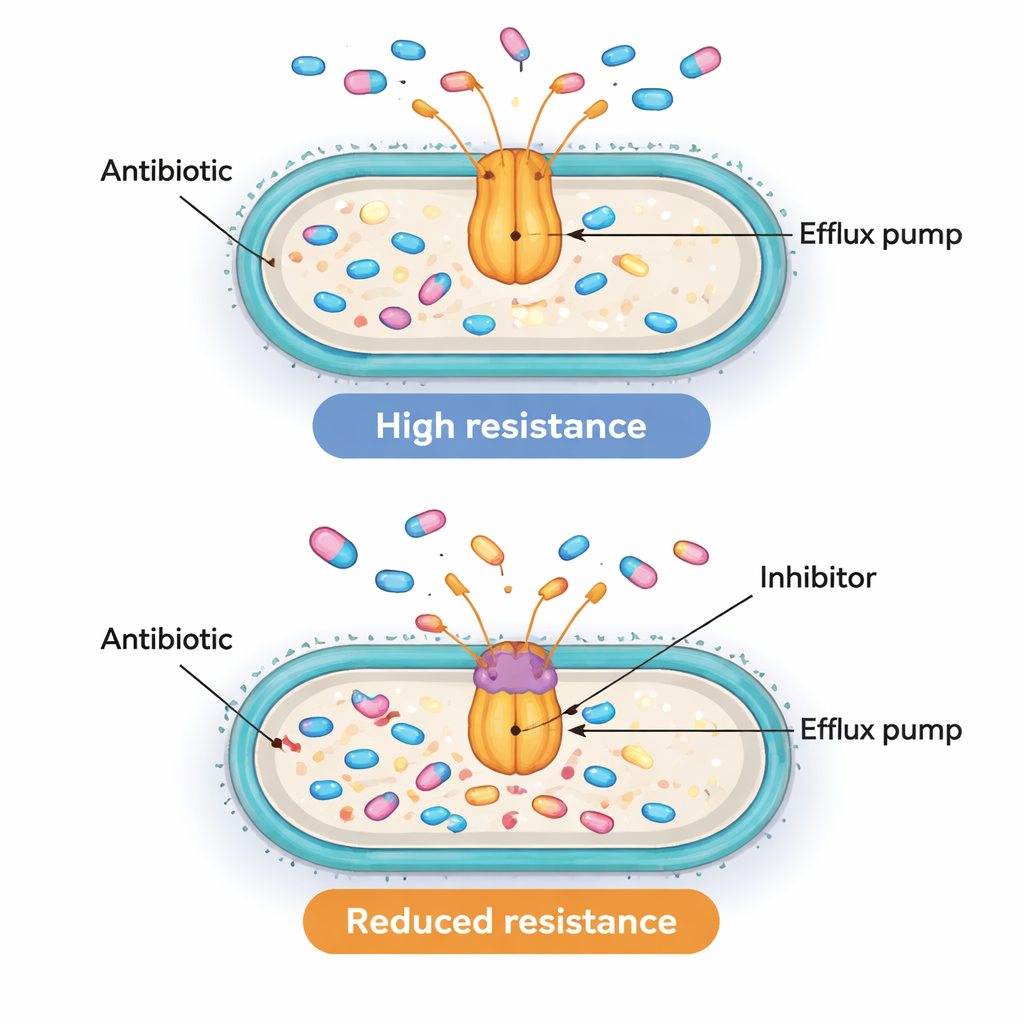
Un casse‑tête complexe de la résistance avec des cibles prometteuses
Toutes les souches ne se comportaient pas de la même manière. Certaines bactéries avec une forte expression des gènes de pompe ne retrouvaient que partiellement leur sensibilité lorsque les pompes étaient bloquées, ce qui implique que d’autres voies de résistance — telles que des modifications de la cible de l’antibiotique à l’intérieur de la cellule, la production d’enzymes qui inactivent les médicaments, ou des pompes alternatives — contribuent aussi. La gentamicine, un antibiotique aminoglycoside, par exemple, restait en grande partie inchangée par les profils observés pour marA/soxS et AcrAB‑TolC, soulignant que la multirésistance est généralement constituée de plusieurs défenses qui se chevauchent plutôt que d’un mécanisme unique.
Ce que cela signifie pour les traitements futurs
Pour les non‑spécialistes, le message clé est que certaines bactéries hospitalières peuvent survivre aux antibiotiques non seulement en bloquant ou en dégradant les médicaments, mais en les expulsant activement. Cette étude relie une activité accrue de deux « interrupteurs » génétiques, MarA et SoxS, à des pompes d’efflux plus actives et à une résistance plus forte à une classe d’antibiotiques largement utilisée. Lorsque les pompes sont expérimentalement obstruées, nombre de ces bactéries redeviennent au moins partiellement sensibles. Bien que le travail ne prouve pas encore précisément comment ces régulateurs contrôlent les pompes, il met en évidence à la fois les régulateurs et les pompes comme des cibles intéressantes. À long terme, associer des antibiotiques classiques à des inhibiteurs de pompes sûrs — ou à des médicaments qui diminuent l’activité de ces régulateurs globaux — pourrait contribuer à restaurer l’efficacité des traitements existants contre des infections multirésistantes autrement redoutables.
Citation: Obaid, A.J., Alkawaz, A.J. & Naser, M.S. Integrated analysis of global regulators and efflux genes associated with antimicrobial resistance reversal in multidrug resistant Klebsiella pneumoniae. Sci Rep 16, 7435 (2026). https://doi.org/10.1038/s41598-026-37272-w
Mots-clés: résistance aux antibiotiques, pompes d’efflux, Klebsiella pneumoniae, fluoroquinolones, inversion de la résistance