Clear Sky Science · fr
La diminution de l’expression de la désubiquitinase USP10 corrèle avec l’apoptose neuronale dans la myélopathie associée au HTLV-1
Pourquoi cela compte pour les personnes vivant avec des maladies nerveuses d’origine virale
Certains virus n’entraînent pas seulement des infections brèves ; ils peuvent silencieusement endommager le système nerveux pendant de nombreuses années. Le virus T des lymphocytes T de type 1 (HTLV‑1) en est un exemple et peut provoquer une affection chronique de la moelle épinière appelée myélopathie associée au HTLV‑1 (HAM). Les personnes atteintes de HAM perdent progressivement de la force et le contrôle de leurs jambes, ainsi que des fonctions vésicales et sensitives. Cette étude pose une question simple mais cruciale : pourquoi les cellules nerveuses de la moelle épinière meurent‑elles dans cette condition, et une seule molécule protectrice pourrait‑elle aider à expliquer qui s’en sort mieux ou pire ?
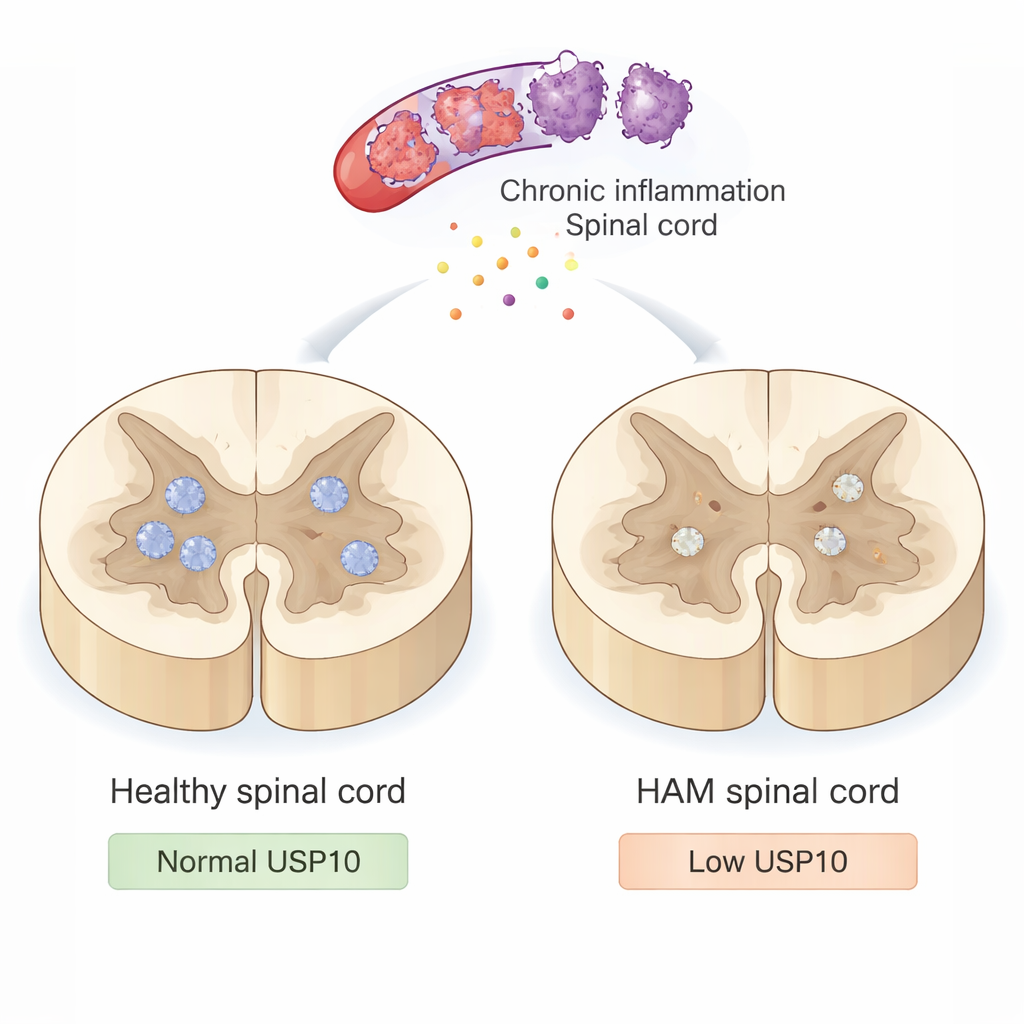
Une attaque lente contre la moelle épinière
La HAM n’est pas causée par une infection directe des neurones par le virus. Au contraire, le HTLV‑1 infecte des cellules immunitaires qui envahissent la moelle épinière et déclenchent une inflammation prolongée. Ces cellules immunitaires hyperactives libèrent des substances toxiques et des signaux inflammatoires qui, bien qu’ils visent à contrôler l’infection, blessent aussi les neurones voisins et leur myéline isolante. Avec le temps, cette agression sourde conduit à des jambes raides et faibles et à des difficultés à marcher. Pourtant, les médecins ne comprennent pas entièrement pourquoi certains neurones succombent à cet environnement inflammatoire tandis que d’autres survivent pendant des décennies.
Une enzyme de « nettoyage » cellulaire suspectée
Les chercheurs se sont intéressés à une protéine appelée USP10, une enzyme qui aide à réguler le système de contrôle de la qualité des protéines de la cellule et qui limite le stress cellulaire et la mort cellulaire programmée (apoptose). USP10 est active dans de nombreux tissus, y compris le cerveau et la moelle épinière, et des travaux antérieurs dans la maladie de Parkinson, l’accident vasculaire cérébral et d’autres affections suggèrent qu’elle aide les neurones à résister aux dommages oxydatifs et inflammatoires. En utilisant des échantillons de moelle épinière provenant de huit personnes décédées avec une HAM et de deux témoins neurologiquement sains, l’équipe a utilisé des techniques de coloration pour voir où USP10 était présente et quelle était son intensité d’expression dans les cellules nerveuses.
Moins d’USP10, plus de neurones en train de mourir
Dans les moelles épinières saines, USP10 était fortement visible dans de nombreux neurones. Dans la plupart des cas de HAM toutefois, la coloration pour USP10 dans les neurones était nettement réduite, et chez un patient elle était presque absente. Les scientifiques ont ensuite recherché des marques d’apoptose avec deux méthodes : un test TUNEL qui détecte l’ADN fragmenté et une coloration pour la caspase‑3 active, une protéine impliquée tôt dans la mort cellulaire. Chez les témoins, quasiment aucun neurone n’a montré ces signaux de mort. En revanche, chez les patients HAM, une large fraction des neurones était positive au TUNEL et beaucoup présentaient une caspase‑3 active. De manière importante, les échantillons avec une expression plus faible d’USP10 avaient tendance à comporter plus de neurones apoptotiques et moins de neurones survivants marqués par NeuN, un marqueur neuronal standard. Un patient notable atteint de HAM qui marchait encore avec une canne après 22 ans montrait une forte expression d’USP10 et un nombre de neurones relativement préservé, ce qui suggère que des niveaux plus élevés d’USP10 pourraient aider à protéger contre un handicap sévère.
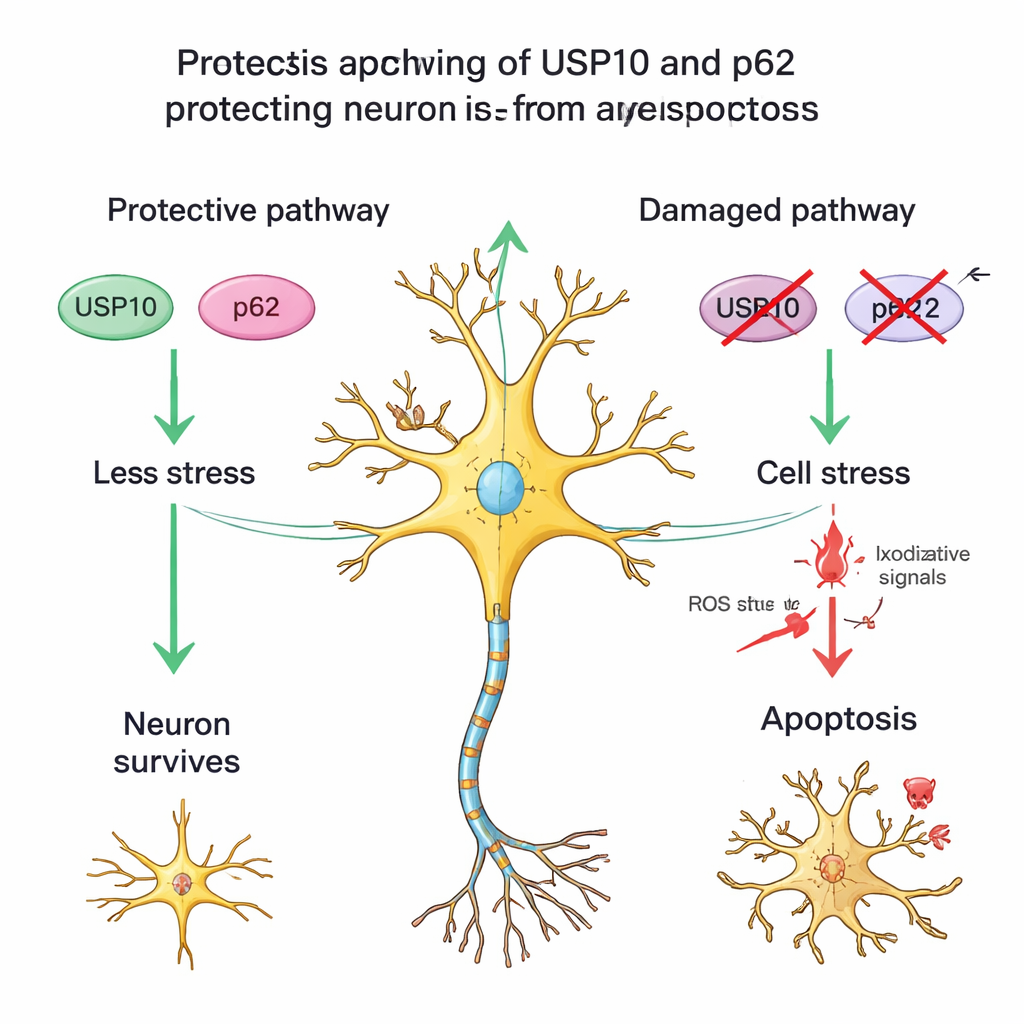
Une protéine partenaire et des cellules stressées mais survivantes
L’équipe a également examiné une autre protéine, p62, qui travaille avec USP10 dans la gestion des protéines endommagées et la régulation des voies de stress et de survie. Dans les moelles épinières saines, la coloration pour p62 était modérée ; parmi les patients HAM, ceux présentant une faible USP10 avaient souvent aussi une coloration p62 plus faible et moins de neurones survivants. Ce schéma soutient l’idée d’un partenariat USP10–p62 aidant les neurones à résister à l’inflammation chronique. Les chercheurs ont en outre remarqué de nombreux neurones dans les tissus HAM qui avaient la morphologie typique des cellules nerveuses mais avaient perdu la coloration NeuN, un signe observé dans d’autres lésions cérébrales lorsque les neurones sont en état de stress sévère mais pas encore complètement morts. Cela suggère que dans la HAM, certains neurones sont non seulement perdus définitivement mais d’autres restent dans un état endommagé et vulnérable, potentiellement parce que les défenses liées à USP10 sont affaiblies.
Ce que cela pourrait signifier pour le diagnostic et le traitement futurs
Cette étude ne prouve pas que la perte d’USP10 cause directement la mort neuronale, car elle repose sur un petit nombre d’échantillons d’autopsie et ne peut pas suivre les changements au fil du temps. Néanmoins, les liens constants entre faible USP10, réduction de p62, augmentation des signes d’apoptose et diminution des neurones survivants pointent vers une voie commune qui pourrait relier l’inflammation chronique à la dégénérescence neuronale lente dans la HAM. Pour les patients, cela ouvre une possibilité encourageante : mesurer ou renforcer les voies liées à USP10 dans la moelle épinière — ou potentiellement dans des échantillons plus accessibles comme le liquide cérébro‑spinal — pourrait un jour aider à identifier ceux à risque d’évolution rapide, orienter la surveillance ou inspirer de nouveaux traitements conçus pour renforcer les systèmes de protection contre le stress de la cellule dans les maladies neuroinflammatoires induites par des virus.
Citation: Arishima, S., Takahashi, M., Dozono, M. et al. Downregulation of the deubiquitinating enzyme USP10 correlates with neuronal apoptosis in HTLV-1-associated myelopathy. Sci Rep 16, 6062 (2026). https://doi.org/10.1038/s41598-026-37271-x
Mots-clés: Myélopathie associée au HTLV-1, neuroinflammation, apoptose neuronale, USP10, dégénérescence de la moelle épinière