Clear Sky Science · fr
Activité antibactérienne et cytotoxicité des ciments à base de silicate tricalcique avec différents additifs antibactériens
Pourquoi cela compte pour votre prochain plombage
Lorsque vous avez une carie profonde, les dentistes cherchent désormais à préserver autant que possible la dent naturelle plutôt que d’enlever tout le tissu. Cela signifie souvent qu’une fine couche de dentine ramollie, contenant des bactéries, est laissée sous le plombage. Cette étude pose une question simple mais cruciale : peut‑on améliorer un ciment largement utilisé pour la réparation des dents afin qu’il élimine discrètement les germes résiduels sans nuire aux cellules vivantes à l’intérieur de la dent ?
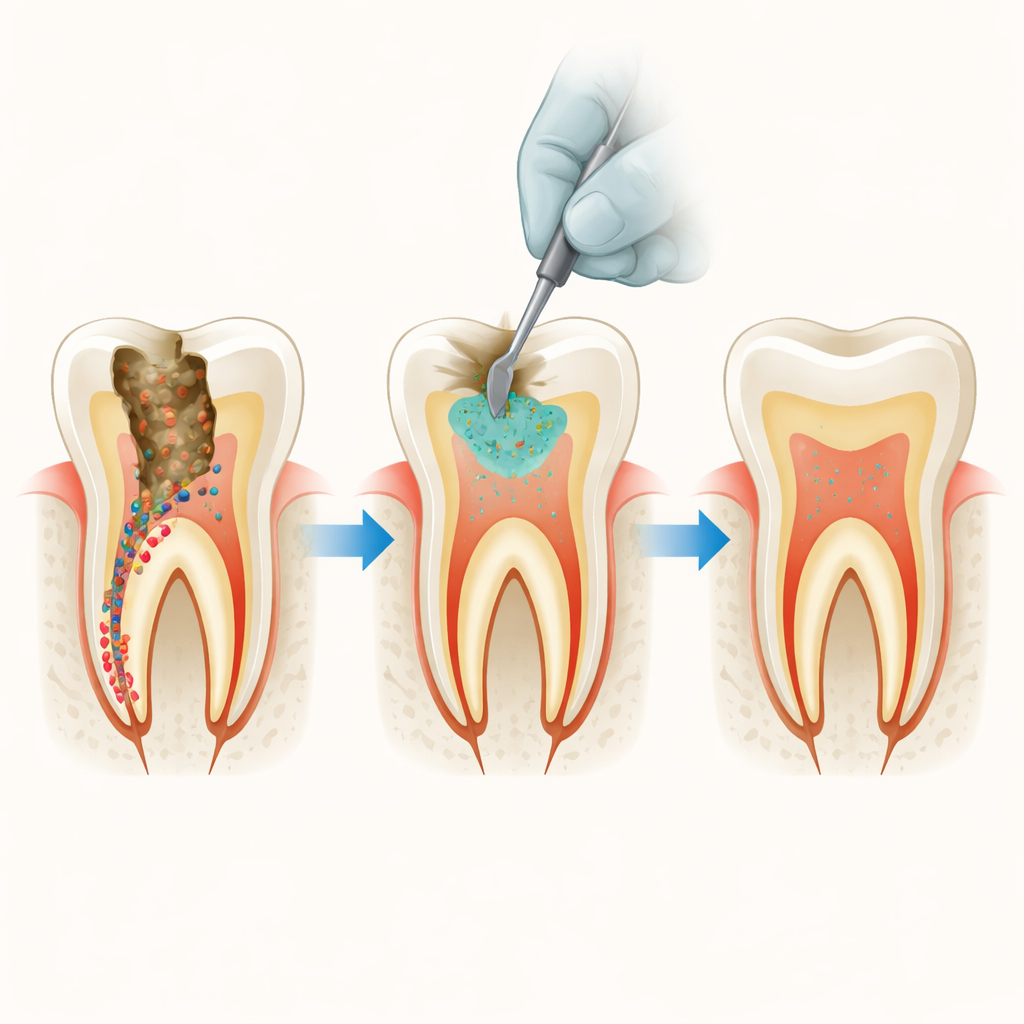
Caries profondes et germes cachés
Les techniques modernes de « forage minimal » visent à éviter d’exposer le cœur mou de la dent, ou pulpe, en laissant une dentine qui peut encore se reminéraliser. L’inconvénient est que certaines bactéries cariogènes, comme Streptococcus mutans et des espèces de Lactobacillus, peuvent subsister dans cette couche. Avec le temps, ces bactéries peuvent provoquer une nouvelle dégradation sous un plombage apparemment sain. Les ciments à base de silicate tricalcique sont populaires pour sceller les caries profondes parce qu’ils favorisent la reformations minérale et créent une barrière étanche, mais pris seuls ils ne sont pas très efficaces pour éliminer les bactéries.
Transformer un ciment courant en agent anti‑germes
Les chercheurs ont pris ce ciment connu et y ont incorporé cinq additifs antibactériens différents à diverses concentrations. Deux étaient des composés organiques fréquemment trouvés dans les désinfectants (chlorure de benzalkonium et cétrimide), et trois étaient des substances inorganiques utilisées dans des produits ou matériaux dentaires (dioxyde de titane, oxyde de zinc et fluorure stanneux). Ils ont pressé ces mélanges en disques minuscules et les ont placés sur des boîtes ensemencées de cinq types de bactéries associées aux caries et aux infections buccales. En mesurant les zones claires autour de chaque disque où les bactéries ne pouvaient pas croître, ils ont pu évaluer la puissance de chaque recette pour contenir les germes.
Trouver le juste milieu entre tuer les germes et préserver les cellules
Parce qu’un matériau qui tue les bactéries mais empoisonne aussi les cellules dentaires serait inutilisable en bouche, l’équipe a aussi testé comment les additifs les plus prometteurs affectaient des cellules vivantes. Ils ont exposé indirectement deux types de cellules humaines — des fibroblastes, cellules de soutien courantes, et des cellules souches pulpares dentaires, qui participent à la réparation des tissus dentaires — aux ciments. Un test basé sur un changement de couleur a mesuré le nombre de cellules restées actives, et des colorants fluorescents spécifiques ont montré les cellules vivantes (vert) et mortes (rouge) au microscope. Ce montage imitait la situation réelle d’une carie profonde, où le ciment est séparé de la pulpe par une fine couche de dentine et libère des substances qui diffusent vers les cellules.
Ce qui a le mieux fonctionné et ce qui était trop agressif
Les résultats ont montré que le type et la quantité d’additif comptaient énormément. Le chlorure de benzalkonium a fourni l’effet antibactérien le plus fort et le plus large, produisant de grandes zones sans germes contre toutes les espèces testées, en particulier les souches de Lactobacillus souvent rencontrées dans les caries profondes. Le cétrimide a également apporté un effet, mais nécessitait généralement des concentrations plus élevées pour égaler les performances du benzalkonium. Les trois agents inorganiques n’ont amélioré l’effet antibactérien du ciment qu’aux doses les plus élevées testées, et encore principalement contre certaines bactéries comme S. mutans et Actinomyces. Côté sécurité, le ciment de base seul était bien toléré par les deux types cellulaires et semblait même soutenir la santé des fibroblastes. L’ajout de chlorure de benzalkonium restait inoffensif pour les fibroblastes jusqu’à environ 1 %, devenait légèrement dommageable à 2–4 % et clairement plus nocif à 7 %. Les cellules souches pulpares étaient globalement plus sensibles : le chlorure de benzalkonium et le cétrimide ont réduit leur survie, le cétrimide devenant modérément toxique à partir de 2 %.
Ce que cela pourrait signifier pour les soins dentaires futurs
En regroupant ces résultats, l’étude met en évidence une recette particulièrement prometteuse : un ciment à base de silicate tricalcique contenant 1 % de chlorure de benzalkonium. À ce niveau, le matériau supprimait fortement les bactéries nocives tout en gardant les fibroblastes pleinement vivants et les cellules souches pulpares majoritairement viables. Concrètement, cela laisse entrevoir que les plombages profonds futurs pourraient être fabriqués à partir d’un ciment qui combat discrètement les germes résiduels sous la surface tout en restant suffisamment doux pour le tissu vivant à l’intérieur de la dent. D’autres travaux sont nécessaires — notamment dans des conditions buccales complexes et réelles — mais cette formule équilibrée pourrait aider les dentistes à mieux protéger les dents traitées par des techniques peu invasives.
Citation: Banon, R., Martens, L., De Coster, P. et al. Antibacterial activity and cytotoxicity of tricalcium silicate-based cements with different antibacterial additives. Sci Rep 16, 8349 (2026). https://doi.org/10.1038/s41598-026-37269-5
Mots-clés: caries dentaires profondes, ciment dentaire antibactérien, silicate tricalcique, chlorure de benzalkonium, biocompatibilité des cellules pulpares