Clear Sky Science · fr
Imagerie des biomolécules intercellulaires à l’aide d’indicateurs protéiques fluorescents avec ancrages lipid-PEG
Observer la communication cellulaire en temps réel
Notre cerveau et notre corps reposent sur une conversation chimique constante entre les cellules. Ions et neurotransmetteurs véhiculent des messages à travers de minuscules interstices, mais ces signaux rapides et éphémères sont difficiles à visualiser sans les perturber. Cette étude présente une méthode simple pour « peindre » des cellules vivantes avec des capteurs lumineux qui se fixent à leur surface externe, permettant aux scientifiques d’observer ces messages — en particulier les ions potassium et le neurotransmetteur glutamate — en direct et avec précision. 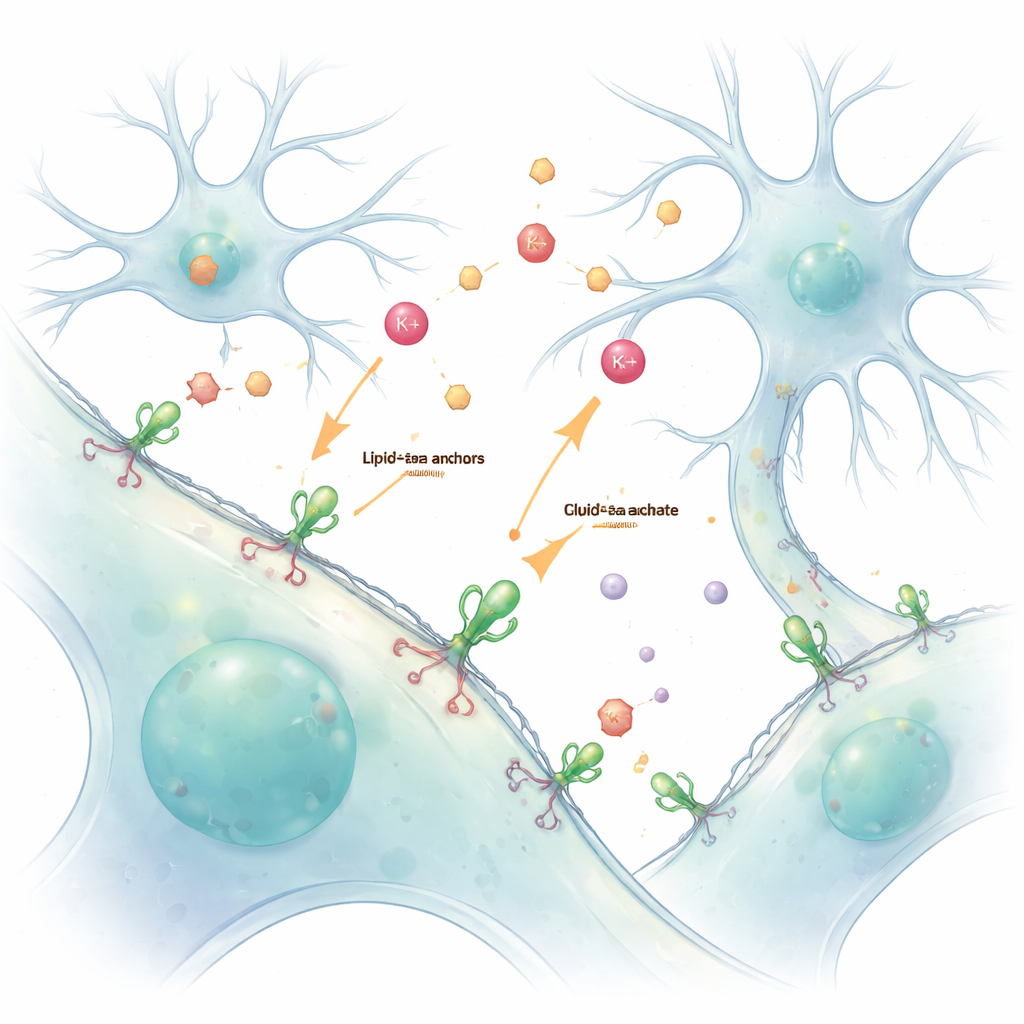
Une nouvelle façon d’étiqueter la surface cellulaire
Traditionnellement, les chercheurs conçoivent des cellules pour qu’elles produisent des capteurs protéiques fluorescents à partir de leur propre ADN. Bien que puissante, cette approche génétique place souvent les capteurs à l’intérieur de la cellule, rendant difficile la distinction entre ce qui se passe à l’intérieur et à l’extérieur. Les auteurs ont résolu ce problème en utilisant une poignée chimique appelée ancrage lipid–PEG. Une extrémité de cette molécule s’insère dans la membrane externe, tandis que l’autre est liée chimiquement à un capteur protéique fluorescent. Lorsque ces capteurs préparés sont simplement ajoutés à des cellules vivantes, ils enrobent spontanément la surface externe, formant une couche lumineuse et stable qui rend compte de ce qui se passe dans le fluide environnant.
Convertir le potassium et le glutamate en lumière
L’équipe a adapté deux indicateurs fluorescents existants : GINKO2, qui répond aux ions potassium, et R-iGluSnFR1, qui répond au glutamate. Ils ont purifié ces protéines à partir de bactéries puis y ont attaché les ancrages lipid–PEG. Dans des cellules humaines en culture, le capteur de potassium ancré dessinait un contour régulier le long de la surface cellulaire et s’éclairait chaque fois que le potassium extracellulaire augmentait, puis s’assombrissait lorsque les niveaux retombaient. Il est important de noter que ses propriétés d’émission et sa sensibilité correspondaient étroitement à celles du capteur non modifié lors d’expériences en tube, montrant que l’ancrage n’altérait pas ses performances. Il en fut de même pour le capteur de glutamate, qui resta réactif après ancrage et mettait clairement en évidence le glutamate dans l’espace juste à l’extérieur des cellules.
Écouter les neurones en culture et en tranches
Les chercheurs sont ensuite passés aux cellules nerveuses de l’hippocampe de souris, une région cérébrale importante pour l’apprentissage et la mémoire. Ils ont recouvert ces neurones du capteur de glutamate ancré lipid–PEG et chargé l’intérieur des mêmes cellules avec un colorant calcique distinct qui rend compte de l’activité électrique. En utilisant la microscopie par réflexion interne totale, ils ont pu observer des éclairs rouges de glutamate à la surface cellulaire tandis que des signaux verts à l’intérieur des cellules indiquaient les décharges électriques. Cette vue bicolore a montré que les capteurs ancrés pouvaient suivre la libération spontanée de neurotransmetteurs sans aucune modification génétique des neurones eux-mêmes.
Cartographier des vagues chimiques à travers le tissu cérébral
Ensuite, l’équipe a testé la méthode sur des tranches cérébrales aiguës, qui préservent les connexions naturelles de l’hippocampe. Ils ont appliqué le capteur de potassium ancré aux tranches et stimulé électriquement les fibres nerveuses. Le capteur ancré a produit des augmentations de fluorescence claires et répétables après chaque stimulation, tandis que les capteurs non ancrés diffusaient rapidement et donnaient des signaux faibles et instables. En baignant les tranches dans des solutions de potassium de concentrations connues, et en corrigeant la faible luminescence propre au tissu, les auteurs ont établi une courbe d’étalonnage et estimé les concentrations effectives de potassium extracellulaire. Les niveaux de base étaient d’environ 2,5 millimolaires et montaient à environ 3,4 millimolaires lors de stimulations modestes, en accord avec des mesures électrodes classiques. Les capteurs ancrés pour le potassium et le glutamate ont révélé que ces signaux se propageaient différemment : les variations de glutamate restaient proches des synapses actives, tandis que les augmentations de potassium s’étendaient sur des centaines de micromètres, suggérant des effets plus larges sur l’excitabilité du réseau. 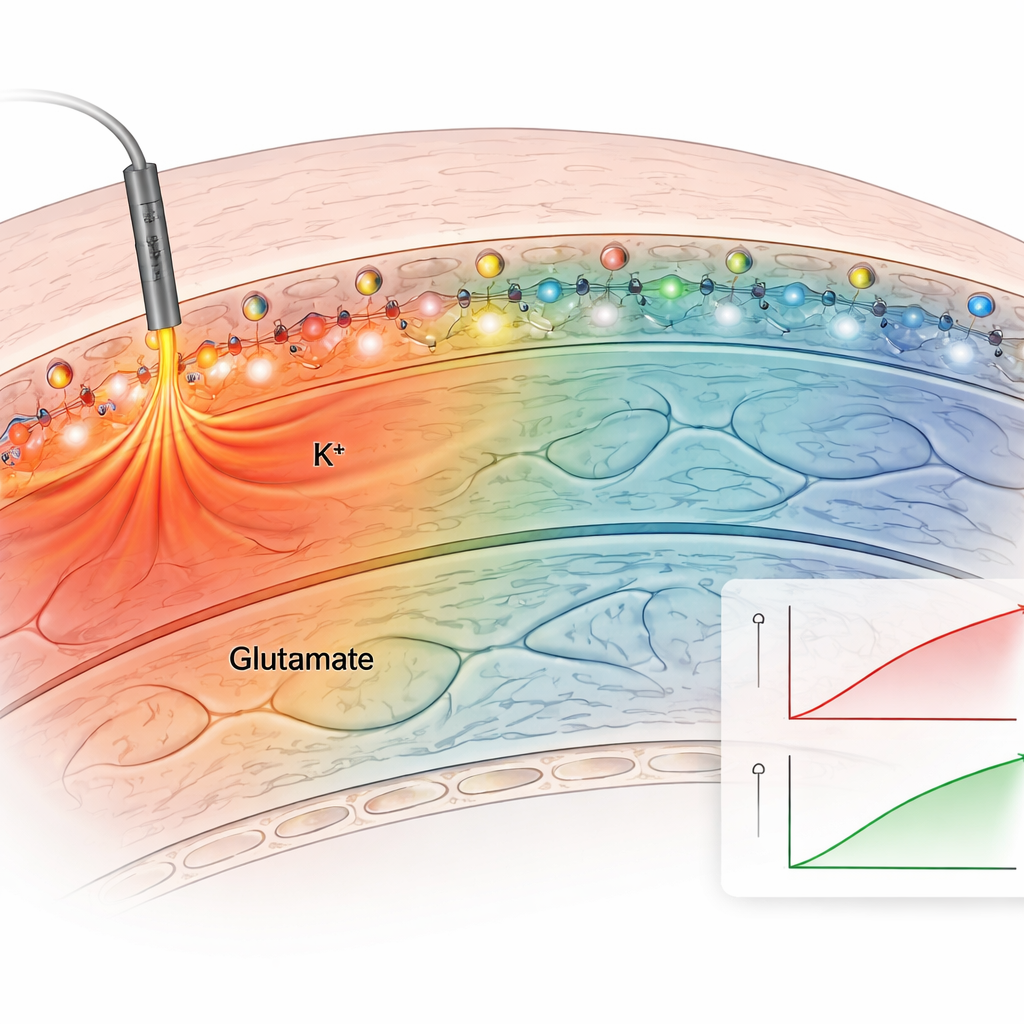
Examiner comment le cerveau génère et élimine les signaux
Parce que les capteurs sont fixés à la surface cellulaire, les auteurs ont pu disséquer les processus qui façonnent ces vagues extracellulaires. Le blocage des transporteurs de glutamate, qui normalement éliminent le glutamate, a entraîné des signaux plus importants et plus durables sur le capteur de glutamate ancré, confirmant que l’absorption locale limite la diffusion du glutamate. Le blocage des récepteurs ionotropes AMPA a réduit à la fois les réponses électriques et les signaux de potassium, indiquant que la majeure partie de l’augmentation du potassium provient des neurones postsynaptiques activés par l’entrée synaptique. Le blocage des canaux sodiques avec la tétrodotoxine a presque abol i les changements de potassium, liant directement ces variations aux potentiels d’action. Ensemble, ces expériences illustrent comment des capteurs ancrés peuvent transformer une chimie distribuée et complexe en films et cartes intuitives.
Pourquoi cela compte pour la recherche cérébrale future
Pour les non-spécialistes, le message clé est que ce travail offre une façon rapide et non génétique d’enrober des cellules et des tissus vivants de capteurs moléculaires très sensibles. Plutôt que de ré-ingénier chaque type cellulaire, les scientifiques peuvent ajouter des protéines capteurs préfabriquées depuis l’extérieur et visualiser immédiatement comment ions et neurotransmetteurs évoluent en temps réel à la surface cellulaire. Cette approche améliore le contrôle, la reproductibilité et la précision spatiale tout en évitant les défis de la délivrance génique, en particulier dans des préparations délicates comme les tranches cérébrales aiguës. À mesure que de nouveaux indicateurs fluorescents seront développés pour d’autres molécules, la même stratégie d’ancrage lipid–PEG pourrait devenir une boîte à outils largement utilisée pour observer le langage chimique des cellules à travers l’organisme.
Citation: Mita, M., Kiyosue, K. & Tani, T. Imaging intercellular biomolecules by using fluorescent protein indicators with lipid-PEG anchors. Sci Rep 16, 6964 (2026). https://doi.org/10.1038/s41598-026-37240-4
Mots-clés: signalisation extracellulaire, biocapteurs fluorescents, imagerie du glutamate, dynamique du potassium, neurones hippocampiques