Clear Sky Science · fr
Convolution de graphe dynamique avec élagage exhaustif et classification GNN pour une détection précise des métastases ganglionnaires
Pourquoi de minuscules modifications dans les ganglions comptent
Lorsque le cancer du sein se propage, sa première halte est souvent les ganglions lymphatiques, de petits filtres situés le long du système de drainage du corps. Savoir si des cellules cancéreuses ont atteint ces ganglions est l’un des indices les plus importants que les médecins utilisent pour choisir la chirurgie, la chimiothérapie et la radiothérapie. Pourtant, même des pathologistes experts peuvent manquer de très petits foyers de cellules cancéreuses sur des images numériques de microscope, surtout lorsqu’ils ressemblent presque à du tissu sain. Cette étude présente un nouveau cadre d’intelligence artificielle qui considère le tissu comme un réseau de régions connectées, lui permettant de repérer des signes subtils de propagation avec une précision remarquable.
Transformer les images de tissu en réseaux
Les chercheurs travaillent sur d’immenses lames numériques colorées de tissu, appelées images en coupe totale (whole-slide images), provenant de biopsies ganglionnaires de cancers du sein. Ces images contiennent des millions de pixels et un mélange déroutant de types cellulaires, de couleurs et de textures. Pour dompter cette complexité, l’équipe nettoie d’abord les images : elle normalise la luminosité et la couleur, réduit le bruit et génère des copies augmentées en faisant pivoter et retourner des fragments, afin que l’algorithme apprenne à gérer la variation naturelle. Chaque fragment d’image est ensuite découpé en petites régions relativement homogènes ("superpixels"), qui deviennent les points — ou nœuds — d’un graphe, tandis que les relations entre régions voisines forment les lignes de connexion — ou arêtes. Cette vue en réseau préserve mieux les formes et agencements irréguliers du tissu réel que les méthodes d’image traditionnelles basées sur une grille.
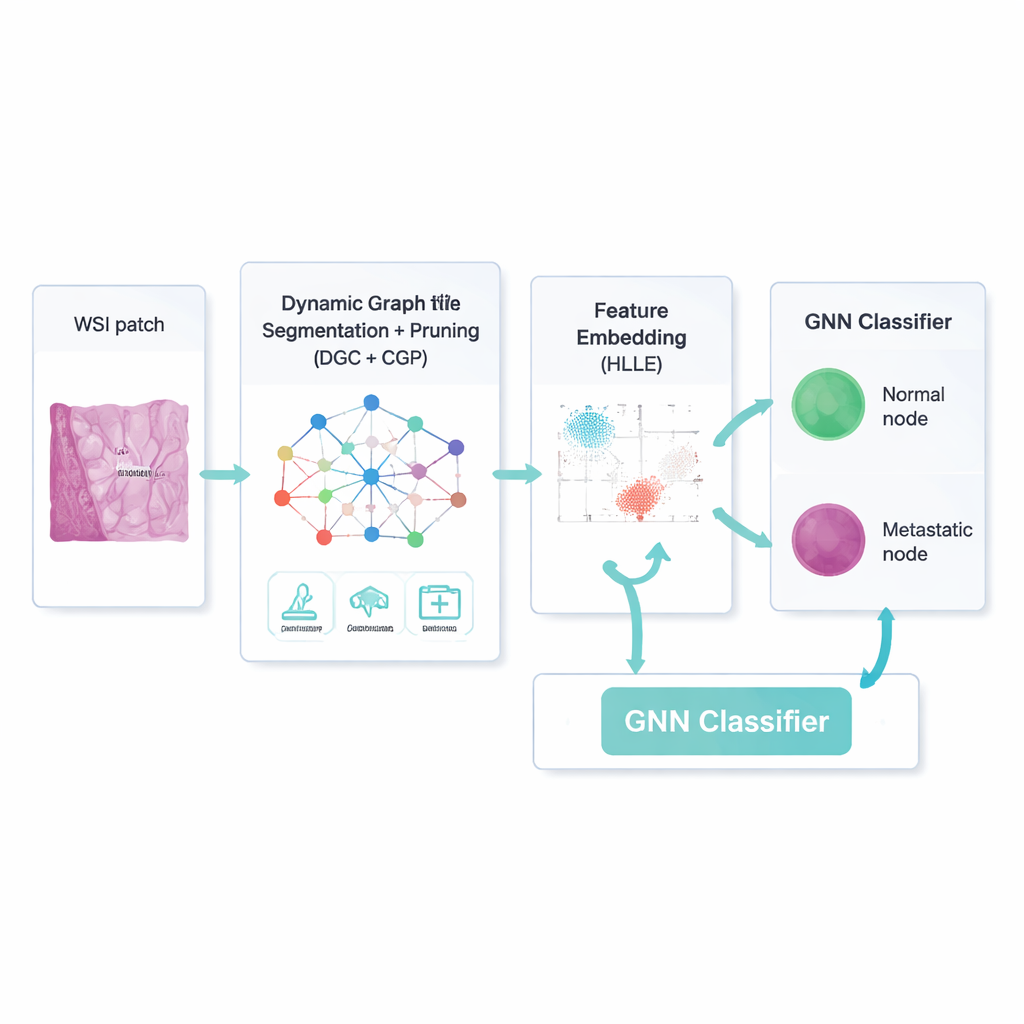
Une façon plus intelligente de se concentrer sur l’essentiel
Construire un réseau ne suffit pas ; de nombreuses connexions et caractéristiques d’image sont non pertinentes voire trompeuses. Le cadre utilise donc un autoencodeur convolutionnel de graphe dynamique — un type de réseau neuronal qui apprend à la fois l’apparence de chaque région et la manière dont les régions s’influencent mutuellement. Un mécanisme supplémentaire d’« attention » apprend au modèle à pondérer certains canaux d’image plus que d’autres, par exemple en mettant l’accent sur les contours à la frontière d’une tumeur. Parallèlement, une stratégie appelée Comprehensive Graph Gradual Pruning taille progressivement les éléments peu utiles : connexions faibles entre régions, caractéristiques numériques moins informatives et poids du modèle à faible impact. Cet élagage se produit pendant l’entraînement, pas après, de sorte que le système apprend à faire plus avec moins, devenant à la fois plus rapide et plus facile à interpréter.
Compresser des motifs sans en perdre la forme
Après que le modèle a isolé les régions ganglionnaires probables du tissu de fond, il doit encore décrire chaque région de manière compacte mais significative. Pour cela, les auteurs utilisent une technique appelée Hessian-based Locally Linear Embedding. En termes simples, elle réduit de nombreuses caractéristiques numériques en un plus petit ensemble tout en essayant de préserver la « forme » courbée de la disposition des exemples dans l’espace des caractéristiques — par exemple comment de minuscules métastases diffèrent des cellules immunitaires normales selon des motifs subtils de texture ou de couleur. Ces descriptions compressées deviennent l’entrée d’un classificateur par réseau de neurones graphique, qui opère à nouveau sur le réseau de régions et leurs connexions épurées, décidant pour chaque nœud s’il est métastatique ou non.
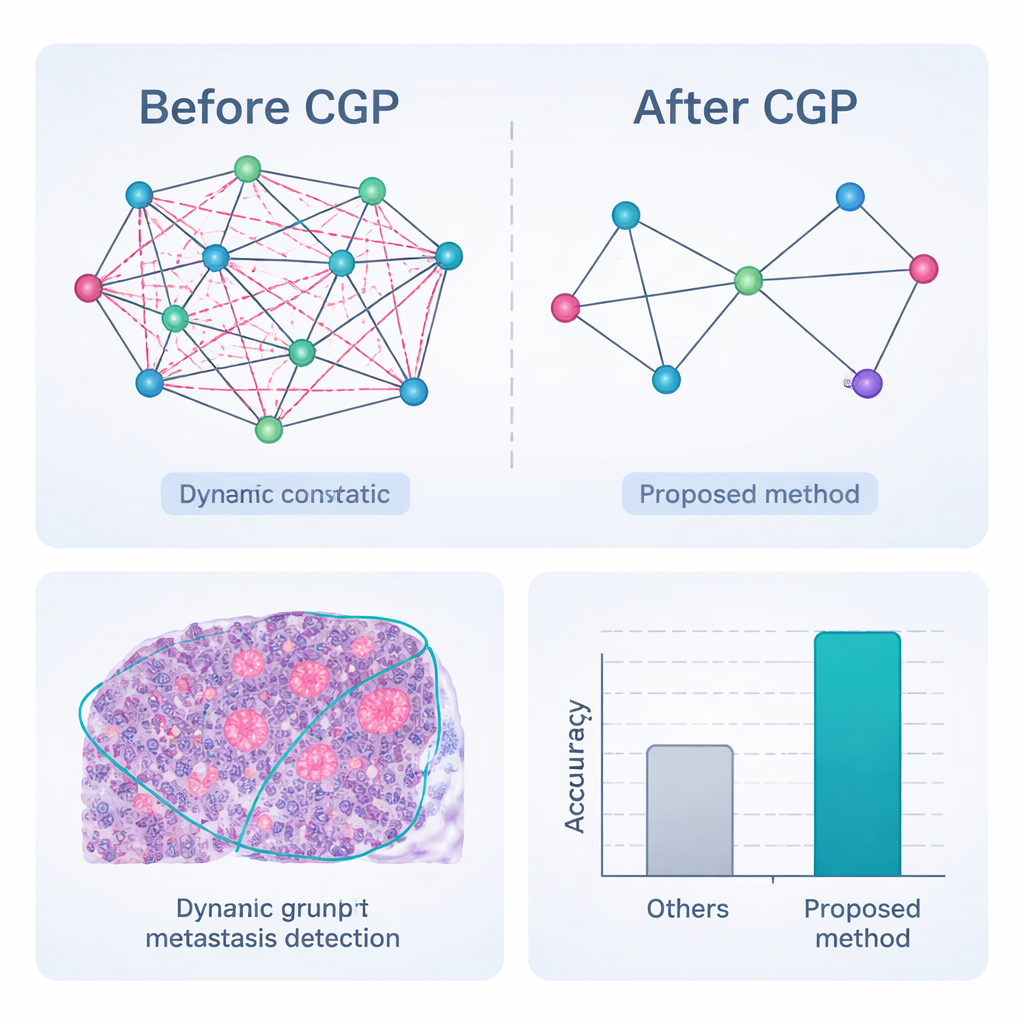
Mettre le cadre à l’épreuve
Le pipeline complet — prétraitement, segmentation dynamique par graphe avec élagage, projection des caractéristiques et classification basée sur le graphe — a été évalué sur CAMELYON17, une collection publique de 1 000 lames ganglionnaires annotées par des experts provenant de patientes atteintes de cancer du sein. Comparée à une gamme de concurrents performants en apprentissage profond, incluant des réseaux convolutionnels populaires et des modèles hybrides à transformeur, la nouvelle méthode a obtenu les meilleurs scores sur presque toutes les mesures. Elle a correctement classé les ganglions comme cancéreux ou non dans 98,65 % des cas et a montré une meilleure concordance avec les contours d’experts des zones tumorales, en particulier pour des métastases très petites ou peu contrastées. Surtout, parce que le graphe est agressivement élagué, le système atteint ces résultats avec beaucoup moins de calculs et une consommation mémoire réduite, le rendant plus adapté à une utilisation en temps réel dans des laboratoires de pathologie à forte activité.
Ce que cela signifie pour les patients et les cliniciens
En termes concrets, ce travail montre comment considérer le tissu comme un réseau de régions connectées intelligemment réduit peut aider les ordinateurs à agir comme des seconds lecteurs extrêmement attentifs des lames ganglionnaires. En concentrant l’attention et la puissance de calcul sur les structures les plus informatives tout en écartant le bruit, le cadre est meilleur pour repérer de minuscules germes de cancer qui pourraient autrement être manqués, et il le fait de manière assez efficace pour être pratique. Bien qu’une validation clinique supplémentaire soit nécessaire, de tels outils pourraient aider les pathologistes à prendre des décisions plus rapides et plus cohérentes sur la présence de propagation du cancer — des informations qui influencent directement les plans de traitement et, en fin de compte, les résultats pour les patients.
Citation: H. N., C., N., S., S., A.R. et al. Dynamic graph convolution with comprehensive pruning and GNN classification for precise lymph node metastasis detection. Sci Rep 16, 6682 (2026). https://doi.org/10.1038/s41598-026-37193-8
Mots-clés: métastase ganglionnaire, pathologie numérique, réseaux de neurones graphiques, segmentation d'images médicales, cancer du sein