Clear Sky Science · fr
Caractérisation structurelle de la liaison des métaux dans la tyrosylprotéine sulfotransférase humaine 2, TPST2
Pourquoi de minuscules ions métalliques comptent pour la signalisation cellulaire
À l’intérieur de nos cellules, d’innombrables machines moléculaires règlent discrètement la croissance des tissus, l’action des hormones et la communication des cellules immunitaires. L’une de ces machines, une enzyme appelée TPST2, ajoute une petite étiquette sulfate à certaines protéines lorsqu’elles traversent le centre d’expédition cellulaire, l’appareil de Golgi. Cette étude révèle comment de simples ions métalliques comme le sodium et le manganèse aident TPST2 à fonctionner plus efficacement en rigidifiant subtilement des parties de sa structure — un aperçu qui pourrait relier l’équilibre minéral des cellules au cancer et aux pathologies liées aux hormones. 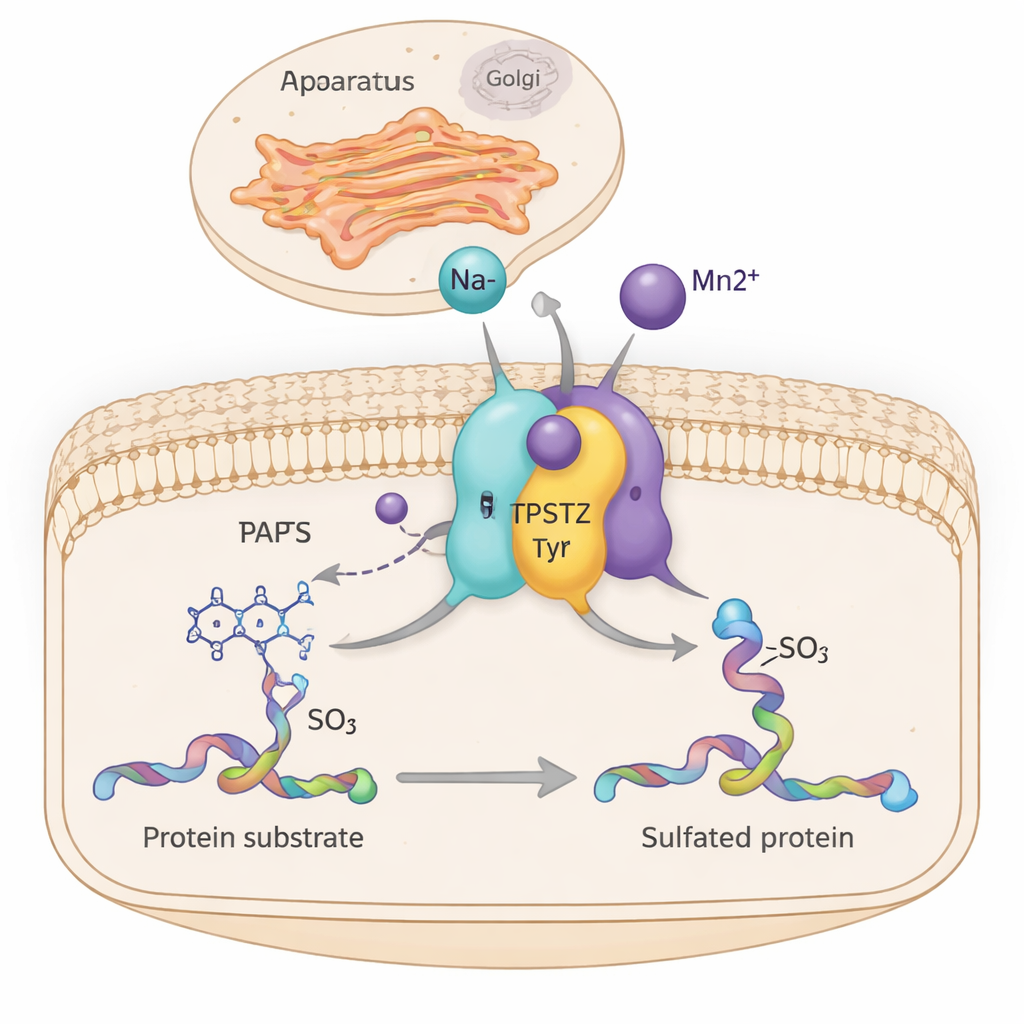
Une protéine qui orne d’autres protéines
TPST2 appartient à une famille d’enzymes qui effectuent la « sulfation de la tyrosine », une modification chimique ajoutée à des résidus tyrosine spécifiques des protéines. Ces protéines sulfées jouent des rôles essentiels en dehors des cellules, influençant la coagulation sanguine, le mouvement des globules blancs, la liaison hormone–récepteur, et même l’entrée des virus dans les cellules. Chez l’homme, il existe deux enzymes principales de sulfation, TPST1 et TPST2, qui sont ancrées dans la membrane du Golgi et modifient les protéines lors de leur préparation à l’exportation. Des études chez la souris montrent que la perte de TPST2 perturbe la production d’hormones thyroïdiennes, freine la croissance et cause l’infertilité masculine, soulignant son importance pour la physiologie normale.
Liens avec le cancer et l’évasion immunitaire
Des travaux récents ont relié TPST2 directement à des maladies. Dans le mélanome, TPST2 modifie un composant du récepteur de l’interféron de manière à affaiblir la signalisation immunitaire, et le blocage de TPST2 renforce l’efficacité des thérapies par points de contrôle immunitaire ciblant PD-1. Dans le cancer du pancréas, une voie dépendante de TPST2 contribue à stabiliser une protéine (intégrine β4) qui favorise la croissance et la diffusion tumorales. Inhiber TPST2 dans ces modèles ralentit la division et l’invasion des cellules cancéreuses. Parce que TPST2 agit sur des protéines à la surface cellulaire, il reconfigure la façon dont les cellules perçoivent et répondent à leur environnement, ce qui en fait une cible attractive pour de nouveaux traitements.
Trouver les « interrupteurs » métalliques
Les biochimistes savent depuis longtemps que TPST2 devient beaucoup plus actif en présence de métaux divalents comme le manganèse (Mn²⁺), mais la raison structurelle faisait défaut. Dans cette étude, les auteurs ont produit le cœur catalytique de la TPST2 humaine et l’ont cristallisé avec un produit secondaire de réaction et soit du sodium (Na⁺), soit du manganèse. À l’aide de cristallographie aux rayons X à haute résolution, ils ont découvert deux petites poches de liaison aux métaux à l’intérieur de l’enzyme, chacune présentant une disposition nettement à six coordonnées (octaédrique) des atomes environnants. En ajustant la longueur d’onde des rayons X aux signatures propres de différents métaux, ils ont confirmé que le Mn²⁺ occupe sélectivement ces sites, tandis que des métaux comme le zinc et le cuivre se lient soit faiblement à d’autres emplacements, soit pas du tout.
Rigidifier des éléments mobiles clés plutôt que remodeler l’ensemble
De façon surprenante, TPST2 avec du sodium et TPST2 avec du manganèse paraissaient presque identiques globalement ; il n’y avait pas d’ouverture ou de fermeture dramatique de la protéine. Au lieu de cela, les métaux affectaient principalement deux régions flexibles près de l’entrée du site actif : une hélice appelée α3 et une boucle proche connue sous le nom de boucle α12–α13. À l’état sans métal ou faiblement lié, ces segments bougent et sont partiellement désordonnés. Lorsque Na⁺ se lie, ils deviennent plus ordonnés ; le Mn²⁺ les verrouille encore davantage, comme le montrent la réduction du mouvement thermique dans les données de diffraction et des analyses informatiques de flexibilité. Cette rigidité accrue élève modestement la température de fusion de l’enzyme et diminuerait le coût « entropique » d’organiser le site actif — facilitant et accélérant la mise en position des substrats pour la sulfation par TPST2. 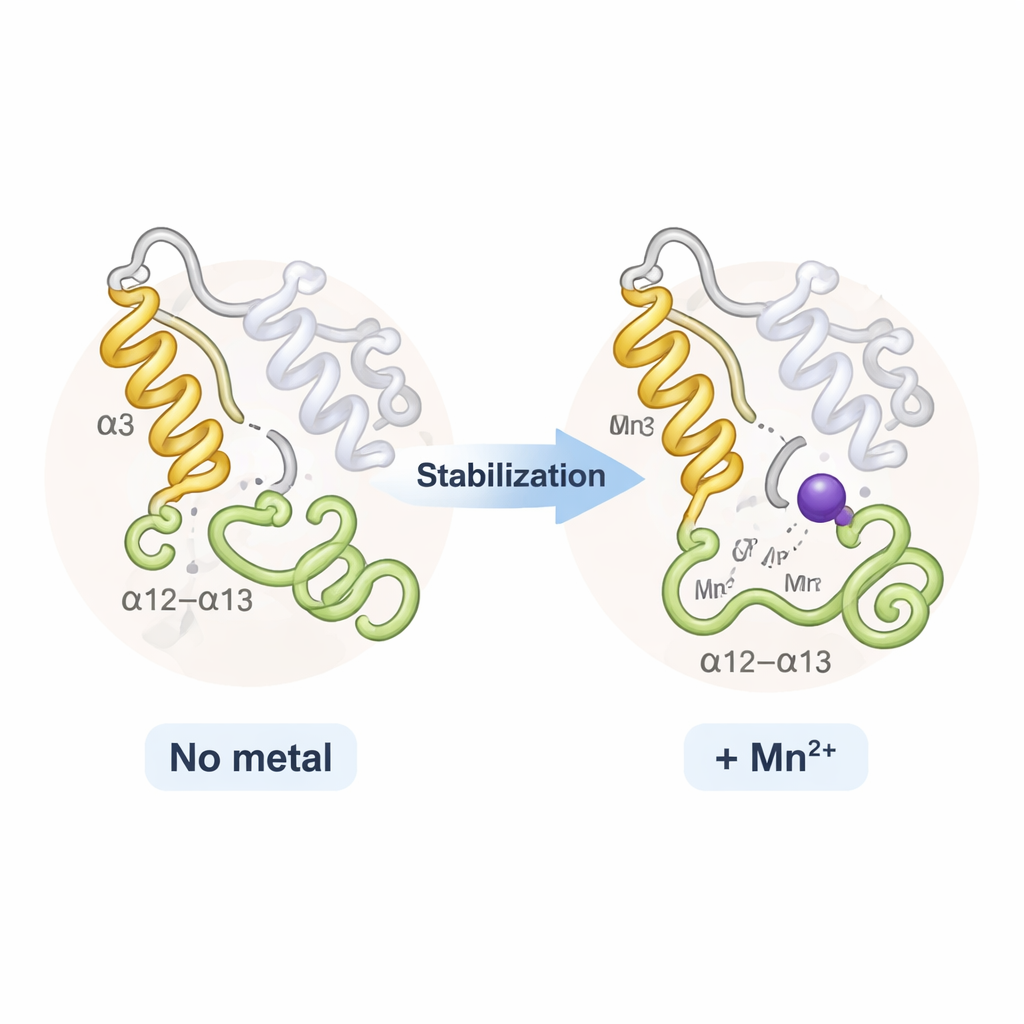
Des minéraux cellulaires au contrôle de la signalisation
Les auteurs proposent un modèle « d’activation par ordonnancement ». En l’absence de métal lié, TPST2 est souple autour de l’entrée du site actif et travaille de manière inefficace. Le sodium, abondant dans les cellules, peut se lier aux mêmes sites et créer un état partiellement ordonné et modérément actif. Le manganèse, présent en quantités micromolaires finement contrôlées au sein du Golgi, se lie plus fortement et verrouille les régions clés dans un état optimal, maximisant l’efficacité catalytique. Cela suggère que de subtiles variations des niveaux de manganèse dans le Golgi pourraient régler l’intensité avec laquelle TPST2 modifie ses cibles. Étant donné que TPST2 influence la production d’hormones et la signalisation tumorale, ce travail met en lumière un lien potentiel entre l’équilibre des ions métalliques, les « décorations » protéiques et la maladie — et fournit un cadre structurel pour concevoir des médicaments modulant l’activité de TPST2 en mimant ou perturbant la liaison des métaux.
Citation: Jin, M., Noh, C., Yang, J. et al. Structural characterization of metal binding in human tyrosylprotein sulfotransferase 2, TPST2. Sci Rep 16, 6066 (2026). https://doi.org/10.1038/s41598-026-37189-4
Mots-clés: sulfation de la tyrosine, TPST2, manganèse, appareil de Golgi, modification des protéines