Clear Sky Science · fr
Apprentissage automatique intégratif et docking moléculaire révèlent que la narirutine cible ABCC1/ABCG2 pour remodeler le microenvironnement immunitaire dans le cancer colorectal
Un composé fruitier porteur de grands espoirs contre le cancer
Le cancer colorectal est l’un des cancers les plus meurtriers au monde, et de nombreux patients subissent encore des traitements rudes et rencontrent la résistance aux médicaments. Cette étude examine la narirutine, une substance naturelle présente dans les agrumes, pour déterminer si elle pourrait aider l’organisme à combattre les tumeurs du côlon de manière plus douce — en modifiant la manière dont les cellules cancéreuses gèrent les médicaments et dont les cellules immunitaires se comportent autour de la tumeur.
De l’agrume à la cible anticancéreuse
Les chercheurs ont commencé par se poser une question simple : si la narirutine était un médicament, quelles parties de nos cellules viserait‑elle ? En utilisant de larges bases de données publiques sur le cancer et des outils informatiques de prédiction, ils ont analysé des milliers de gènes issus de tumeurs du côlon et de tissus sains. Ils ont ensuite croisé ces gènes liés au cancer avec ceux que la narirutine est la plus susceptible d’affecter. Sur plus de 3 000 gènes altérés dans le cancer colorectal, la narirutine était prédite interagir de manière significative avec seulement neuf d’entre eux, et en particulier avec cinq gènes « nŒuds » situés à des points de contrôle clés à l’intérieur des cellules tumorales.
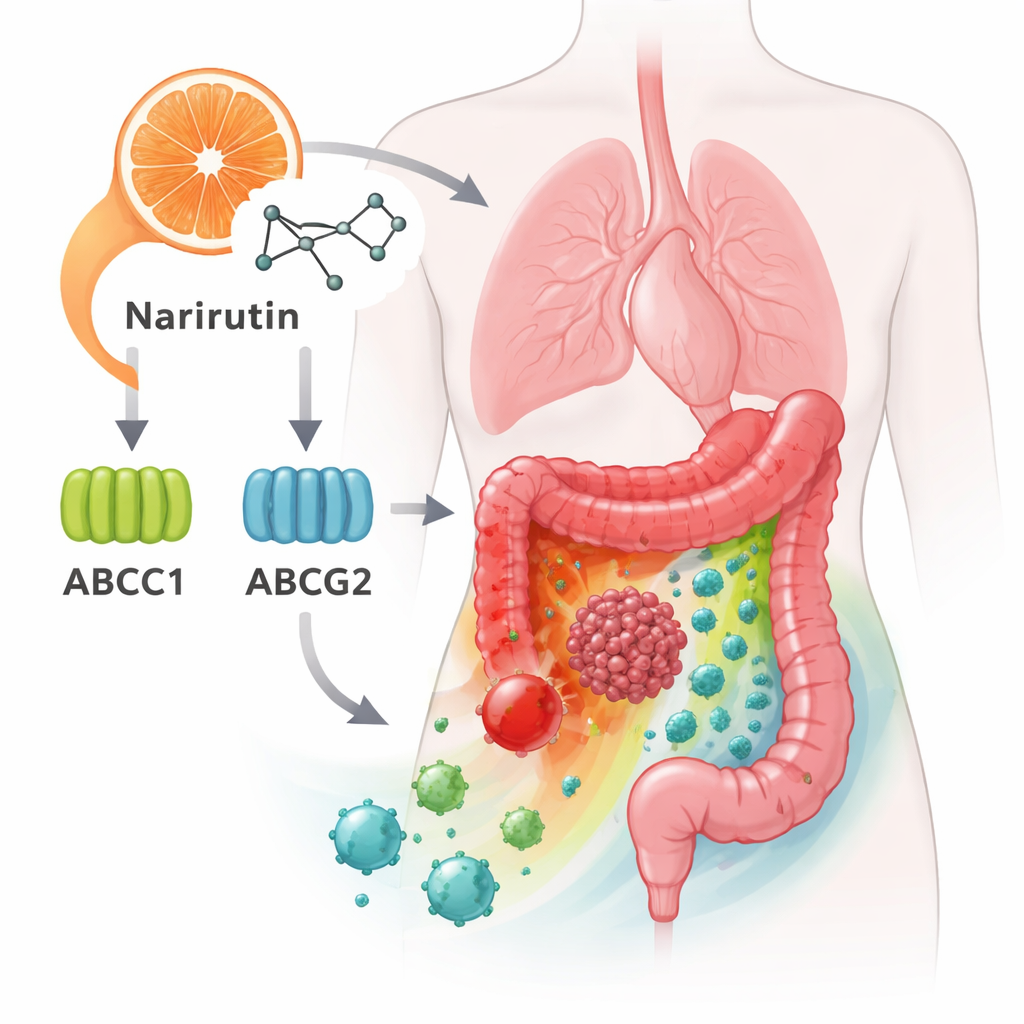
Gardiens clés à la surface des cellules cancéreuses
Parmi ces gènes nŒuds, deux se sont démarqués : ABCC1 et ABCG2. Ils codent des protéines en forme de pompes qui se trouvent dans la membrane externe des cellules et expulsent les médicaments — une des raisons pour lesquelles certains cancers développent une résistance à la chimiothérapie. La nouvelle analyse suggère que la narirutine peut se lier à ces pompes et potentiellement influencer leur fonctionnement. D’autres gènes nŒuds, dont CA12, EPHX2 et PTGS1, participent à la gestion des acides, des lipides et des signaux inflammatoires par la cellule. Ensemble, ces gènes contribuent à déterminer si une tumeur progresse sans contrôle, comment elle répond aux médicaments et comment elle interagit avec les tissus normaux environnants.
Liaison simulée et conséquences dans le monde réel
Pour tester si la narirutine pouvait réellement se fixer à ces protéines cibles, l’équipe a utilisé le docking moléculaire — des modèles informatiques à haute résolution qui prédisent comment une petite molécule s’insère dans une protéine plus grande. Ces simulations ont montré que la narirutine s’emboîte bien dans des poches de ses protéines cibles et établit des contacts stables, ce qui rend la liaison physiquement plausible. Lorsque les chercheurs ont examiné les données patients, ils ont constaté que les gènes nŒuds distinguaient nettement les tissus cancéreux des tissus normaux et étaient liés à la survie. Par exemple, des niveaux plus élevés d’ABCC1 et de PTGS1 étaient généralement associés à de moins bons pronostics, suggérant qu’une réduction de l’expression de ces gènes — potentiellement via des composés comme la narirutine — pourrait être bénéfique.
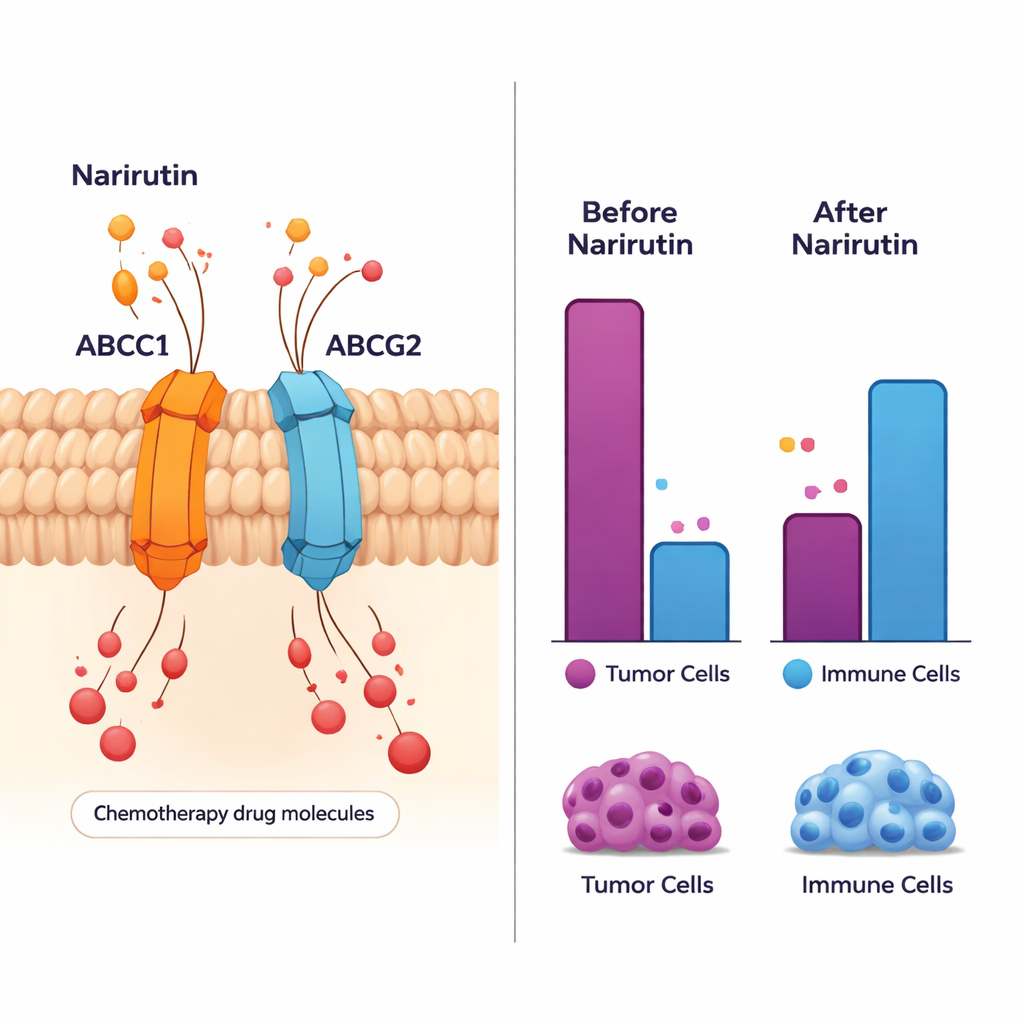
Remodeler le voisinage immunitaire de la tumeur
Le cancer ne se développe pas isolément ; il vit au sein d’un « voisinage » animé de cellules immunitaires, de vaisseaux sanguins et de tissus de soutien. L’étude a examiné 28 types différents de cellules immunitaires autour des tumeurs du côlon et a observé des modifications générales par rapport au tissu sain. Certaines cellules immunitaires bénéfiques, comme des cellules B activées et des sous‑types spécifiques de cellules T, étaient plus abondantes ou se comportaient différemment dans les tumeurs. Les principales cibles de la narirutine, en particulier ABCC1, ABCG2 et PTGS1, présentaient de fortes corrélations avec ces changements immunitaires. Cela suggère qu’en agissant sur ces gènes, la narirutine pourrait non seulement affecter directement les cellules cancéreuses, mais aussi moduler la réponse immunitaire locale — rendant possiblement l’environnement moins propice à la croissance tumorale.
Promesses, mais travail encore nécessaire
En termes simples, cette recherche propose qu’un flavonoïde naturel issu des agrumes pourrait « boucher les pompes » que les cellules cancéreuses utilisent pour échapper à la chimiothérapie et contribuer à réinitialiser le paysage immunitaire autour des tumeurs du côlon. Le travail repose sur des analyses informatiques puissantes et de larges jeux de données génétiques, plutôt que sur des essais en laboratoire ou cliniques, et constitue donc une étape précoce mais importante. Si des expérimentations futures sur des cellules, des animaux et des patients confirment ces prédictions, la narirutine — ou des médicaments inspirés par elle — pourrait un jour faire partie de thérapies combinées rendant les traitements standards du cancer colorectal plus efficaces et moins sujets à la résistance.
Citation: Bian, R., Wang, H., Zhang, H. et al. Integrative machine learning and molecular docking reveal Narirutin targets ABCC1/ABCG2 for immune microenvironment remodeling in colorectal cancer. Sci Rep 16, 7649 (2026). https://doi.org/10.1038/s41598-026-37181-y
Mots-clés: cancer colorectal, narirutine, résistance aux médicaments, microenvironnement tumoral, modulation immunitaire