Clear Sky Science · fr
Évaluation multimodale par imagerie du microenvironnement hypoxique de la moelle osseuse et des lésions des vaisseaux de type H dans le diabète
Pourquoi la santé des os compte dans le diabète
On associe souvent le diabète de type 1 à la glycémie et à l’insuline, mais la maladie remodèle aussi silencieusement le squelette. De nombreux patients développent des os fragilisés et présentent un risque accru de fractures, même lorsque leurs tests de densité osseuse apparaissent presque normaux. Cette étude explore ce qui se passe au cœur de la moelle osseuse chez des lapins modèles du diabète, en utilisant des techniques d’imagerie médicale avancées pour observer en direct les petits vaisseaux et les niveaux d’oxygène. Comprendre ce dommage caché pourrait ouvrir la voie à un diagnostic plus précoce et à de nouveaux traitements protégeant la solidité osseuse des personnes vivant avec le diabète.
Les voies sanguines cachées de l’os
À l’intérieur des os longs comme le tibia se trouve une riche forêt de vaisseaux sanguins qui non seulement nourrissent l’os, mais en guident aussi la croissance et la réparation. Parmi ces vaisseaux se trouve un sous-type particulier appelé « vaisseaux de type H », regroupés près des extrémités osseuses où se situent les plaques de croissance et un remodelage osseux actif. Ces vaisseaux transportent davantage d’oxygène que d’autres et sont étroitement liés à la formation de nouvel os. Dans le diabète de type 1, toutefois, une hyperglycémie chronique déclenche des sous-produits chimiques et un stress oxydatif qui peuvent étouffer ce système finement réglé. Les chercheurs ont cherché à visualiser, chez des animaux vivants, comment ces changements se déroulent dans différentes régions de l’os.
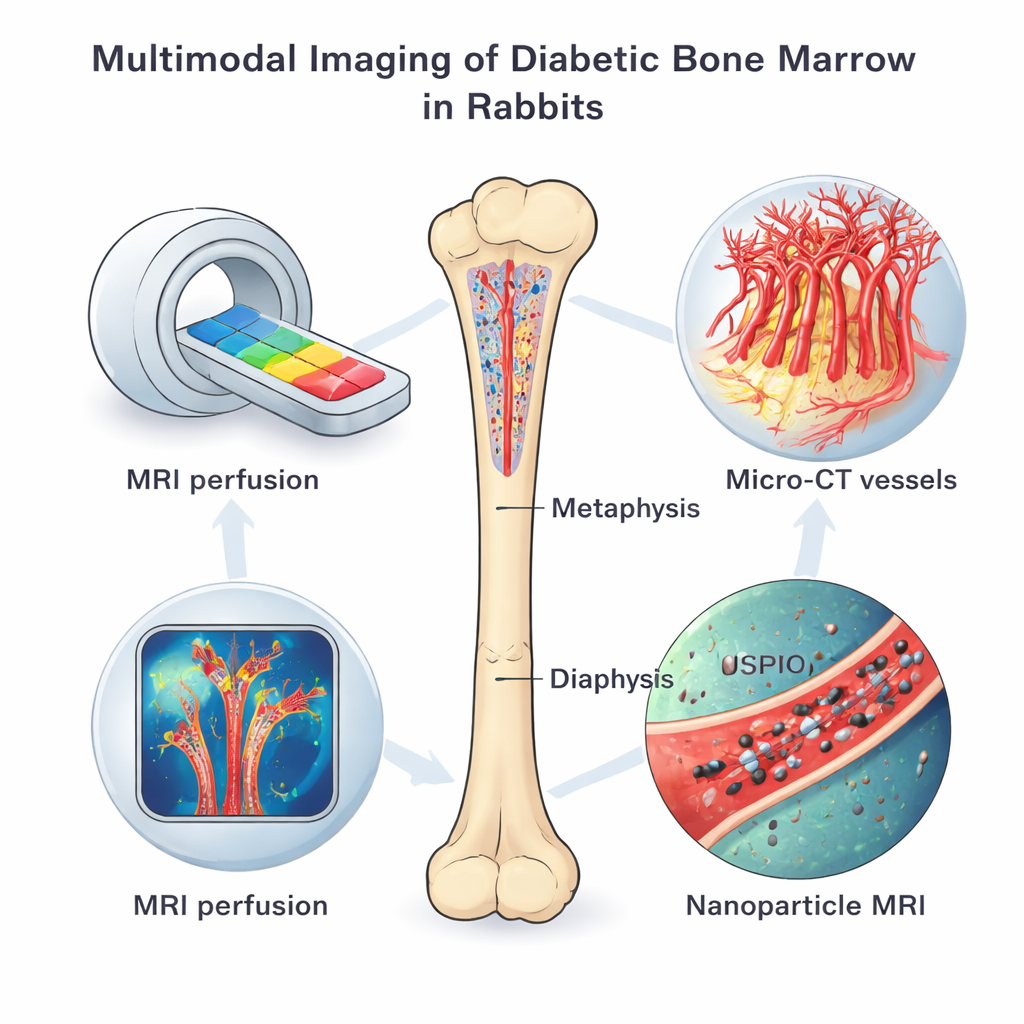
Scanner l’os vivant sous plusieurs angles
L’équipe a utilisé une batterie d’outils d’imagerie sur des lapins atteints de diabète de type 1 induit chimiquement et sur des témoins sains, tous étudiés quatre mois après l’établissement du diabète. Une IRM dynamique avec agent de contraste a suivi la vitesse d’entrée et de sortie d’un colorant dans la moelle osseuse, révélant la perfusion des microvaisseaux et leur perméabilité. Une autre technique d’IRM, enrichie par des nanoparticules à base de fer, a montré à quel point les cellules endothéliales prenaient activement ces particules, signe d’un métabolisme et d’un comportement vasculaire altérés. Après le sacrifice des animaux, des micro-CT à haute résolution ont cartographié le réseau tridimensionnel des microvaisseaux, tandis que des colorations fluorescentes, des tests génétiques et la microscopie électronique ont examiné en détail les types de vaisseaux, les protéines sensibles à l’oxygène et les dommages cellulaires.
Où le diabète frappe le plus fort à l’intérieur de l’os
À travers toutes les méthodes d’imagerie, les lapins diabétiques présentaient des vaisseaux de la moelle osseuse plus perméables et anormaux que ceux des animaux sains. Le colorant de contraste circulait plus vite et persistait plus longtemps, et les nanoparticules de fer étaient captées de façon plus intense, surtout près de la métaphyse — la région terminale de l’os riche en vaisseaux de type H. La micro-CT a révélé que les os diabétiques avaient beaucoup moins de petits vaisseaux et un volume vasculaire global réduit, au point que l’avantage habituel de la métaphyse par rapport à la diaphyse disparaissait. La cytométrie en flux et le marquage fluorescent ont confirmé que la proportion de vaisseaux de type H elle-même chutait fortement dans le diabète, tandis que les nouveaux bourgeonnements vasculaires le long de la plaque de croissance devenaient rares. En bref, la niche vasculaire qui soutient normalement une formation osseuse robuste était sélectivement amincie et endommagée.
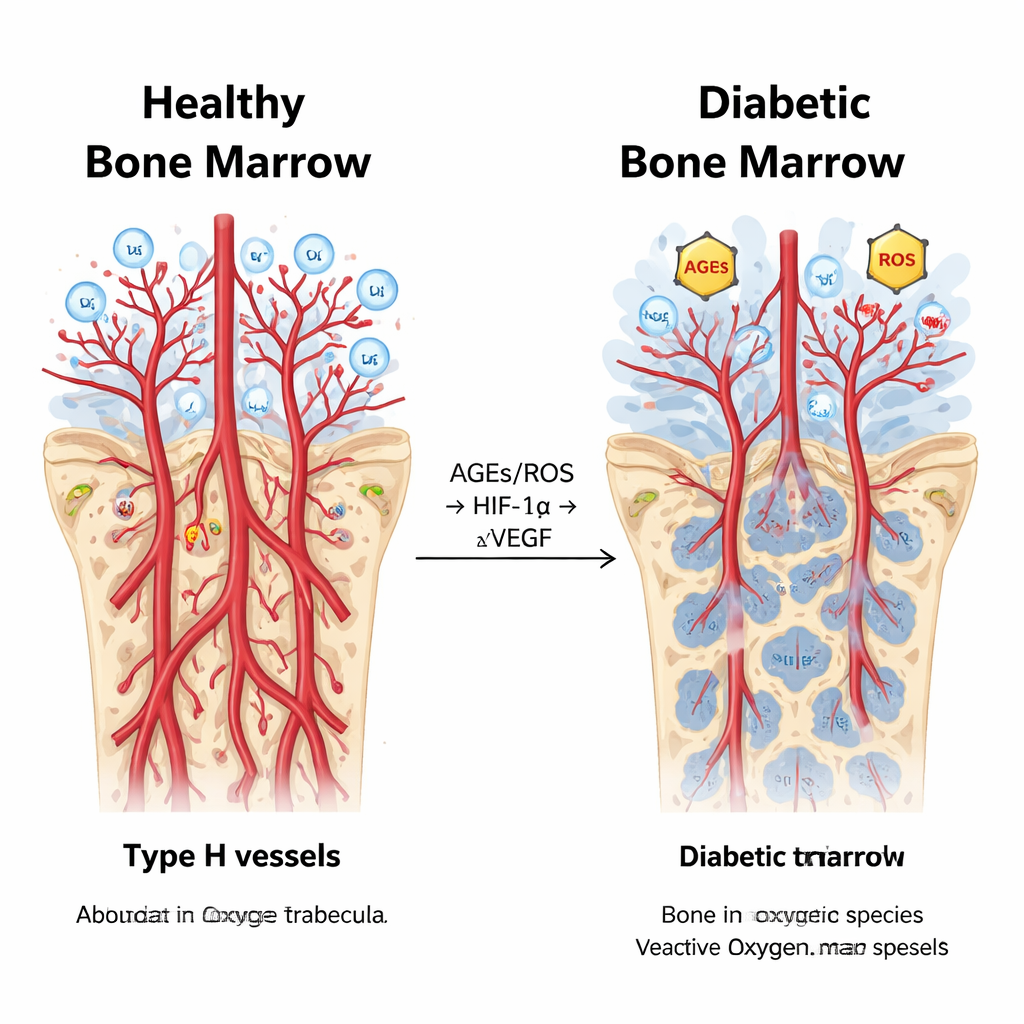
Une cascade chimique embrouillée dans la moelle diabétique
En creusant plus loin, les scientifiques ont mesuré des molécules impliquées dans l’hypoxie — le manque d’oxygène suffisant — et dans le stress oxydatif induit par l’hyperglycémie. Les lapins diabétiques présentaient des niveaux plus élevés de produits de glycation avancée (AGE) et d’espèces réactives de l’oxygène (ROS), ainsi qu’une activité renforcée de la protéine détectrice d’oxygène HIF-1α et de son récepteur partenaire AGER, en particulier dans la métaphyse. De façon surprenante, bien que HIF-1α favorise normalement la croissance vasculaire, le signal clé de croissance VEGF était en réalité supprimé dans la moelle osseuse diabétique, et le bourgeonnement vasculaire diminuait. Les analyses statistiques ont lié ces éléments : les marqueurs du stress oxydatif et de la perfusion anormale augmentaient et diminuaient en parallèle avec HIF-1α, tandis que le VEGF et les mesures de densité vasculaire évoluaient en sens inverse. Ce schéma suggère que dans le diabète chronique, le système d’alarme à l’oxygène est détourné, entraînant inflammation et fuite vasculaire au lieu d’une formation saine de vaisseaux et d’os.
Ce que cela signifie pour les personnes atteintes de diabète
En termes simples, l’étude montre que le diabète n’amincit pas les os de manière uniforme ; il crée des « points chauds » localisés de lésions vasculaires et d’hypoxie, en particulier là où l’os devrait être le plus solide et le plus régénératif. En combinant plusieurs méthodes d’imagerie, les chercheurs ont pu voir à la fois la fuite fonctionnelle et la perte structurelle des vaisseaux de type H, et relier ces changements à une voie biochimique précise impliquant les AGE, les ROS, HIF-1α et le VEGF. Pour les patients, ce travail suggère que des examens à venir pourraient un jour détecter précocement les dommages osseux avant l’apparition de fractures, et que des thérapies visant à restaurer une signalisation de l’oxygène saine et à protéger les vaisseaux de type H pourraient devenir un nouvel axe pour prévenir la maladie osseuse diabétique.
Citation: Lei, H., Wang, K., Li, L. et al. Multimodal imaging evaluation of hypoxic bone marrow microenvironment and type H vascular injury in diabetes. Sci Rep 16, 7206 (2026). https://doi.org/10.1038/s41598-026-37164-z
Mots-clés: diabète de type 1, moelle osseuse, lésion microvasculaire, hypoxie, fragilité osseuse