Clear Sky Science · fr
Le refroidissement ultra-rapide sur double surface solide sous pression améliorée améliore la récupération après décongélation des hépatocytes et des tranches de foie coupées avec précision
Pourquoi la congélation du tissu hépatique est importante
Maintenir des cellules et des tissus vivants en dehors du corps est l’un des piliers discrets de la médecine moderne. Des cellules hépatiques congelées aident les chercheurs à tester de nouveaux médicaments, modéliser les maladies et, peut‑être un jour, réparer des organes défaillants. Mais congeler du matériel vivant est délicat : si des cristaux de glace se forment à l’intérieur ou entre les cellules, ils déchirent les structures fragiles. Cette étude explore une nouvelle manière de congeler des cellules hépatiques et des tranches de foie fines si rapidement et dans des conditions si contrôlées que les cristaux de glace dommageables ont à peine le temps de se former.
Le problème de la glace et des protecteurs chimiques
La cryoconservation conventionnelle repose sur deux outils imparfaits : le froid et les produits chimiques. À mesure que les échantillons sont refroidis, l’eau a tendance à former de la glace, qui peut perforer les membranes et perturber les tissus. Pour lutter contre cela, les scientifiques ajoutent des agents cryoprotecteurs, comme le diméthylsulfoxyde (DMSO), qui aident l’eau à se solidifier sous une forme vitreuse plutôt qu’en cristaux. Cependant, aux concentrations élevées généralement utilisées, ces agents peuvent eux‑mêmes être toxiques pour les cellules ou provoquer des gonflements et contractions dommageables lorsqu’ils pénètrent et sortent des tissus. L’objectif des auteurs était de réduire la quantité de DMSO nécessaire tout en évitant la formation de glace nocive, rendant ainsi la conservation de cellules et de tissus hépatiques plus sûre et plus pratique.
Une nouvelle manière de presser et refroidir simultanément
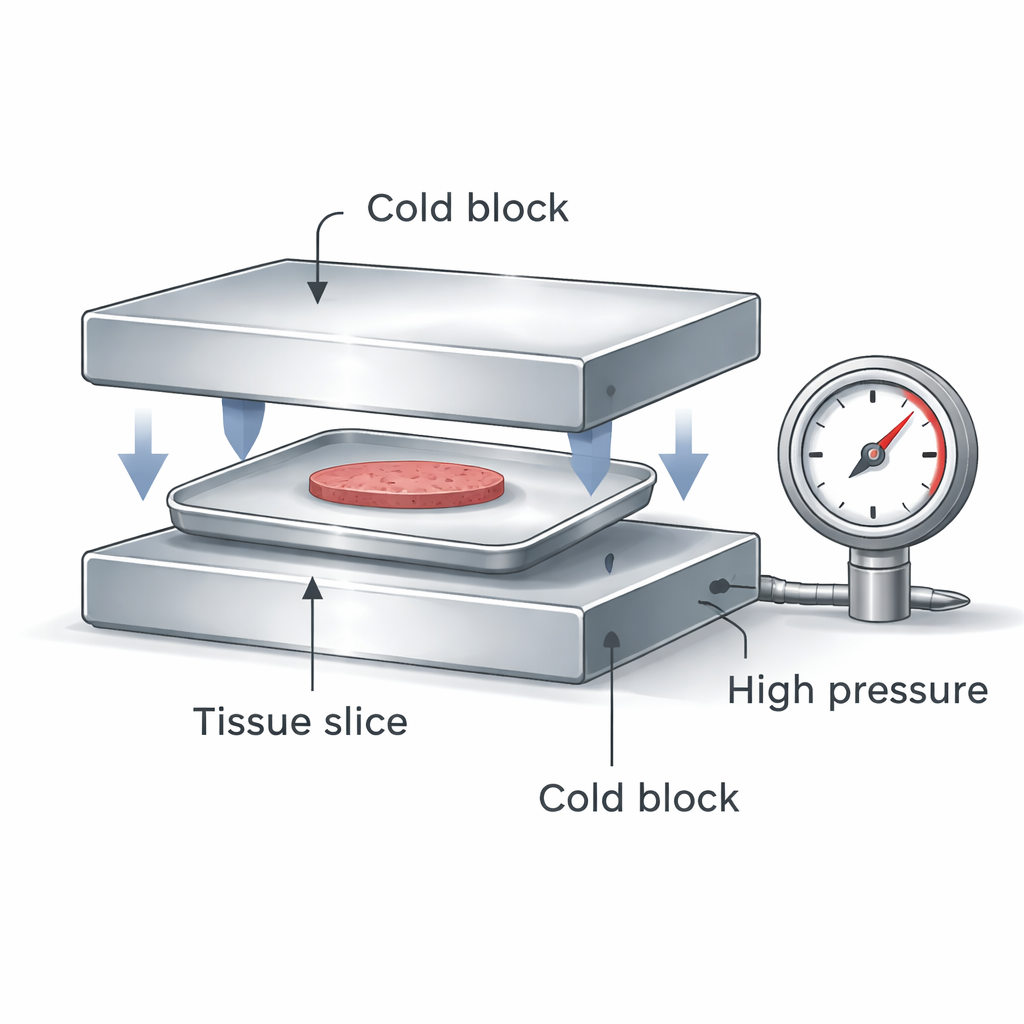
L’équipe a conçu un dispositif compact qui enferme un contenant plat en aluminium scellé, contenant des cellules hépatiques ou des tranches de foie coupées avec précision, entre deux blocs métalliques extrêmement froids. Quand les blocs se referment, ils accomplissent deux choses importantes à la fois : ils créent une haute pression à l’intérieur du contenant scellé et ils extraient la chaleur de l’échantillon à la fois par le dessus et par le dessous. La haute pression modifie le comportement de l’eau de sorte que la glace se forme à des températures plus basses et que la solution vitrifie plus facilement. Le contact double face assure une vitesse de refroidissement beaucoup plus rapide et plus uniforme qu’en plongeant simplement une fiole en plastique dans l’azote liquide, et le contenant scellé maintient l’échantillon isolé de toute contamination.
Trouver le juste équilibre entre sécurité et survie
Pour vérifier si cette approche était assez douce pour du matériel vivant, les chercheurs ont d’abord contrôlé que le contenant en aluminium lui‑même n’endommageait pas les cellules dérivées du foie HepG2 pendant les brèves manipulations utilisées. La survie cellulaire est restée essentiellement inchangée. Ils ont ensuite exposé ces cellules à différents niveaux de DMSO avant congélation et ont confirmé un compromis bien connu : plus de DMSO supprime mieux la glace mais devient clairement toxique à 30 %, tandis que 20 % reste globalement tolérable. Pour les tranches de foie de souris, ils ont testé quelle pression le tissu pouvait supporter en l’absence de congélation. Des impulsions brèves allant jusqu’à 150 mégapascals ont eu peu d’effet sur la viabilité, mais 200 mégapascals ont entraîné environ 30 % de perte, marquant une limite supérieure pour un fonctionnement sûr.
Des tranches de foie mieux préservées après décongélation
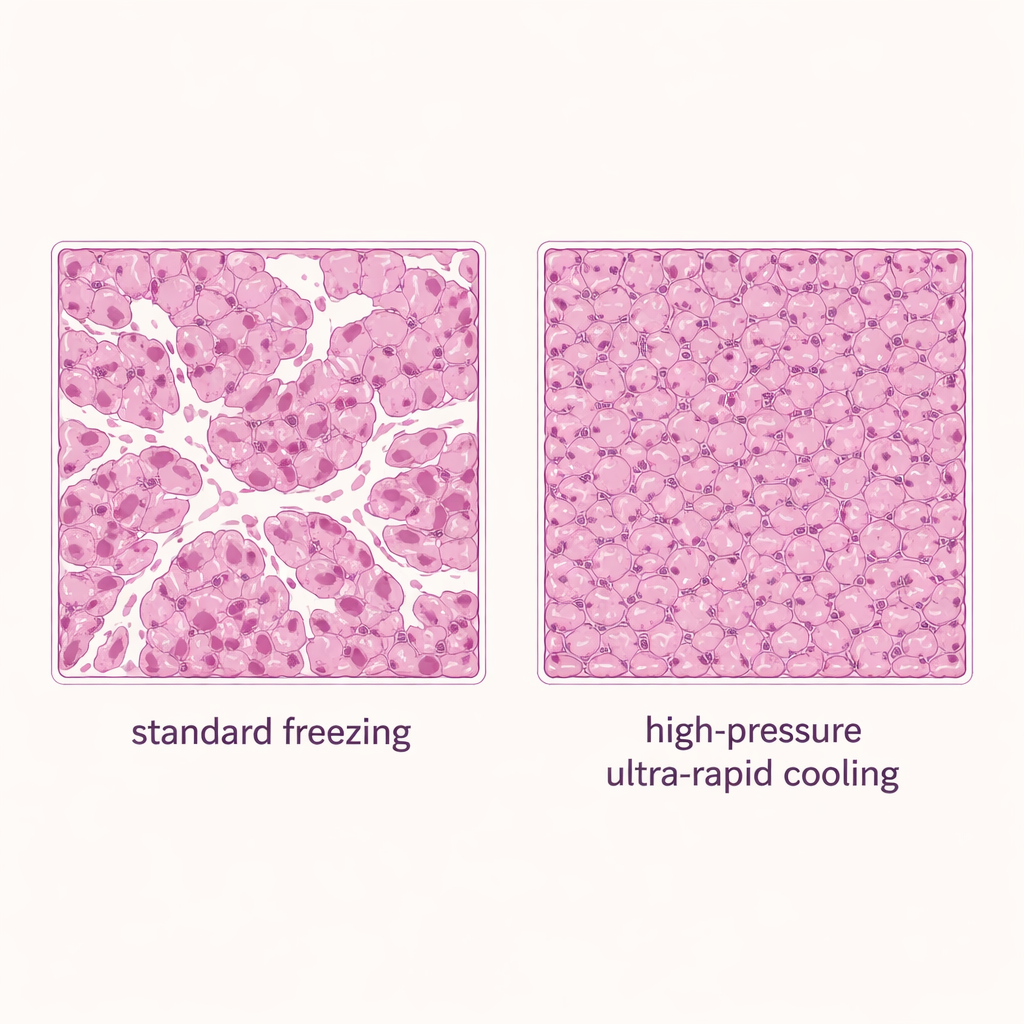
Une fois les plages sûres établies, les auteurs ont comparé trois méthodes de congélation pour les tranches de foie : l’immersion standard du contenant scellé dans l’azote liquide (une approche par convection ou fluide), le refroidissement par surface solide sans pression ajoutée, et le refroidissement par surface solide avec haute pression à 150 mégapascals. Tous les groupes ont utilisé 20 % de DMSO. La méthode assistée par pression a donné les meilleurs résultats : environ 80 % de la viabilité initiale du tissu a été conservée, surpassant à la fois la congélation standard et le refroidissement sur surface solide seul. La microscopie de coupes tissulaires colorées corrobore ces résultats. Les échantillons congelés par immersion conventionnelle montraient de nombreux espaces blancs ouverts — signatures de dommages dus à la glace — tandis que le refroidissement sur surface solide amélioré par la pression produisait un tissu plus dense et plus intact avec beaucoup moins de vides.
Ce que cela signifie pour la conservation future des tissus
Globalement, l’étude montre que comprimer une tranche de foie scellée dans un boîtier en aluminium entre deux blocs ultra‑froids sous haute pression soigneusement contrôlée peut grandement améliorer la survie du tissu après décongélation. En combinant un refroidissement plus rapide et plus homogène avec un comportement de l’eau modifié par la pression, la méthode limite la croissance de glace dommageable tout en utilisant une concentration modérée et cliniquement familière de DMSO. Pour un lecteur non spécialiste, la conclusion est que l’ingénierie intelligente — la manière dont nous emballons et refroidissons les tissus — peut être aussi importante que les produits chimiques que nous ajoutons. Cette approche double face sous haute pression pourrait devenir une étape vers une conservation des tissus hépatiques, et éventuellement d’autres organes, plus sûre et plus fiable pour la recherche et la thérapie.
Citation: Amini, M., Benson, J.D. Pressure enhanced dual-solid-surface ultra-rapid cooling improves post-thaw recovery in hepatocytes and precision cut liver slices. Sci Rep 16, 5994 (2026). https://doi.org/10.1038/s41598-026-37136-3
Mots-clés: cryoconservation, tissu hépatique, vitrification, refroidissement sous haute pression, congélation sans glace