Clear Sky Science · fr
DANEELpath outils d’analyse numérique open source pour la recherche histopathologique dans des modèles de neuroblastome
Pourquoi de minuscules tumeurs en gel comptent
Le cancer n’est pas seulement une masse de cellules rebelles ; c’est tout un voisinage où les cellules communiquent entre elles et avec l’échafaudage qui les entoure. Dans les cancers pédiatriques comme le neuroblastome, cette structure de soutien environnante peut favoriser la croissance tumorale et la résistance aux traitements. Cette étude présente DANEELpath, un ensemble d’outils numériques gratuits et open source qui transforme les images au microscope de mini-tumeurs cultivées en laboratoire en cartes quantitatives riches. Ce faisant, il aide les scientifiques à comprendre comment les cellules tumorales s’organisent, comment elles répondent aux molécules expérimentales et comment ces connaissances pourraient se traduire par de meilleurs traitements pour les enfants.
Construire de petits mondes tumoraux en laboratoire
Pour imiter l’environnement complexe d’une vraie tumeur, les chercheurs cultivent des cellules de neuroblastome dans des hydrogels 3D souples à base de gélatine et de soie. Dans ce contexte, les cellules forment naturellement des amas sphériques, un peu comme de minuscules tumeurs. Un acteur clé de cet environnement est la vitronectine, une protéine adhésive de la matrice extracellulaire qui aide les cellules à s’attacher et peut favoriser une maladie plus agressive. L’équipe a préparé des hydrogels avec et sans vitronectine supplémentaire et a exposé certains d’entre eux au cilengitide, un médicament expérimental qui bloque des récepteurs cellulaires liés à la vitronectine. Après des semaines de croissance, les gels ont été sectionnés, colorés et scannés en images entières à haute résolution, créant une version numérique de chaque mini-monde tumoral.
Transformer des images complexes en motifs mesurables
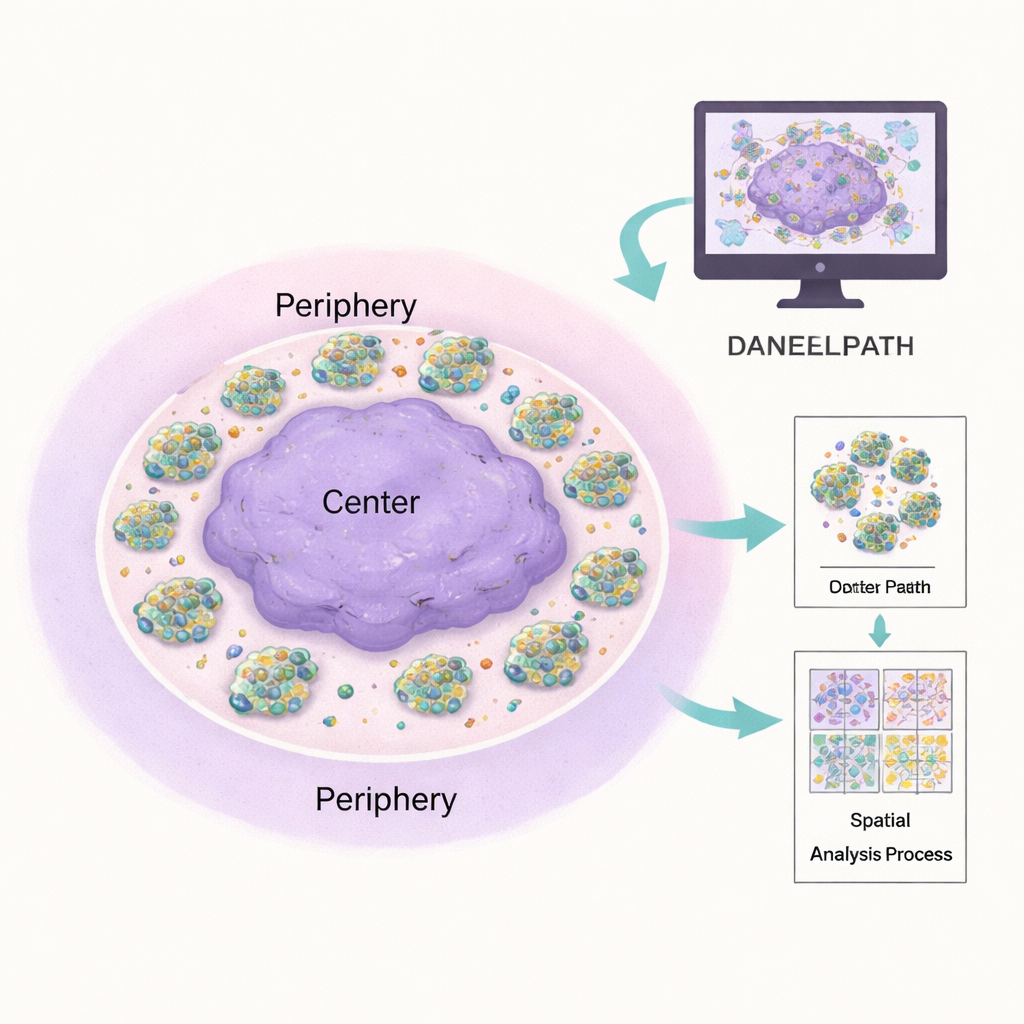
La pathologie traditionnelle repose sur l’œil expert au microscope, ce qui est puissant mais difficile à standardiser et à mettre à l’échelle. DANEELpath s’intègre à la plateforme open source populaire QuPath et automatise une grande partie de ce travail. À l’aide de modèles d’apprentissage profond appelés U-Net, la boîte à outils peut délimiter avec précision chaque amas cellulaire sur des colorations courantes, même lorsque les amas varient de quelques cellules à plusieurs centaines. Elle applique ensuite des méthodes mathématiques pour diviser chaque hydrogel de forme irrégulière en un anneau « centre » et un anneau « périphérie » équilibrés, garantissant que les comparaisons entre régions internes et externes sont justes, quelle que soit la forme du gel. Cela a permis aux auteurs de confirmer que les amas de neuroblastome tendent à être plus denses vers le bord de l’hydrogel et que ce motif change selon la teneur en vitronectine et le traitement médicamenteux.
Mesurer l’espacement cellulaire et les voisins des amas
Au-delà du simple comptage des amas, DANEELpath étudie comment les cellules et les amas sont organisés dans l’espace. À l’intérieur de chaque amas, un autre outil détecte les noyaux cellulaires individuels et mesure la distance jusqu’au voisin le plus proche, résumant ainsi la compacité des cellules. Entre les amas, la boîte à outils propose trois façons de définir les « voisins », y compris une méthode basée sur les diagrammes de Voronoi qui trace des zones d’influence autour de chaque amas. En comparant ces mesures dans différentes conditions, les chercheurs ont montré que le cilengitide modifie le nombre de voisins qu’un gros amas possède et la distribution de ces voisins, mais de façons qui dépendent de la présence ou non de vitronectine dans le gel. Cela illustre comment la matrice environnante et les médicaments mécaniques façonnent ensemble l’organisation tumorale.
Observer l’auréole autour des amas tumoraux
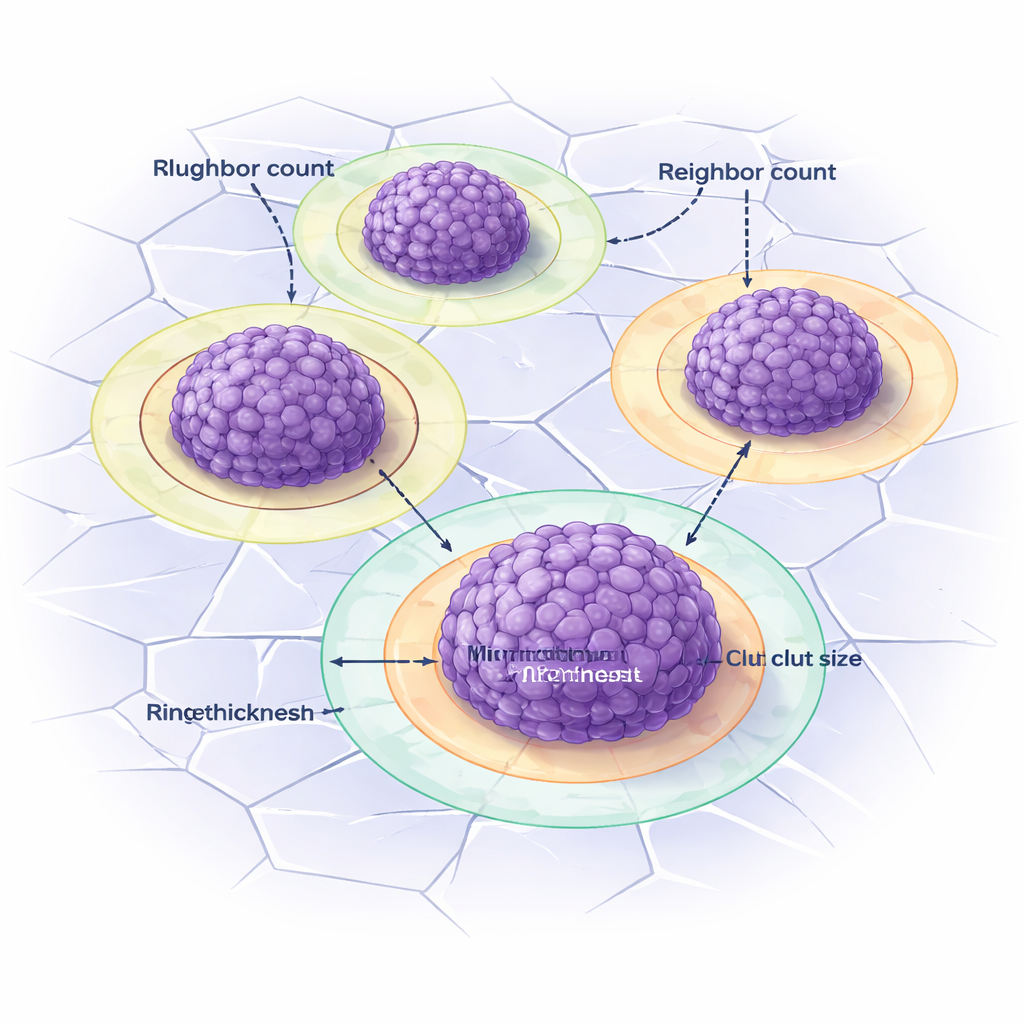
La vitronectine dans ces modèles forme souvent des anneaux saillants autour des amas : une « corona » brillante lorsque seule la vitronectine produite par les cellules est présente, et un halo pâle lorsque de la vitronectine supplémentaire est intégrée au gel. Séparer ces anneaux du cœur de l’amas est délicat à l’œil nu. DANEELpath s’y attaque en traçant d’abord des régions d’influence basées sur Voronoi autour de chaque amas, puis en s’étendant vers l’extérieur juste assez pour capturer l’anneau sans empiéter sur les voisins. Des règles simples de contraste d’image sont utilisées pour détecter coronas et halos, et la boîte à outils mesure automatiquement leur épaisseur. Des stratégies similaires ont aussi été appliquées à des échantillons de patients réels, par exemple pour cartographier les cellules immunitaires au bord des régions tumorales ou définir des zones autour des vaisseaux sanguins afin d’étudier la disposition de la vitronectine et d’autres marqueurs dans le neuroblastome humain.
Ce que cela signifie pour la recherche future sur le cancer
En substance, ce travail transforme des images pathologiques statiques en mesures détaillées et reproductibles de l’organisation des cellules tumorales et de leur environnement. Pour les non-spécialistes, cela signifie que les chercheurs peuvent désormais tester plus facilement comment de nouveaux médicaments, matériaux d’échafaudage ou modifications génétiques modifient non seulement la croissance tumorale, mais aussi sa distribution spatiale. Parce que DANEELpath est open source, fonctionne via une interface graphique et tourne sur des ordinateurs ordinaires, il abaisse la barrière pour que des laboratoires du monde entier adoptent l’analyse d’images avancée. Avec le temps, de tels outils pourraient aider à relier des motifs observés dans des modèles 3D et des tissus de patients aux résultats cliniques, guidant des traitements plus ciblés et efficaces pour les enfants atteints de neuroblastome à haut risque.
Citation: Vieco-Martí, I., López-Carrasco, A., Navarro, S. et al. DANEELpath open source digital analysis tools for histopathological research in neuroblastoma models. Sci Rep 16, 6162 (2026). https://doi.org/10.1038/s41598-026-37134-5
Mots-clés: neuroblastome, pathologie numérique, hydrogels 3D, matrice extracellulaire, apprentissage profond