Clear Sky Science · fr
Étude comparative sur la prédiction des métastases à distance après chirurgie du cancer du poumon basée sur des modèles d’apprentissage automatique
Pourquoi il est important de prédire la diffusion du cancer
Le cancer du poumon reste l’un des cancers les plus mortels, même lorsque les chirurgiens retirent toutes les tumeurs visibles. Beaucoup de patients développent par la suite des foyers tumoraux cachés qui apparaissent au cerveau, aux os, au foie ou dans d’autres organes. Les médecins aimeraient savoir, peu de temps après l’intervention, quels patients sont plus susceptibles de présenter ce type de dissémination afin d’adapter les visites de suivi et les traitements. Cette étude examine si des programmes informatiques modernes, appelés modèles d’apprentissage automatique, peuvent aider à prévoir qui présente un risque accru, en s’appuyant sur des informations que les hôpitaux collectent déjà dans les soins courants.
Analyse approfondie de nombreux patients
Les chercheurs ont examiné les dossiers de 3 120 personnes atteintes d’un cancer du poumon de stade I à III ayant subi l’ablation de leur tumeur dans un centre anticancéreux unique en Chine. Tous avaient au moins deux ans de suivi. Pour chaque patient, l’équipe a rassemblé 52 types d’informations, notamment l’âge, le sexe, le poids corporel, les antécédents tabagiques, les résultats d’imagerie, les détails de l’intervention, les analyses de laboratoire et la réalisation éventuelle de traitements complémentaires comme la chimiothérapie ou la radiothérapie après la chirurgie. Au fil du temps, 596 de ces patients ont développé des métastases à distance, tandis que 2 524 n’en ont pas eu. Cette mixité issue du monde réel a permis à l’équipe d’identifier quelles caractéristiques étaient liées à la dissémination future.
Apprendre aux ordinateurs à reconnaître des profils de risque
Plutôt que de se fier à une seule formule, les scientifiques ont comparé neuf méthodes d’apprentissage automatique différentes, depuis des arbres de décision simples jusqu’à des techniques plus avancées combinant de nombreux petits modèles. Ils ont d’abord utilisé un filtre mathématique pour réduire les 52 facteurs initiaux à un ensemble plus restreint et plus informatif. Ensuite, en plusieurs itérations, ils ont entraîné chaque modèle sur une partie des données et l’ont testé sur des patients qu’il n’avait jamais « vus » auparavant. Parce qu’environ un patient sur cinq seulement a développé une métastase, ils ont ajusté l’entraînement pour que l’ordinateur ne se contente pas de prédire « faible risque » pour tout le monde. Ils ont évalué les performances à l’aide de plusieurs mesures, notamment la capacité des modèles à distinguer les patients à haut risque de ceux à faible risque et la concordance entre les risques prédits et les événements observés.
Identifier le modèle le plus fiable
Parmi les neuf approches, une appelée Gradient Boosting Decision Tree (GBDT) s’est démarquée. Sur les données de test, elle a correctement classé les patients avec une précision globale d’environ 77 %, et son score synthétique de discrimination (l’aire sous la courbe ROC) était de 0,81, ce qui est considéré comme solide pour des outils de prédiction médicale. Le modèle était particulièrement performant pour identifier les patients qui resteraient indemnes de métastases (forte « valeur prédictive négative »), ce qui signifie qu’un résultat faible risque était généralement rassurant. Lorsque l’équipe a examiné le comportement du modèle sur de nombreuses divisions aléatoires des données, ses performances sont restées stables, ce qui suggère qu’il n’apprenait pas simplement des particularités d’un sous‑ensemble donné.
Ce qui guide les décisions du modèle
Une critique fréquente de l’apprentissage automatique est qu’il peut constituer une « boîte noire ». Pour y remédier, les auteurs ont utilisé une méthode d’explication appelée SHAP, qui attribue à chaque facteur une contribution à l’estimation finale du risque pour chaque patient. Cette analyse a montré que les signaux les plus forts étaient la réalisation d’une chimiothérapie ou d’une radiothérapie après la chirurgie, le nombre de ganglions lymphatiques envahis par le cancer, l’âge, l’indice de masse corporelle (IMC) et le taux de neutrophiles préopératoire, un type de globule blanc. Les patients présentant une implication ganglionnaire plus avancée et des signes d’inflammation systémique avaient tendance à voir leur risque prédictif augmenter. Les auteurs soulignent que les fortes contributions liées à la chimiothérapie et à la radiothérapie ne signifient pas que ces traitements provoquent des métastases ; elles reflètent plutôt le fait que les médecins avaient déjà estimé la maladie comme plus agressive, de sorte que ces patients partaient d’un risque plus élevé.
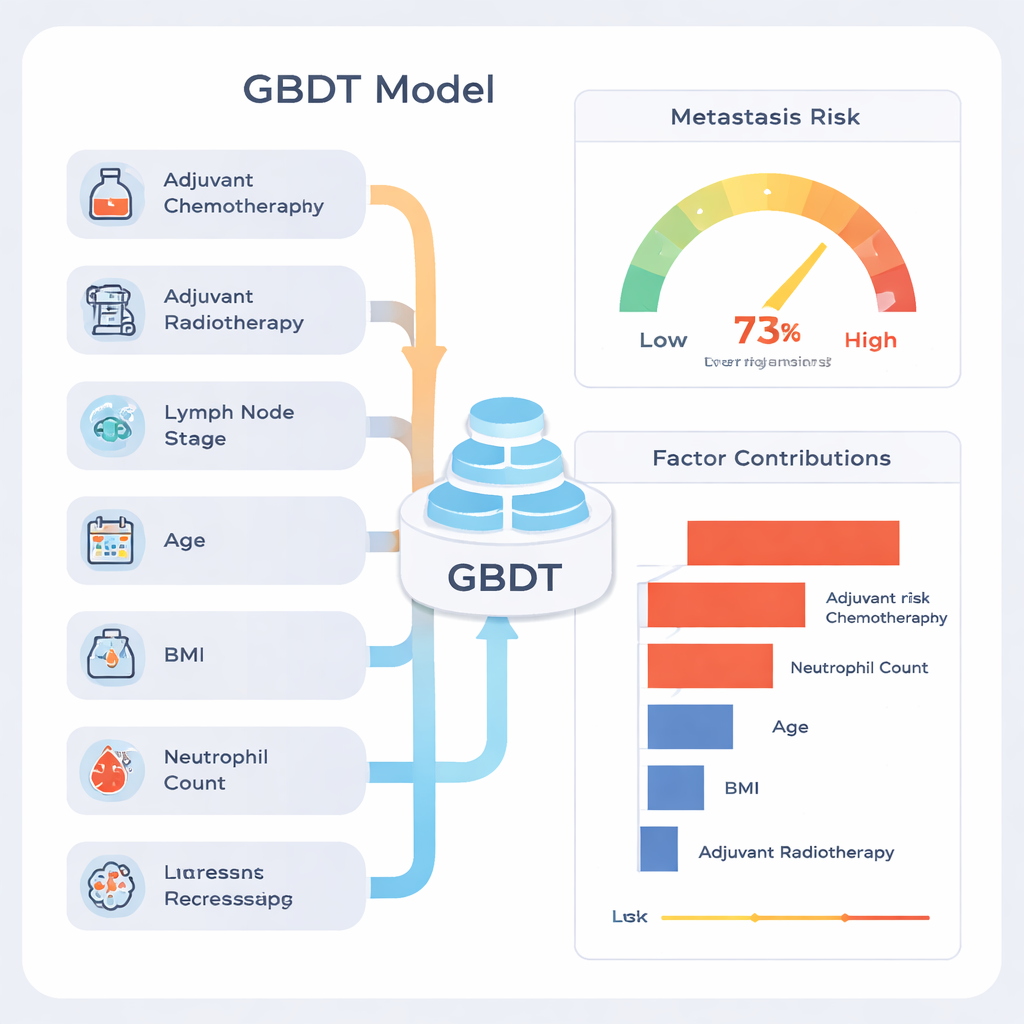
Comment cela pourrait aider les patients en pratique
Parce que le modèle utilise des informations que la plupart des centres anticancéreux consignent déjà, il pourrait, après des validations complémentaires, être intégré aux logiciels hospitaliers. Pour un nouveau patient ayant subi une chirurgie pulmonaire, le système pourrait récupérer ses données et fournir une probabilité personnalisée de métastase à distance, accompagnée d’une explication simple des facteurs qui augmentent ou diminuent le risque. Les cliniciens pourraient alors s’en servir pour décider qui mérite un suivi d’imagerie plus rapproché, un accompagnement renforcé ou une inclusion dans des essais cliniques, et qui pourrait éviter une surveillance intensive en toute sécurité. L’étude a été réalisée dans un seul hôpital, donc l’outil doit encore être vérifié et affiné dans d’autres régions et systèmes de santé. Mais il offre une feuille de route prometteuse pour combiner des données cliniques de routine avec un apprentissage automatique transparent afin d’améliorer les soins à long terme des personnes atteintes d’un cancer du poumon.
Citation: Guo, X., Xu, T., Luo, Y. et al. Comparative study on predicting postoperative distant metastasis of lung cancer based on machine learning models. Sci Rep 16, 6468 (2026). https://doi.org/10.1038/s41598-026-37113-w
Mots-clés: cancer du poumon, métastases à distance, apprentissage automatique, prévision du risque, suivi postopératoire