Clear Sky Science · fr
Les LncRNAs associés à la sénescence TRMP et TRMP-S favorisent le cancer gastrique en activant IGFL4
Pourquoi cette recherche est importante
Le cancer de l’estomac (gastrique) reste l’un des cancers les plus meurtriers dans le monde, principalement parce qu’il est souvent diagnostiqué tard et peut être difficile à traiter. Cette étude révèle comment deux molécules génétiques peu connues, appelées TRMP et TRMP-S, aident les tumeurs gastriques à croître et à se disséminer. En exposant la chaîne d’événements qu’elles déclenchent à l’intérieur des cellules cancéreuses et dans le microenvironnement immunitaire tumoral, ce travail ouvre des pistes pour diagnostiquer les patients plus tôt et concevoir des traitements ciblés plus efficaces.
Messages cachés dans notre ADN
La plupart des gens pensent aux gènes comme à des plans pour fabriquer des protéines, mais notre ADN produit aussi des longs ARN non codants (lncRNAs) qui ne traduisent pas de protéines et influencent néanmoins fortement le comportement cellulaire. TRMP et son variant d’épissage plus court TRMP-S sont deux de ces lncRNAs. Ils avaient été associés auparavant au vieillissement et au contrôle du cycle cellulaire dans des cellules pulmonaires et coliques, mais leur rôle dans le cancer gastrique était inconnu. Comme les lncRNAs peuvent servir de marqueurs diagnostiques et de cibles thérapeutiques, les auteurs ont cherché à déterminer si TRMP et TRMP-S favorisent la transformation des cellules gastriques en cellules cancéreuses et comment ils interagissent avec d’autres molécules pour le faire.
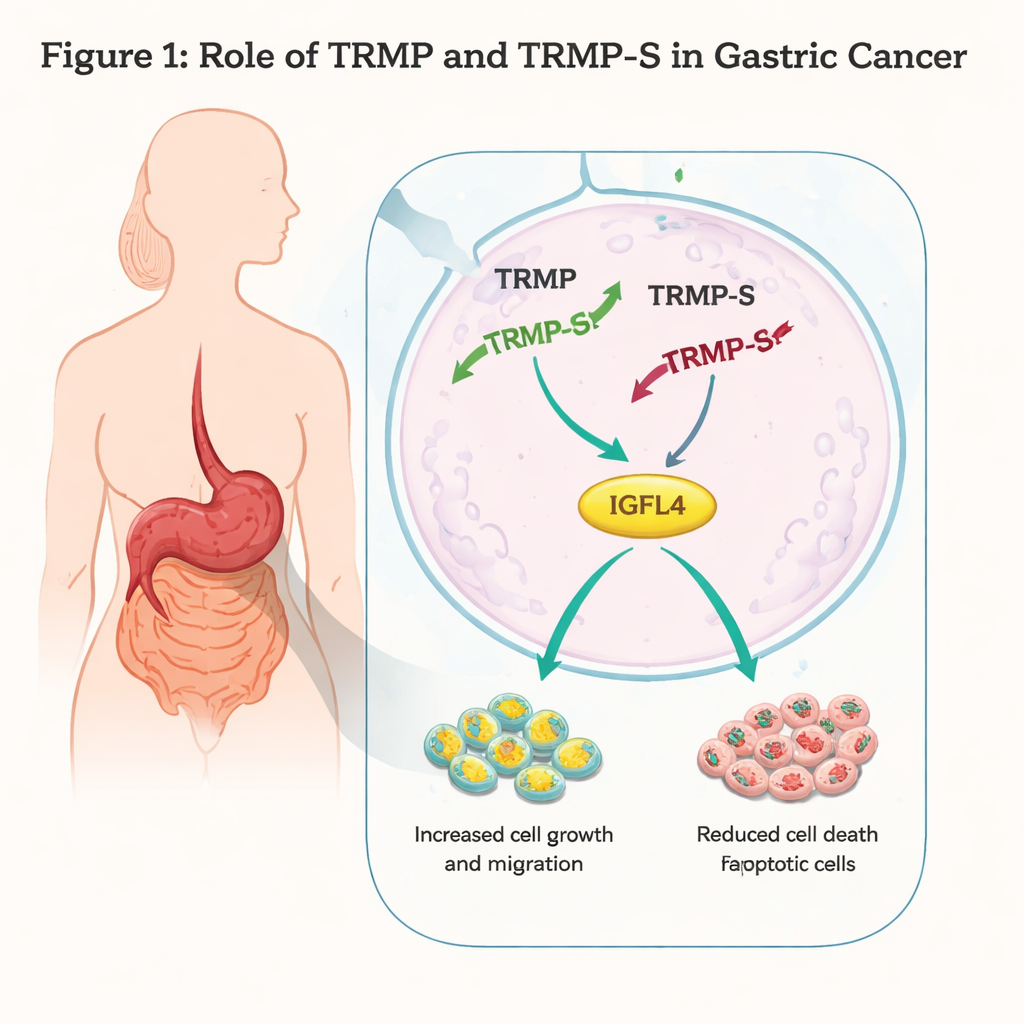
Couper l’accélérateur du cancer
Les chercheurs ont travaillé sur deux lignées cellulaires humaines de cancer gastrique, AGS et MKN45, et ont utilisé des outils génétiques pour réduire les niveaux de TRMP-S et TRMP. Lorsque TRMP-S a été supprimé, les cellules cancéreuses ont proliféré plus lentement, formé moins de colonies et montré une moindre capacité à migrer à travers des barrières artificielles ou à refermer des plaies en culture. La cytométrie en flux et les analyses protéiques ont montré un accroissement de l’apoptose (mort cellulaire programmée) et un arrêt du cycle cellulaire en phase G1, un « point de contrôle » clé avant la réplication de l’ADN. Les niveaux de p73, membre de la famille des suppresseurs tumoraux p53, ont augmenté en l’absence de TRMP-S, ce qui concorde avec un renforcement du contrôle du cycle et une augmentation de la mort cellulaire. Pris ensemble, ces résultats indiquent que TRMP-S agit normalement comme un accélérateur pour les cellules du cancer gastrique.
Un partenaire clé : le signal IGFL4
Pour comprendre comment TRMP et TRMP-S exercent leurs effets, l’équipe a exploité de larges jeux de données de patients issus du Cancer Genome Atlas et d’une cohorte coréenne de cancer gastrique. Ils ont recherché des gènes à la fois surexprimés dans les tumeurs et corrélés positivement aux niveaux de TRMP, puis ont construit un « modèle de risque » à six gènes qui prédisaient la survie des patients — des scores plus élevés étant associés à de moins bons pronostics. Parmi ces gènes, un s’est distingué : IGFL4, membre d’une famille voisine des facteurs de croissance de type insuline, connus pour stimuler la croissance et la survie dans de nombreux cancers. Dans les cellules de cancer gastrique, l’inhibition de TRMP-S a fortement réduit les niveaux d’ARN et de protéine d’IGFL4, tandis qu’un test d’immunoprécipitation d’ARN a montré que TRMP et TRMP-S se lient physiquement à la protéine IGFL4. La réduction directe de TRMP avait le même effet atténuateur sur IGFL4, suggérant que ces lncRNAs contribuent à stabiliser ou à favoriser la production de ce signal pro-croissance.
Ralentir la dissémination et remodeler la scène immunitaire
Lorsque les chercheurs ont utilisé des petits ARN interférents pour éteindre IGFL4 lui-même, les cellules de cancer gastrique ont ralenti leur croissance, migré moins, et montré une capacité réduite à envahir des membranes et à refermer des plaies. L’analyse des données tumorales de patients a révélé que les niveaux d’IGFL4 étaient significativement plus élevés dans les tumeurs gastriques que dans le tissu gastrique normal, et augmentés dans de nombreux autres types de cancers. Fait important, les tumeurs à expression élevée d’IGFL4 présentaient des profils distincts d’infiltration immunitaire : plus de macrophages indifférenciés (M0) et moins de cellules plasmatiques, de monocytes, d’éosinophiles et de neutrophiles. Des scores immunitaires computationnels ont suggéré que les tumeurs à fort IGFL4 pourraient mieux répondre aux immunothérapies modernes ciblant les points de contrôle immunitaires, indiquant qu’IGFL4 pourrait aider à identifier les patients susceptibles de bénéficier de ces traitements.
Un petit ARN qui freine
L’étude a aussi mis au jour une contrepartie à cette voie pro-tumorale. En corrélant l’expression des microARN et des gènes chez les patients, les auteurs ont identifié miR-129-5p comme un petit ARN corrélé négativement à la fois à TRMP et à IGFL4. Dans les cellules de cancer gastrique, l’ajout de miR-129-5p a réduit les niveaux d’IGFL4 et ralenti la croissance, tandis que le blocage de miR-129-5p a augmenté IGFL4 et accéléré la prolifération. Un autre microARN candidat, miR-4739, n’a pas affecté mesurablement IGFL4 et a été écarté. Ces résultats étayent l’existence d’une chaîne de régulation dans laquelle TRMP et TRMP-S, miR-129-5p et IGFL4 forment un réseau qui ajuste la vigueur de la croissance des cellules de cancer gastrique et leurs interactions avec leur environnement.
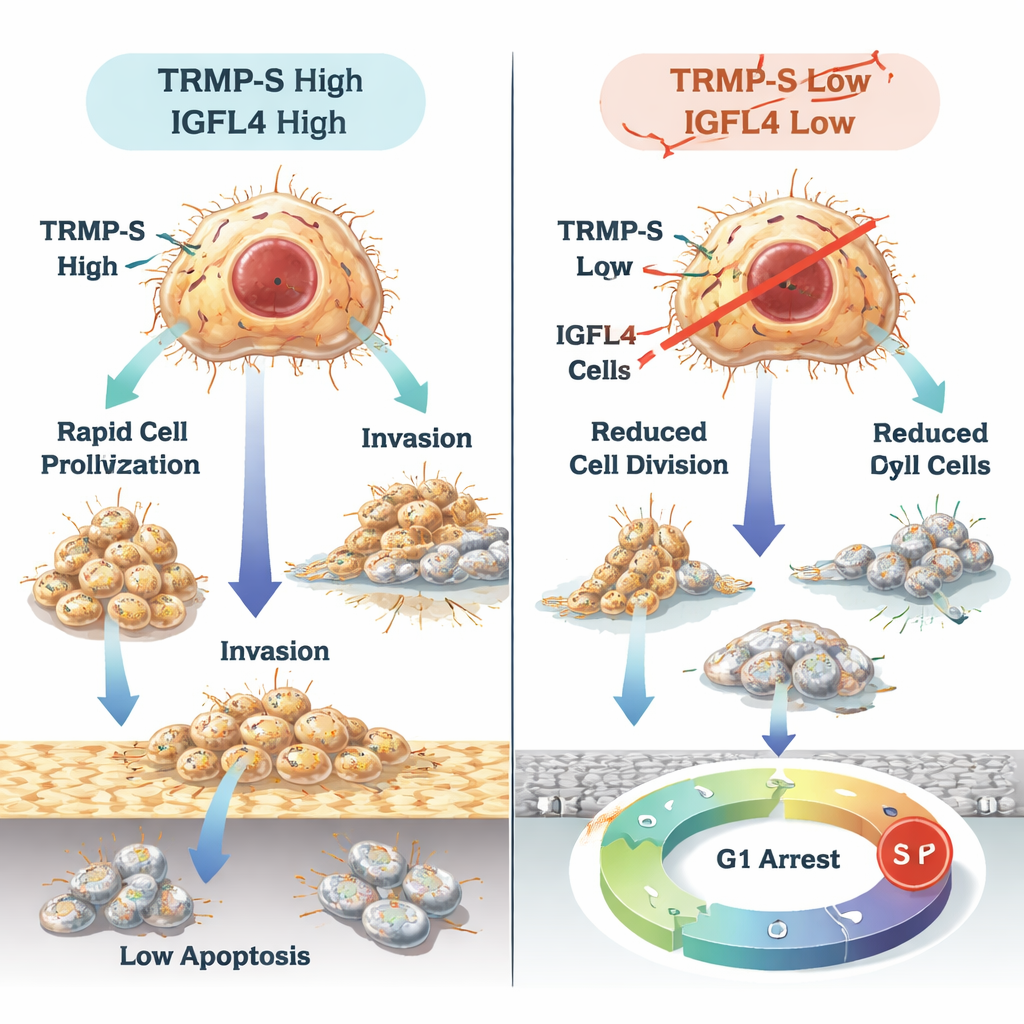
Ce que cela pourrait signifier pour les patients
En termes simples, ce travail montre que TRMP et TRMP-S agissent comme des chefs d’orchestre en coulisse qui activent IGFL4 et aident les cellules du cancer gastrique à croître, se disséminer et échapper aux mécanismes naturels d’arrêt. Parallèlement, le petit ARN miR-129-5p joue le rôle de frein sur IGFL4, et IGFL4 contribue à façonner la manière dont les cellules immunitaires s’agrègent autour des tumeurs et l’efficacité potentielle des thérapies qui réveillent le système immunitaire. Bien que des études supplémentaires et des essais cliniques soient nécessaires, TRMP, TRMP-S, IGFL4 et miR-129-5p constituent ensemble un ensemble prometteur de marqueurs pronostiques et de cibles potentielles pour des médicaments visant à ralentir ou arrêter le cancer gastrique.
Citation: Zhang, M., Mi, Y., Li, F. et al. Senescence-associated LncRNAs TRMP and TRMP-S promote gastric cancer by activating IGFL4. Sci Rep 16, 6740 (2026). https://doi.org/10.1038/s41598-026-37106-9
Mots-clés: cancer gastrique, ARN non codant long, TRMP, IGFL4, microenvironnement tumoral