Clear Sky Science · fr
Identification de RBX1 comme régulateur de la transcription de LIPT1 et son rôle dans la mort cellulaire induite par le cuivre dans les cellules de GBM
Pourquoi le cuivre et les tumeurs cérébrales comptent
Le glioblastome multiforme est l’une des formes de cancer du cerveau les plus mortelles, la majorité des patients survivant peu de temps après le diagnostic malgré des interventions chirurgicales, une radiothérapie et une chimiothérapie agressives. Cette étude explore un allié inattendu contre ces tumeurs : le métal cuivre. Les chercheurs examinent une forme récemment reconnue de mort cellulaire déclenchée par le cuivre et identifient une voie moléculaire qui pourrait aider les cliniciens à exploiter ce processus pour affaiblir les tumeurs et potentiellement renforcer l’attaque du système immunitaire contre les cellules cancéreuses.
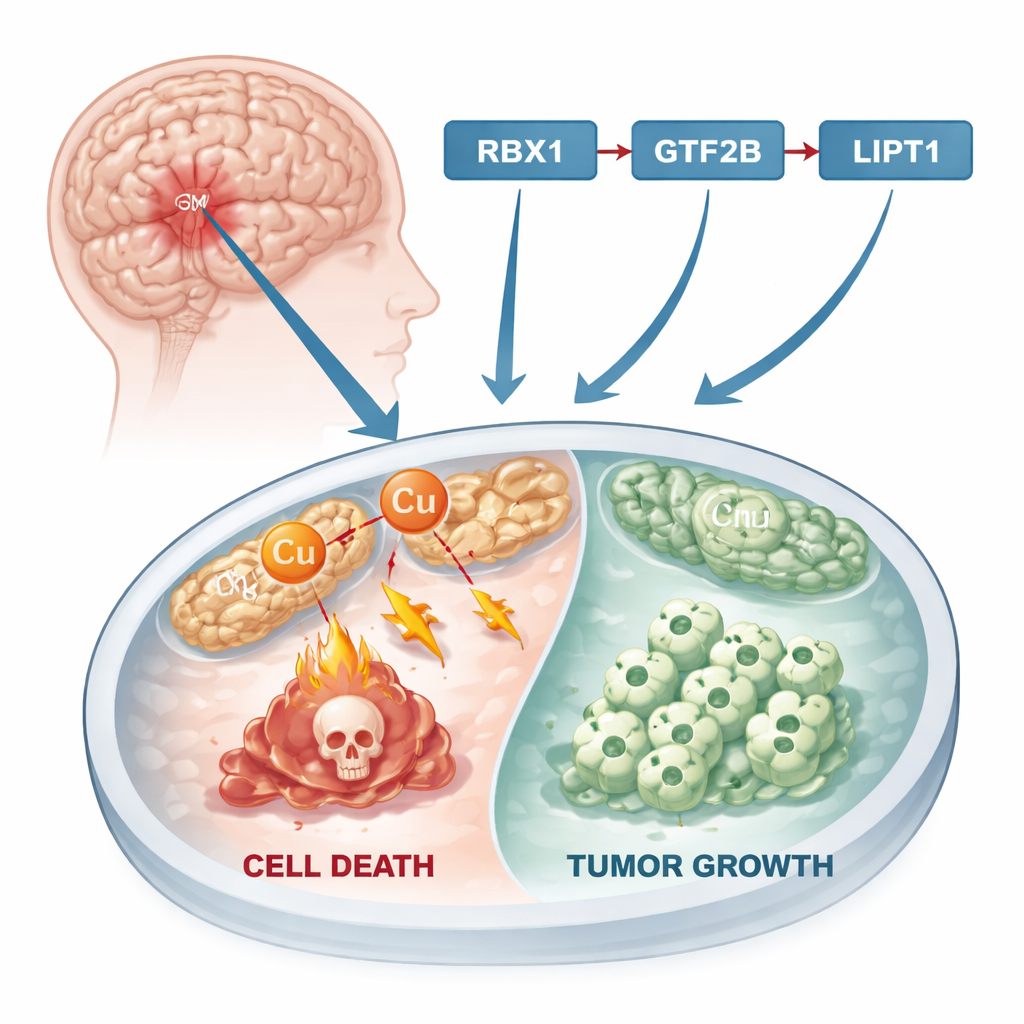
Une nouvelle voie de mort cellulaire
Pendant des décennies, la recherche sur le cancer s’est concentrée sur des formes familières de mort cellulaire comme l’apoptose, où les cellules endommagées s’éteignent discrètement. Récemment, les scientifiques ont découvert une voie différente appelée mort cellulaire induite par le cuivre, ou « cuproptose ». Dans ce processus, un excès de cuivre s’accumule à l’intérieur des centrales énergétiques de la cellule, les mitochondries. Là, il perturbe des protéines clés, provoquant la formation d’agrégats toxiques qui finissent par tuer la cellule. Parce que de nombreuses tumeurs présentent un métabolisme des métaux altéré et des taux de cuivre plus élevés que les tissus normaux, la cuproptose représente un point d’appui potentiel : si les chercheurs parviennent à pousser les cellules tumorales vers cette issue induite par le cuivre, ils pourraient ralentir ou arrêter la croissance cancéreuse.
Mise en lumière d’un gène clé dans le glioblastome
Les auteurs ont commencé par examiner un groupe de gènes déjà connus pour être impliqués dans la cuproptose et ont comparé leur comportement dans des échantillons de glioblastome versus du tissu cérébral normal. Un gène en particulier, nommé LIPT1, s’est démarqué. Il était plus actif dans les tissus de glioblastome et dans plusieurs lignées cellulaires de glioblastome que dans les cellules cérébrales normales. Fait important, les patients dont les tumeurs présentaient une activité élevée de LIPT1 avaient tendance à rester plus longtemps sans récidive après le traitement. Des niveaux élevés de LIPT1 s’associaient également à une plus grande présence de cellules T CD8, les effecteurs du système immunitaire contre le cancer, ce qui suggère que ce gène pourrait aider à rendre le microenvironnement tumoral plus vulnérable à l’attaque immunitaire.
Que se passe-t-il lorsque l’interrupteur de la mort par le cuivre est atténué
Pour tester si LIPT1 influence réellement la mort induite par le cuivre, l’équipe a exposé des cellules de glioblastome à une combinaison médicamenteuse transportant du cuivre qui déclenche de manière fiable la cuproptose. Ils ont ensuite utilisé des outils génétiques pour réduire les niveaux de LIPT1. Lorsque LIPT1 était supprimé, les cellules tumorales devenaient plus résistantes à la mort induite par le cuivre, survivaient mieux et montraient une plus grande capacité de migration et d’invasion — des comportements associés à une agressivité accrue du cancer. Dans des cultures mixtes de cellules tumorales et de cellules T CD8 humaines, l’abaissement de LIPT1 réduisait aussi la libération de médiateurs immunitaires et rendait les cellules cancéreuses plus difficiles à éliminer par les lymphocytes T. Ensemble, ces expériences indiquent que LIPT1 augmente la sensibilité à la mort induite par le cuivre et soutient l’activité immunitaire anti-tumorale.
Remonter la chaîne de commandement jusqu’à RBX1
Le défi suivant était de comprendre pourquoi LIPT1 est surexprimé dans le glioblastome. En combinant plusieurs grandes bases de données génomiques et protéiques, les chercheurs ont identifié un facteur de transcription — une sorte d’interrupteur maître de l’activité génique — appelé GTF2B, qui se lie à proximité du gène LIPT1 et stimule vraisemblablement son expression. Ils se sont ensuite demandé ce qui contrôle GTF2B lui-même. Une seconde protéine, RBX1, est apparue comme un candidat fort. RBX1 fait partie du système cellulaire d’étiquetage et d’élimination qui marque d’autres protéines pour leur dégradation. Dans les cellules de glioblastome, les niveaux de RBX1 étaient plus faibles que dans les cellules cérébrales normales, tandis que GTF2B et LIPT1 étaient plus élevés. Des essais en laboratoire ont montré que RBX1 peut attacher de petites étiquettes « détruis-moi » à GTF2B, entraînant sa dégradation ; lorsque RBX1 était augmenté, les niveaux de GTF2B et l’activité de LIPT1 diminuaient, et le blocage du système de dégradation cellulaire inversait cet effet.
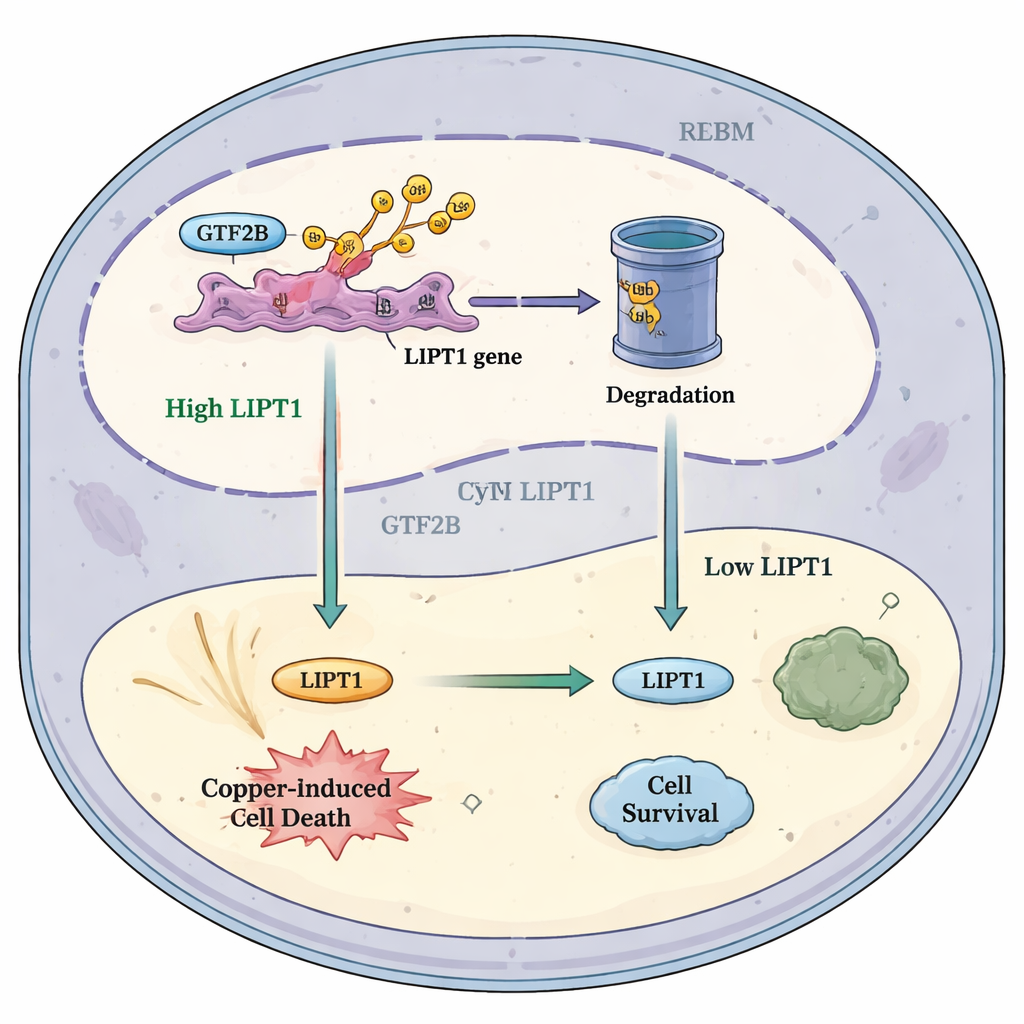
Comment cette voie pourrait aider les traitements futurs
En réunissant ces éléments, les auteurs proposent un modèle simple : dans des conditions saines, RBX1 maintient GTF2B sous contrôle, limitant son activation du gène LIPT1. Dans le glioblastome, la réduction de RBX1 entraîne moins de dégradation de GTF2B. L’excès de GTF2B stimule alors LIPT1, augmentant la sensibilité des cellules tumorales à la mort induite par le cuivre et attirant davantage de cellules immunitaires anti-cancer. Ce modèle suggère qu’ajuster soigneusement cette voie RBX1–GTF2B–LIPT1, éventuellement en combinaison avec des médicaments ciblant le cuivre et des immunothérapies, pourrait faire pencher la balance dans les tumeurs cérébrales en faveur de l’autodestruction. Bien qu’il reste beaucoup de travail avant que cette idée n’atteigne les patients, l’étude met en évidence une intersection prometteuse entre la biologie des métaux, la régulation génique et l’immunologie du cancer, susceptible d’ouvrir de nouvelles voies thérapeutiques pour l’un des cancers les plus tenaces.
Citation: Zeng, J., Liu, J., Hua, S. et al. Identification of RBX1 as a regulator of LIPT1 transcription and its role in copper-induced cell death in GBM cells. Sci Rep 16, 6837 (2026). https://doi.org/10.1038/s41598-026-37105-w
Mots-clés: glioblastome, mort cellulaire induite par le cuivre, LIPT1, immunologie tumorale, voie RBX1