Clear Sky Science · fr
Interféron-λ3 sérique comme biomarqueur à court terme du contrôle de la maladie dans la maladie interstitielle pulmonaire associée à la dermatomyosite anti‑MDA5
Pourquoi cela importe pour les patients et leurs familles
Certaines personnes atteintes d’une maladie rare de la peau et des muscles appelée dermatomyosite développent des cicatrices et une inflammation graves des poumons. Ce problème pulmonaire peut s’aggraver rapidement et devenir potentiellement mortel, si bien que les médecins ont besoin d’un moyen rapide et fiable pour savoir si le traitement précoce fonctionne réellement. Cette étude a exploré si une substance présente dans le sang, appelée interféron‑λ3, peut servir de témoin précoce, aidant les médecins à distinguer — en à peine un mois — qui évolue favorablement et qui reste en danger.
Une maladie rare avec une atteinte pulmonaire dangereuse
La dermatomyosite est une maladie auto-immune : les défenses de l’organisme attaquent par erreur les muscles, la peau et parfois les poumons. Un sous-groupe de patients porte des anticorps dirigés contre une protéine connue sous le nom de MDA5 et est particulièrement susceptible de développer une maladie pulmonaire interstitielle, dans laquelle le tissu pulmonaire devient enflammé et raide. Pour ces patients, les premières semaines après le diagnostic sont critiques. Des médicaments immunosuppresseurs puissants sont initiés rapidement, mais il peut être difficile de savoir tôt si ces traitements calment réellement l’inflammation pulmonaire ou si la maladie progresse silencieusement.
À la recherche d’un signal sanguin à court terme
Les chercheurs se sont concentrés sur une molécule appelée interféron‑λ3 (IFN‑λ3), partie du système de défense antiviral de l’organisme qui influence aussi l’inflammation au niveau des barrières telles que les poumons. Des travaux antérieurs montraient que les taux d’IFN‑λ3 sont anormalement élevés chez les personnes atteintes de dermatomyosite MDA5‑positive et que des taux élevés au diagnostic sont associés à de moins bons résultats. Dans cette étude, l’équipe a posé une nouvelle question : les variations d’IFN‑λ3 au cours du premier mois de traitement reflètent-elles le contrôle de la maladie pulmonaire ? Pour répondre, ils ont réexaminé 24 patients traités dans plusieurs hôpitaux sur plus de deux décennies, tous disposant d’échantillons sanguins conservés au moment du diagnostic puis environ un mois après le début de la thérapie.
Deux trajectoires : bon contrôle et mauvais contrôle
Les patients ont été répartis en deux groupes selon l’évolution de leur maladie pulmonaire durant l’année suivante. Le groupe « bon contrôle » comprenait des personnes qui ont survécu et n’ont présenté aucune poussée pulmonaire pendant au moins douze mois. Le groupe « mauvais contrôle » comprenait ceux qui sont décédés d’une aggravation pulmonaire ou qui ont eu une rechute nette dans l’année. Au moment du diagnostic, les taux d’IFN‑λ3 étaient généralement élevés dans les deux groupes. Mais au bout d’un mois, une nette divergence est apparue. Dans le groupe à bon contrôle, la médiane d’IFN‑λ3 est passée d’environ 95 à 13 unités, une chute rapide et marquée. Dans le groupe à mauvais contrôle, les niveaux ont à peine varié, restant élevés — autour de 130 à 119. Même les patients de ce groupe qui ont montré une certaine diminution présentaient des taux clairement élevés après un mois.
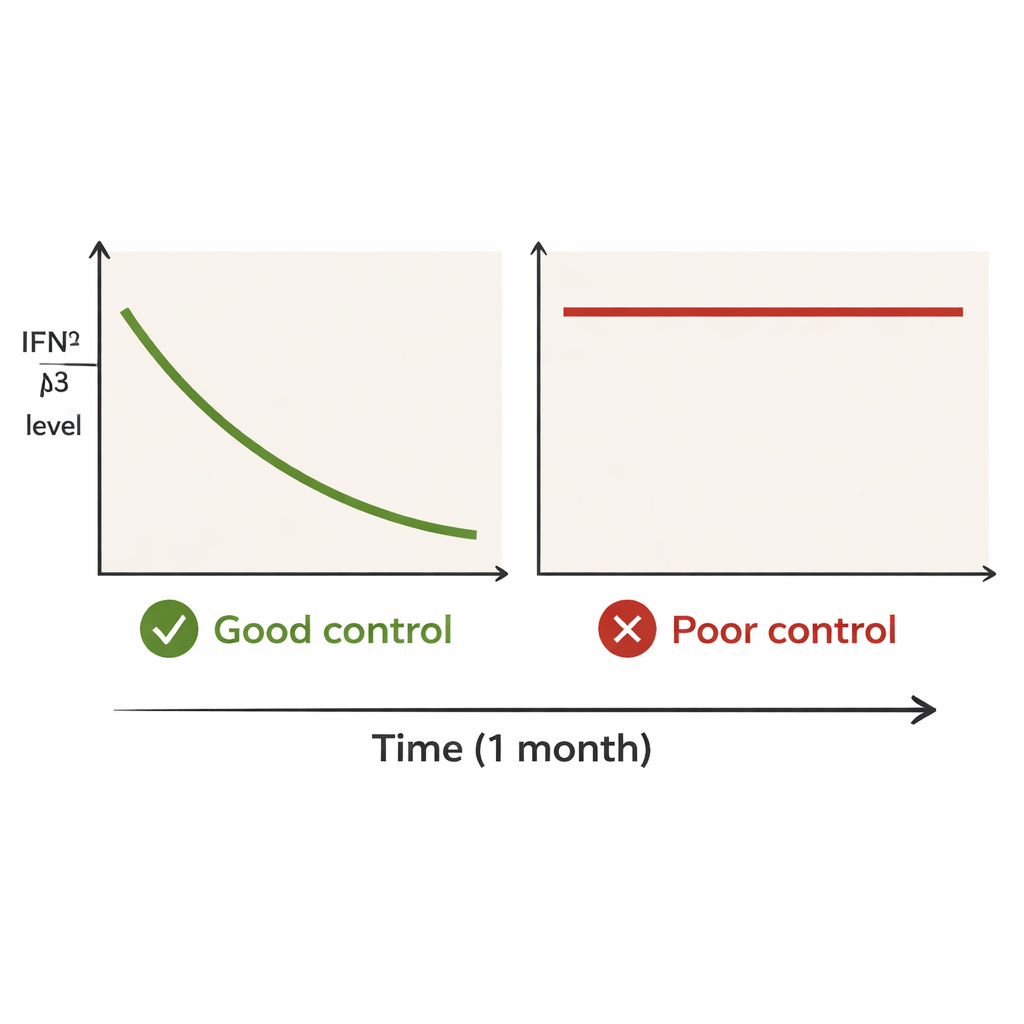
Comment ce marqueur se compare aux autres
Les médecins utilisent déjà d’autres tests sanguins, comme la ferritine et le KL‑6, pour aider à estimer la gravité de ce type de maladie pulmonaire. Cependant, dans cette étude, ces marqueurs ont à peine changé au cours du premier mois et n’ont pas clairement distingué les deux groupes de résultats. L’IFN‑λ3 s’est comporté différemment : il a chuté rapidement chez les patients dont la maladie a été contrôlée et est resté élevé chez ceux qui sont ensuite décédés ou ont rechuté. Cela suggère que le niveau absolu d’IFN‑λ3 à un mois — son amplitude à ce moment précis — peut être plus informatif que la simple variation relative par rapport au niveau de départ. Fait important, ce schéma a persisté même si nombre des patients les plus graves avaient reçu des associations médicamenteuses plus agressives.
Ce que cela pourrait signifier pour la prise en charge
L’étude est relativement petite et rétrospective, ses résultats doivent donc être confirmés par des études prospectives plus larges. Néanmoins, les résultats pointent vers une utilisation pratique : mesurer l’IFN‑λ3 au diagnostic puis environ un mois plus tard pourrait fournir aux médecins une lecture précoce sur l’efficacité du traitement en cours. Si les taux restent élevés, cela pourrait entraîner une surveillance plus étroite, un ajustement des médicaments ou la considération de traitements complémentaires avant que des lésions pulmonaires irréversibles ne surviennent. Pour les patients et leurs familles, un simple test sanguin reflétant le contrôle de la maladie à court terme pourrait offrir des indications plus claires et une meilleure chance de prévenir une complication pulmonaire dangereuse.
Citation: Kitahara, Y., Fujisawa, T., Fukada, A. et al. Serum interferon-λ3 as a short-term biomarker of disease control in anti-MDA5-positive dermatomyositis-associated ILD. Sci Rep 16, 6134 (2026). https://doi.org/10.1038/s41598-026-37104-x
Mots-clés: dermatomyosite, maladie pulmonaire interstitielle, biomarqueurs, interféron lambda 3, maladie pulmonaire auto-immune