Clear Sky Science · fr
Intégrer l’apprentissage automatique et la modélisation physique pour la conception prédictive de nanocomposites chargés en gemcitabine
Des médicaments anticancéreux plus intelligents par conception
Des médicaments anticancéreux comme la gemcitabine peuvent sauver des vies, mais ils se comportent souvent davantage comme des outils grossiers que comme des instruments de précision : ils se dégradent rapidement, manquent leur cible et provoquent des effets secondaires sévères. Cette étude explore comment les ordinateurs peuvent aider les scientifiques à « pré-tester » de nouveaux vecteurs médicamenteux microscopiques à l’écran, plutôt que uniquement en laboratoire, afin de rendre les traitements à la gemcitabine plus efficaces, plus durables et potentiellement plus sûrs pour les patients.
Pourquoi les vecteurs microscopiques sont importants
La chimiothérapie traditionnelle inonde le corps de molécules médicamenteuses qui circulent partout, pas seulement dans les tumeurs. Les nanocomposites — particules conçues des milliers de fois plus petites qu’un grain de sable — offrent un moyen d’enfermer la gemcitabine pour qu’elle soit protégée dans le flux sanguin et délivrée plus directement aux cellules cancéreuses. Deux chiffres déterminent en grande partie l’utilité d’un design. L’efficacité de chargement indique la quantité de médicament contenue dans chaque particule, tandis que l’efficacité d’encapsulation mesure la fraction du médicament initial qui est effectivement piégée plutôt que perdue. Des valeurs élevées pour les deux signifient moins d’injections, moins de matrice porteuse et une meilleure chance d’atteindre la tumeur sans submerger le reste du corps.
Du tâtonnement à la conception guidée par les données
Concevoir ces nanovecteurs à la main revient à essayer de régler une radio avec des centaines de boutons — la taille des particules, la charge de surface, les matériaux, les revêtements et les méthodes de préparation interagissent tous de manière complexe. Jusqu’ici, les chercheurs changeaient surtout un ou deux paramètres à la fois et mesuraient le résultat, un cycle lent et coûteux qui ne révèle qu’une petite tranche du tableau complet. Dans ce travail, les auteurs ont rassemblé 59 recettes de nanovecteurs à la gemcitabine soigneusement vérifiées dans la littérature scientifique et les ont enrichies par des exemples supplémentaires, basés sur la physique, générés par ordinateur. Cet ensemble de données combiné leur a permis de tester plusieurs approches d’apprentissage automatique — des programmes informatiques qui apprennent des motifs dans les données — pour prédire les efficacités de chargement et d’encapsulation à partir des choix de conception seuls.
Laisser la physique orienter les algorithmes
La plupart des systèmes d’apprentissage automatique sont de puissants ajusteurs de courbes : ils repèrent des motifs mais ne savent pas quand une réponse viole les lois de la nature. Pour éviter des prédictions irréalistes, les chercheurs ont construit une méthode hybride qui mêle les données à des règles physiques de base sur la façon dont les molécules médicamenteuses se déplacent, se lient et s’équilibrent dans un système clos. Dans leur cadre, toute prédiction qui impliquerait, par exemple, la création de plus de médicament que ce qui avait été initialement ajouté, ou l’ignorance de la diffusion des molécules à travers un matériau, est légèrement pénalisée pendant l’entraînement. Cette approche « informée par la physique » oriente le modèle vers des réponses qui ont du sens chimique et physique, en particulier dans les régions de l’espace de conception où les mesures expérimentales sont rares.
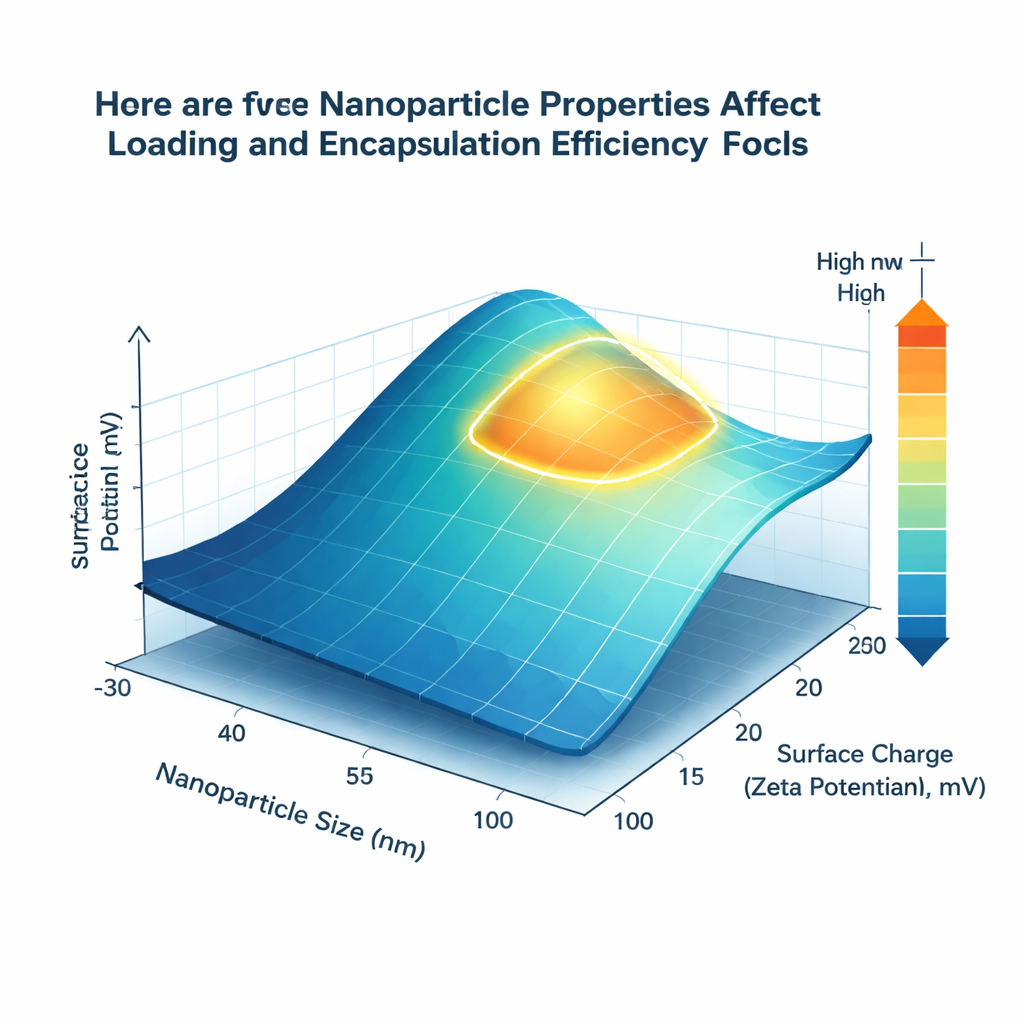
Ce que les modèles ont révélé
Parmi les techniques testées, un algorithme d’ensemble avancé appelé XGBoost a fourni les prévisions les plus précises, correspondant étroitement aux résultats expérimentaux rapportés pour les deux efficacités clés. Mais au-delà de la précision, l’équipe cherchait des règles de conception compréhensibles. En utilisant une méthode appelée SHAP, qui classe l’importance de chaque facteur pour pousser la prédiction vers le haut ou vers le bas, ils ont trouvé que la taille des particules et la charge de surface dominent systématiquement les performances. Des nanovecteurs d’environ 80 à 150 nanomètres de diamètre offraient le meilleur compromis entre surface spécifique et volume interne, améliorant à la fois le chargement et l’encapsulation. Une charge de surface légèrement positive, dans la plage de +15 à +25 millivolts, était associée à une meilleure rétention de la gemcitabine, probablement parce que les surfaces des vecteurs chargées positivement interagissent favorablement avec les groupes chargés négativement du médicament.
Une carte numérique pour les traitements anticancéreux futurs
Le résultat final n’est pas un médicament abouti mais un outil de planification puissant. L’étude fournit une sorte de « carte de conception » qui oriente les chercheurs vers des recettes de nanovecteurs les plus susceptibles de contenir et protéger efficacement la gemcitabine, tout en évitant des millions de combinaisons peu prometteuses. Les auteurs insistent sur le fait que leurs prédictions doivent encore être confirmées par de nouvelles études en laboratoire et sur animaux, et que leur jeu de données — bien que soigneusement assemblé — reste modeste en taille. Néanmoins, ce cadre d’apprentissage automatique conscient de la physique montre comment les ordinateurs peuvent aider à restreindre la recherche de meilleurs vecteurs de médicaments anticancéreux, réduire les coûts et accélérer le passage des idées à des thérapies plus précises et mieux tolérées par les patients.
Citation: Rahdar, A., Fathi-karkan, S. & Shirzad, M. Integrating machine learning and physics-based modeling for predictive design of gemcitabine-loaded nanocomposites. Sci Rep 16, 6268 (2026). https://doi.org/10.1038/s41598-026-37098-6
Mots-clés: nanomédecine, gemcitabine, délivrance de médicaments, apprentissage automatique, nanoparticules