Clear Sky Science · fr
MCT1 en tant que régulateur critique du signal insulinique, de l’homéostasie énergétique et de la fonction des podocytes
Pourquoi les choix énergétiques des cellules rénales comptent
Nos reins filtrent silencieusement des centaines de litres de sang chaque jour, et une grande partie de ce travail repose sur de minuscules cellules appelées podocytes qui entourent les filtres rénaux. Ces cellules doivent sans cesse se remodeler pour retenir les protéines dans le sang et laisser les déchets partir dans l’urine. Cette étude explore comment les podocytes obtiennent l’énergie dont ils ont besoin, ce qui se passe lorsqu’une de leurs principales « portes à carburant » est bloquée, et pourquoi cela peut avoir des conséquences pour des affections courantes comme le diabète et les maladies rénales. 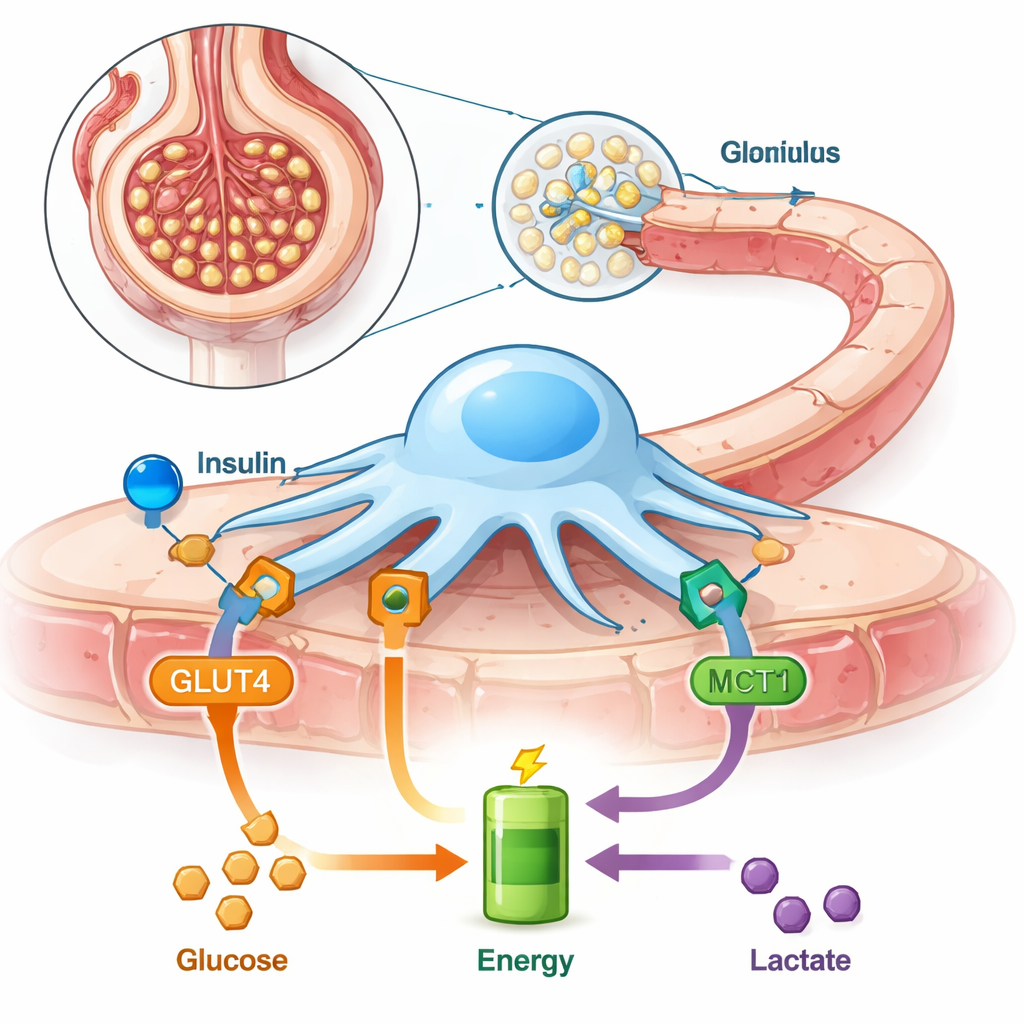
Les gardiens du filtre
Les podocytes se trouvent du côté externe de chaque filtre rénal, envoyant de délicates extensions en forme de pieds qui s’imbriquent pour former une barrière finale avant la production d’urine. Parce qu’ils s’ajustent constamment, ils consomment beaucoup d’énergie. Contrairement à de nombreuses autres cellules, les podocytes dépendent fortement de la dégradation du sucre sans oxygène (une voie appelée glycolyse) et ils sont particulièrement sensibles à l’insuline, qui leur indique d’importer davantage de glucose du sang via un transporteur appelé GLUT4. Les auteurs avaient montré précédemment que les podocytes peuvent aussi utiliser le lactate, une petite molécule souvent considérée comme un « déchet », ce qui suggère que ces cellules sont plus flexibles qu’on ne le pensait.
La porte du lactate : MCT1
Le lactate entre et sort des cellules via des protéines de transport spécialisées. L’un des plus importants est le transporteur de monocarboxylates 1 (MCT1), qui peut acheminer le lactate à l’intérieur des cellules pour y être utilisé comme carburant. Dans cette étude, les chercheurs ont utilisé des podocytes de rat cultivés en laboratoire et ont bloqué MCT1 avec un inhibiteur chimique. Ils ont ensuite examiné comment cela affectait la capacité de l’insuline à stimuler l’absorption du glucose, la quantité d’énergie que les cellules pouvaient produire, l’organisation de leur échafaudage interne, et la « fuite » du filtre vis‑à‑vis d’une grande protéine sanguine appelée albumine. Ils ont également testé des filtres rénaux entiers (glomérules isolés) pour voir comment le lactate et le blocage de MCT1 modifiaient la fuite de protéines dans un système plus intact.
Quand la porte du carburant se ferme
Le blocage de MCT1 a provoqué plusieurs effets marquants. D’abord, il a réduit la quantité de glucose absorbée par les podocytes, à la fois au repos et après stimulation par l’insuline, et a affaibli un interrupteur clé de la voie insulinique (une protéine appelée Akt) sans perturber le récepteur de l’insuline lui‑même. Parallèlement, le réarrangement habituel du transporteur GLUT4 vers la surface cellulaire a été atténué. Les mesures du métabolisme cellulaire ont montré que la production énergétique totale diminuait lorsque MCT1 était bloqué, et que les cellules se détournaient de la glycolyse au profit d’une combustion plus oxydative dans les mitochondries. Même lorsque de l’insuline ou du lactate étaient ajoutés, ce déficit énergétique n’était pas complètement corrigé, ce qui suggère que MCT1 est central pour l’équilibre des sources d’énergie des podocytes. 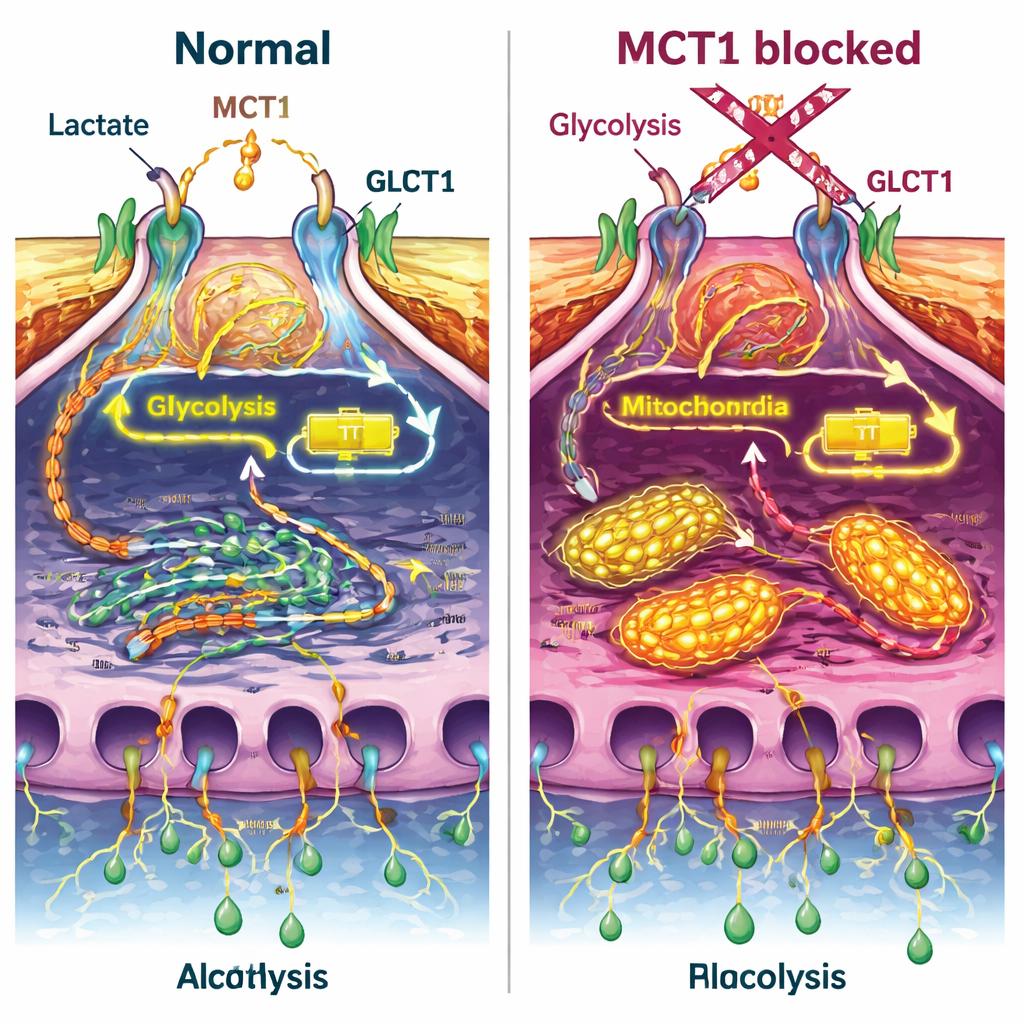
Filtres poreux et échafaudages stressés
Les modifications énergétiques étaient étroitement liées aux dommages physiques. Lorsque MCT1 était bloqué, les couches de podocytes en culture laissaient passer davantage d’albumine, un effet similaire à celui observé avec l’insuline seule. Le lactate lui‑même rendait aussi la barrière plus perméable, et la combinaison de lactate ou d’insuline avec le blocage de MCT1 maintenait une perméabilité élevée. À l’intérieur des cellules, les fibres d’actine qui forment leur structure devenaient plus agglomérées et désorganisées, un motif associé à la perte des fins processus pédiculaires qui composent le filtre. Une autre protéine clé, la néphrine, qui aide à maintenir l’intégrité du filtre et soutient aussi l’action de l’insuline, était réduite ou mal localisée lorsque MCT1 était inhibé. Dans des filtres entiers isolés de reins de rat, l’ajout de lactate augmentait rapidement la fuite d’albumine, et le blocage de MCT1 produisait une hausse similaire, appuyant l’idée qu’une perturbation du traitement du lactate affaiblit directement le filtre.
Implications pour le diabète et la santé rénale
Les auteurs proposent que le mouvement approprié du lactate via MCT1 est essentiel pour que les podocytes maintiennent leur programme énergétique de prédilection, répondent à l’insuline et conservent une barrière de filtration étanche. Lorsque cette « porte » au lactate est perturbée — par le blocage de MCT1 ou par une hyperglycémie chronique qui altère l’équilibre du lactate — les podocytes perdent leur flexibilité métabolique, consomment moins de glucose, reposent davantage sur les mitochondries, et deviennent structurellement instables et poreux. Pour les personnes, ce travail suggère que des changements subtils dans la gestion du lactate par les cellules rénales peuvent contribuer à la résistance à l’insuline et aux premiers signes de lésion rénale bien avant que la fonction rénale globale ne paraisse altérée. Comprendre et, à terme, cibler ce système de transport du lactate pourrait ouvrir de nouvelles voies pour protéger les filtres rénaux dans le diabète et d’autres maladies métaboliques.
Citation: Szrejder, M., Audzeyenka, I., Rachubik, P. et al. MCT1 as a critical regulator of insulin signaling, energy homeostasis and podocyte function. Sci Rep 16, 5906 (2026). https://doi.org/10.1038/s41598-026-37093-x
Mots-clés: podocytes rénaux, métabolisme du lactate, résistance à l’insuline, barrière de filtration glomérulaire, transporteur MCT1