Clear Sky Science · fr
Quantification automatisée des lymphocytes infiltrant la tumeur par apprentissage automatique révèle des caractéristiques pronostiques et immunogénomiques dans le cancer du poumon
Pourquoi compter de minuscules cellules immunitaires dans les tumeurs pulmonaires importe
Le cancer du poumon reste l’un des cancers les plus meurtriers, mais tous les tumeurs ne se comportent pas de la même manière. Certaines sont largement surveillées par des cellules immunitaires qui pénètrent à l’intérieur de la tumeur, tandis que d’autres restent presque intactes. Ces lymphocytes infiltrant la tumeur, ou LIT, peuvent indiquer le pronostic d’un patient et si celui‑ci pourrait bénéficier des traitements d’immunothérapie modernes. Le problème est qu’aujourd’hui, les LIT sont généralement comptés à l’œil au microscope, ce qui est lent et subjectif. Cette étude pose une question d’actualité : peut‑on utiliser l’apprentissage automatique pour mesurer automatiquement ces cellules sur des lames de pathologie de routine, et qu’est‑ce que cela révèle sur la biologie du cancer du poumon et la survie des patients ?
Transformer des lames ordinaires en cartes numériques
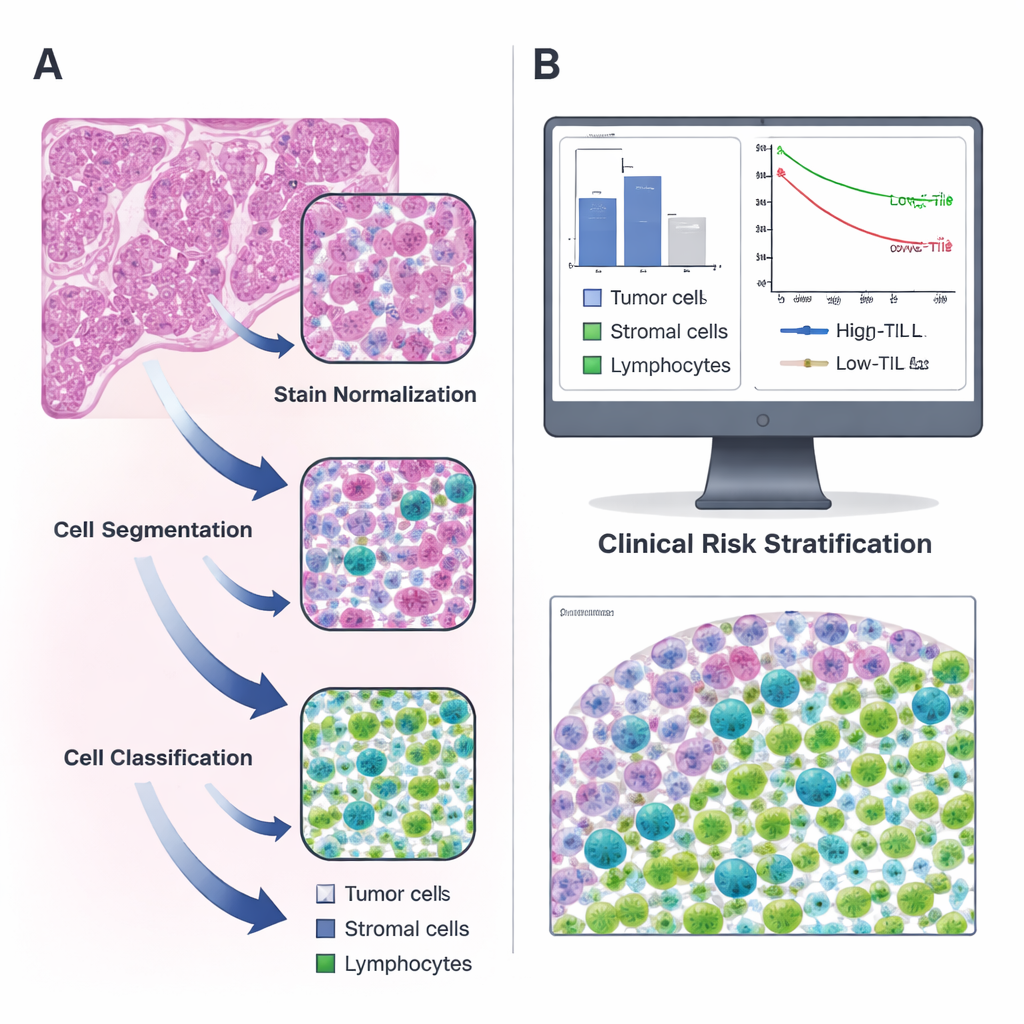
Les chercheurs se sont concentrés sur l’adénocarcinome pulmonaire, un type courant de cancer du poumon, en utilisant des données publiques du Cancer Genome Atlas ainsi qu’un jeu de patients indépendant provenant de leur propre hôpital. Pour chaque patient, ils ont analysé des lames de tissu colorées au hématoxyline et à l’éosine (H&E), ces images rose et pourpre que tout pathologiste connaît bien. Avec le logiciel open source QuPath, ils ont construit une chaîne de traitement étape par étape : d’abord ils ont corrigé les différences de colorimétrie entre les lames ; ensuite ils ont utilisé un algorithme de watershed pour séparer les noyaux cellulaires chevauchants ; enfin, un classifieur informatisé entraîné a étiqueté chaque cellule détectée comme tumeur, tissu de soutien (stroma) ou lymphocyte. Deux pathologistes experts ont examiné et corrigé de manière répétée le travail de la machine jusqu’à ce qu’elle reconnaisse de façon fiable les différents types cellulaires par elle‑même.
Relier le nombre de cellules immunitaires aux résultats des patients
Une fois le système capable d’identifier les cellules avec confiance, l’équipe a calculé le nombre de lymphocytes présents par millimètre carré de tissu tumoral pour plus de 300 patients. Ils ont constaté que les niveaux de LIT variaient largement et représentaient en moyenne seulement une petite fraction de l’ensemble des cellules. À l’aide d’une approche statistique pour déterminer le seuil le plus informatif, ils ont retenu 135 LIT par millimètre carré comme ligne de séparation entre tumeurs à LIT « élevé » et « faible ». Les patients dont les tumeurs dépassaient ce seuil vivaient plus longtemps que ceux dont l’infiltration immunitaire était faible, et ce schéma se confirmait à la fois dans le groupe initial et dans le groupe de validation. En d’autres termes, un simple chiffre produit par un outil automatisé captait des différences de survie significatives, faisant écho à des études antérieures plus laborieuses reposant sur un comptage manuel.
À quoi ressemblent les tumeurs riches en cellules immunitaires en profondeur
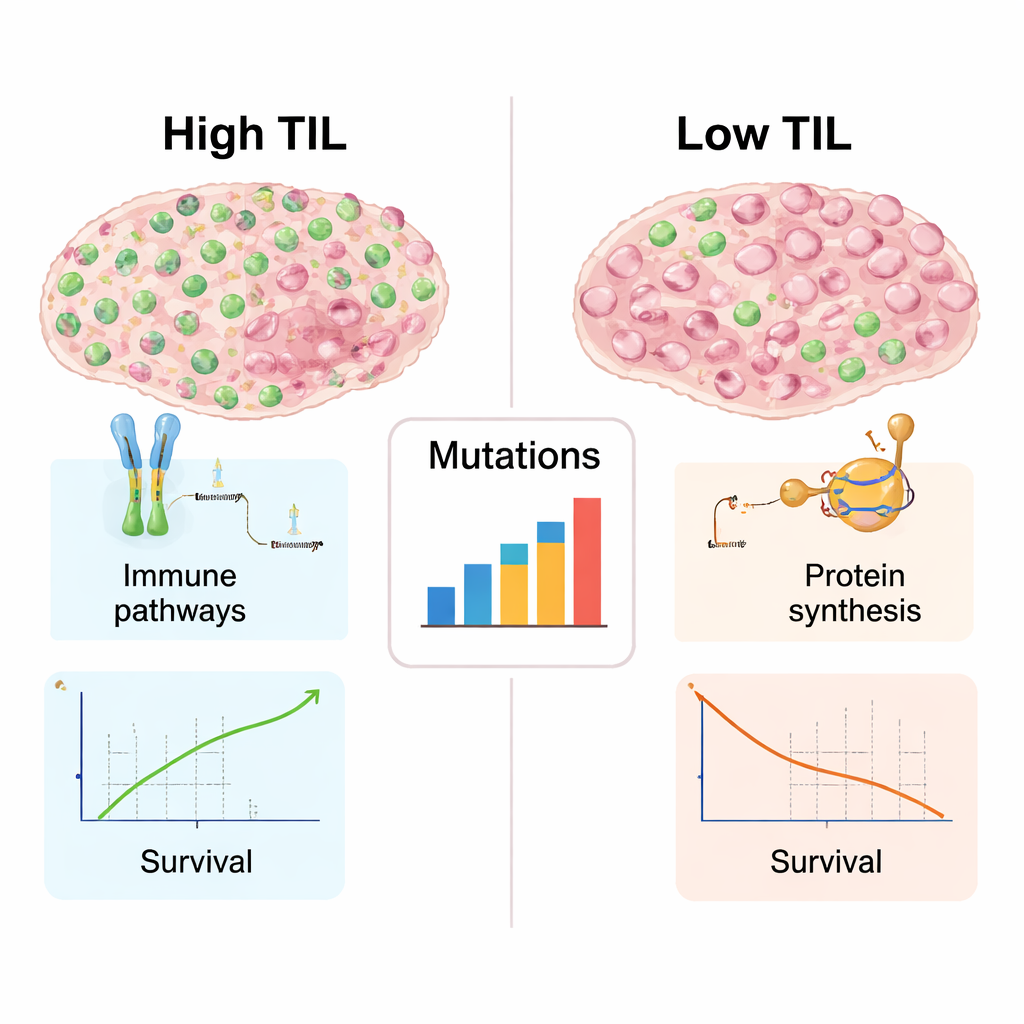
Parce que des données génétiques et moléculaires étaient disponibles pour bon nombre de ces tumeurs, les auteurs ont pu explorer ce qui distinguait les cancers à LIT élevé de ceux à LIT faible au‑delà du simple comptage cellulaire. Les tumeurs fourmillant de lymphocytes montraient des signatures d’activité immunitaire plus marquées : des gènes impliqués dans la reconnaissance des protéines anormales, leur présentation aux lymphocytes T et la coordination de l’attaque immunitaire étaient tous plus actifs. Ces tumeurs présentaient également une diversité plus large de mutations de l’ADN, qui peuvent créer de nouvelles cibles pour le système immunitaire. En revanche, les tumeurs à faible LIT favorisaient l’expression de gènes liés à la fabrication de ribosomes et à la synthèse protéique, signe d’une importante machinerie de croissance mais d’un engagement immunitaire relativement discret. Cette division reflète le contraste désormais familier entre tumeurs « chaudes », riches en cellules immunitaires et plus susceptibles de répondre à l’immunothérapie, et tumeurs « froides », que le système immunitaire ignore pour la plupart.
Apprendre à un ordinateur à prédire le statut immunitaire
L’équipe est allée plus loin et s’est demandé si un ensemble compact de caractéristiques d’image pouvait prédire si une tumeur appartiendrait à la catégorie LIT élevé ou LIT faible sans compter explicitement chaque lymphocyte. Ils ont résumé des motifs texturaux subtils dans les lames — la façon dont l’intensité des pixels varie sur de petits voisinages — en ce qu’on appelle des caractéristiques de Haralick, et les ont combinés avec le stade clinique de la tumeur dans un modèle de forêt aléatoire. En validation croisée, ce classifieur a correctement séparé les tumeurs à LIT élevé de celles à LIT faible avec une forte précision, et il a conservé des performances raisonnables dans la cohorte hospitalière indépendante. Fait important, l’ensemble de l’approche fonctionne sur des ordinateurs standards en utilisant des logiciels librement disponibles, ce qui laisse penser que de nombreux laboratoires de pathologie pourraient, en principe, l’adopter sans matériel spécialisé.
Ce que cela signifie pour la prise en charge future du cancer du poumon
Pour un non‑spécialiste, le message clé est qu’un ordinateur peut apprendre à lire des lames de cancer du poumon de routine d’une manière qui reflète l’intensité de l’engagement du système immunitaire contre la tumeur. Des niveaux élevés de lymphocytes infiltrants signalent une bataille immunitaire plus active, un paysage mutationnel plus riche et une survie globale meilleure. Bien que des travaux supplémentaires soient nécessaires — surtout chez des patients effectivement traités par immunothérapie — cette méthode automatisée pourrait finalement aider les médecins à classer rapidement et de manière cohérente les tumeurs en catégories immunitaires « chaudes » et « froides ». Cela pourrait, à son tour, orienter les décisions sur qui est le plus susceptible de bénéficier des traitements à base d’immunité et susciter de nouvelles stratégies pour rendre les tumeurs froides plus chaudes.
Citation: Li, A., Pang, Y., Zhang, H. et al. Automated quantification of tumor-infiltrating lymphocytes by machine learning reveals prognostic and immunogenomic features in lung cancer. Sci Rep 16, 7006 (2026). https://doi.org/10.1038/s41598-026-37076-y
Mots-clés: adénocarcinome pulmonaire, lymphocytes infiltrant la tumeur, apprentissage automatique, pathologie numérique, immunothérapie du cancer