Clear Sky Science · fr
Diagnostic automatisé de la forme Plus et des stades précoces de la ROP à l’aide de modèles d’apprentissage profond
Pourquoi de petits yeux et des ordinateurs intelligents importent
Chaque année, des milliers de nouveau-nés prématurés risquent de perdre la vue parce que les vaisseaux sanguins à l’arrière de leurs yeux ne se développent pas normalement, une affection appelée rétinopathie du prématuré (ROP). Détecter ce problème tôt peut sauver la vision, mais cela exige des examens oculaires fréquents réalisés par des spécialistes hautement qualifiés — des experts souvent peu nombreux dans de nombreuses régions du monde. Cette étude examine comment l’intelligence artificielle (IA) moderne peut aider les médecins à repérer les signes avant-coureurs dans des photographies rétiniennes, pouvant ainsi apporter un dépistage de niveau expert aux hôpitaux et cliniques dépourvus de spécialistes oculaires.
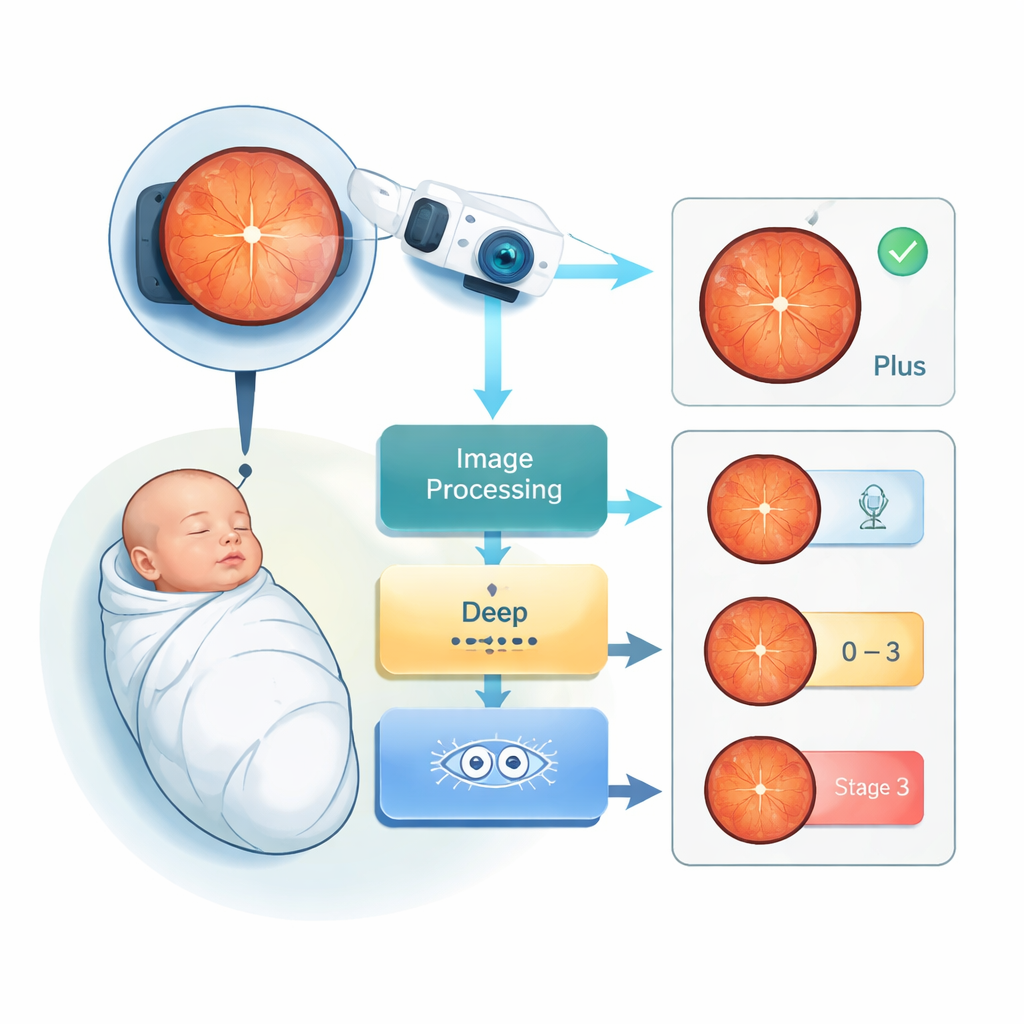
Le problème : une vision fragile chez les tout-petits
La ROP se développe lorsque la naissance prématurée interrompt la croissance normale des vaisseaux sanguins de la rétine, la couche photosensible au fond de l’œil. Les nourrissons nés très tôt ou avec un très faible poids de naissance sont les plus à risque. Dans les cas légers, l’œil se rétablit spontanément. Dans les cas sévères, des vaisseaux anormaux peuvent tirer sur la rétine et provoquer une cécité permanente. Dans le monde, on estime que la ROP cause la cécité chez environ 50 000 personnes, en particulier dans les régions où l’amélioration des soins néonatals a augmenté la survie sans que les programmes de dépistage ou les spécialistes n’aient suivi le rythme. Le dépistage actuel est chronophage, coûteux et subjectif : deux experts peuvent parfois diverger sur le degré de gravité de la maladie chez un nourrisson.
Ce que recherchent les médecins : vaisseaux tortueux et stades précoces
Les ophtalmologistes évaluent la ROP en se fondant sur deux indices principaux dans les images rétiniennes. L’un est le stade général de la maladie, du stade 0 (aucun changement visible) aux stades précoces du problème (1–3). L’autre est la « maladie Plus », un signe d’alerte où les vaisseaux rétiniens deviennent anormalement dilatés et tortueux. La maladie Plus signale un risque accru de lésions graves et déclenche souvent un traitement comme la photocoagulation au laser ou des injections de médicaments. Évaluer ces caractéristiques visuellement est difficile, surtout lorsque les images sont floues ou lorsque les nourrissons nécessitent des examens répétés semaine après semaine. Un système capable de signaler automatiquement la maladie Plus et d’estimer le stade de la ROP à partir des images seul serait un outil d’aide précieux pour les cliniciens.
Comment l’IA voit : tracer des cartes vasculaires à partir de photos oculaires
Les chercheurs ont construit une chaîne d’IA en deux étapes en utilisant plus de 6 000 images rétiniennes provenant de 188 nourrissons. D’abord, ils ont entraîné un réseau neuronal à dessiner une « carte des vaisseaux » précise de chaque rétine, mettant en évidence chaque vaisseau visible, y compris les ramifications les plus fines. Parmi plusieurs modèles de traitement d’image concurrents, une version appelée U-Net++ s’est révélée la plus efficace pour capturer des motifs vasculaires détaillés, en particulier dans des images bruitées ou à faible contraste. Pour améliorer la clarté, l’équipe a appliqué à chaque photo des filtres d’augmentation de contraste et de réduction de bruit avant la segmentation. Pour la détection de la maladie Plus, ils ont ensuite alimenté uniquement les cartes vasculaires — et non les photos couleur complètes — dans un second réseau neuronal, car la maladie Plus est définie presque entièrement par l’épaisseur et la courbure des vaisseaux.
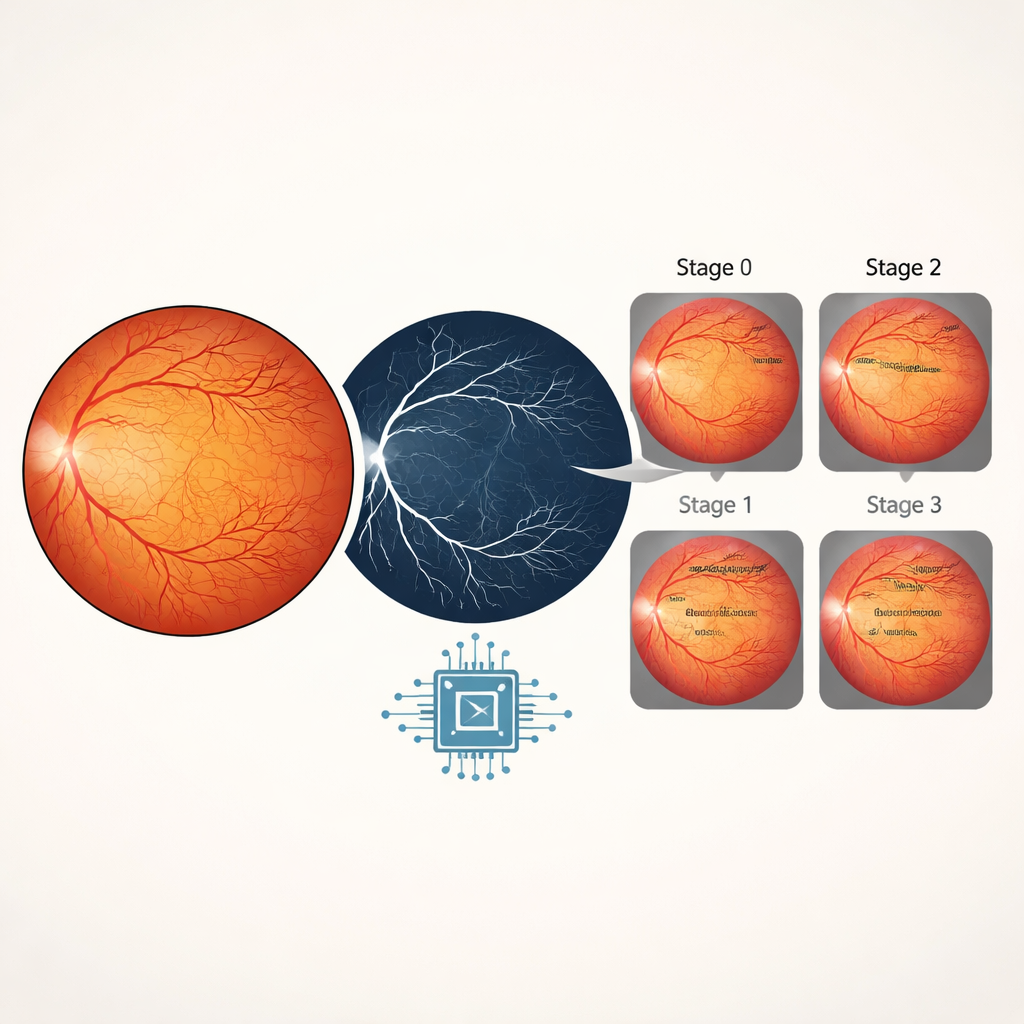
Apprendre au réseau à grader la sévérité de la maladie
Pour évaluer le stade de la ROP, l’IA avait besoin de plus que la seule morphologie des vaisseaux. Le système a donc combiné les images rétiniennes couleur originales avec leurs cartes vasculaires correspondantes, offrant au modèle à la fois une vue d’ensemble de la rétine et une vision affinée de ses vaisseaux. L’équipe a testé plusieurs architectures deep learning bien connues et a constaté qu’un modèle appelé EfficientNetB4 offrait le meilleur compromis entre précision et efficacité. Sur des images de validation mises à l’écart, le détecteur de maladie Plus a atteint une précision de 99,6 %, tandis que le classificateur de stade a obtenu 98 % de précision pour les stades 0 à 3. Des vérifications supplémentaires, incluant des courbes précision-rappel et des courbes ROC, ont montré que le modèle conservait une sensibilité élevée (manquant rarement la maladie) et une spécificité élevée (générant rarement des fausses alertes), malgré la rareté de la maladie Plus par rapport aux images normales.
Regarder à l’intérieur de la « boîte noire »
Parce que les cliniciens doivent pouvoir faire confiance à tout outil influençant les décisions thérapeutiques, les auteurs ont exploré la manière dont leur IA prenait ses décisions. À l’aide de méthodes de visualisation comme t-SNE, ils ont montré que les images de différentes classes (par exemple Plus vs Normal ou Stade 1 vs Stade 3) formaient des clusters bien séparés dans l’espace de caractéristiques interne du modèle. Avec des cartes de chaleur de type Grad-CAM, ils ont mis en évidence les zones de chaque rétine qui influaient le plus sur une prédiction. Pour la maladie Plus, le modèle se focalisait sur les régions où les vaisseaux étaient anormalement larges ou tortueux, en accord avec les critères des experts. Pour le grading des stades, il prêtait aussi attention à d’autres régions comme le disque optique et la macula, ce qui suggère que son raisonnement s’alignait étroitement sur des critères médicaux établis plutôt que sur des artefacts d’image fortuits.
Ce que cela signifie pour les nourrissons et les cliniques
En termes simples, ce travail montre qu’un système d’IA soigneusement conçu peut lire des images rétiniennes de nourrissons prématurés avec une précision proche de celle d’experts, tant pour détecter des modifications vasculaires dangereuses que pour évaluer l’avancement de la maladie. L’étude a été réalisée dans un seul centre médical et n’a inclus que des stades précoces à modérés, de sorte que des essais plus larges multi-hospitaliers et des données issues de cas plus avancés restent nécessaires. Néanmoins, les résultats suggèrent qu’avec une validation supplémentaire et une intégration prudente dans des plateformes de télémédecine, de tels outils pourraient aider des systèmes de santé surchargés à dépister beaucoup plus d’enfants, de manière plus cohérente et à moindre coût. Cela pourrait signifier un traitement plus précoce et une meilleure chance de préserver la vue pour certains des patients les plus vulnérables en soins néonatals.
Citation: Vahidmoghadam, M., Ghorbani, P., Ahmadi, M.J. et al. Automated diagnosis of plus form and early stages of ROP using deep learning models. Sci Rep 16, 7234 (2026). https://doi.org/10.1038/s41598-026-37064-2
Mots-clés: rétinopathie du prématuré, intelligence artificielle, apprentissage profond, imagerie médicale, maladie oculaire néonatale