Clear Sky Science · fr
Recherche sur le mécanisme moléculaire du célastrol ciblant CTNNB1/STAT3 pour inhiber le mélanome uvéal basée sur la pharmacologie de réseau et l’analyse multi-omique
La médecine ancienne rencontre le cancer de l’œil
Le mélanome uvéal est un cancer rare mais mortel qui prend naissance à l’intérieur de l’œil. Une fois qu’il se propage, les traitements actuels changent peu le pronostic. Cette étude examine si le célastrol — une molécule extraite d’une plante utilisée en médecine traditionnelle chinoise — pourrait être réorientée pour combattre ce cancer. En combinant la biologie des mégadonnées, des simulations informatiques et des expériences en laboratoire, les chercheurs dévoilent comment le célastrol pourrait désactiver des commutateurs moléculaires clés qui aident le mélanome uvéal à croître et à se disséminer.
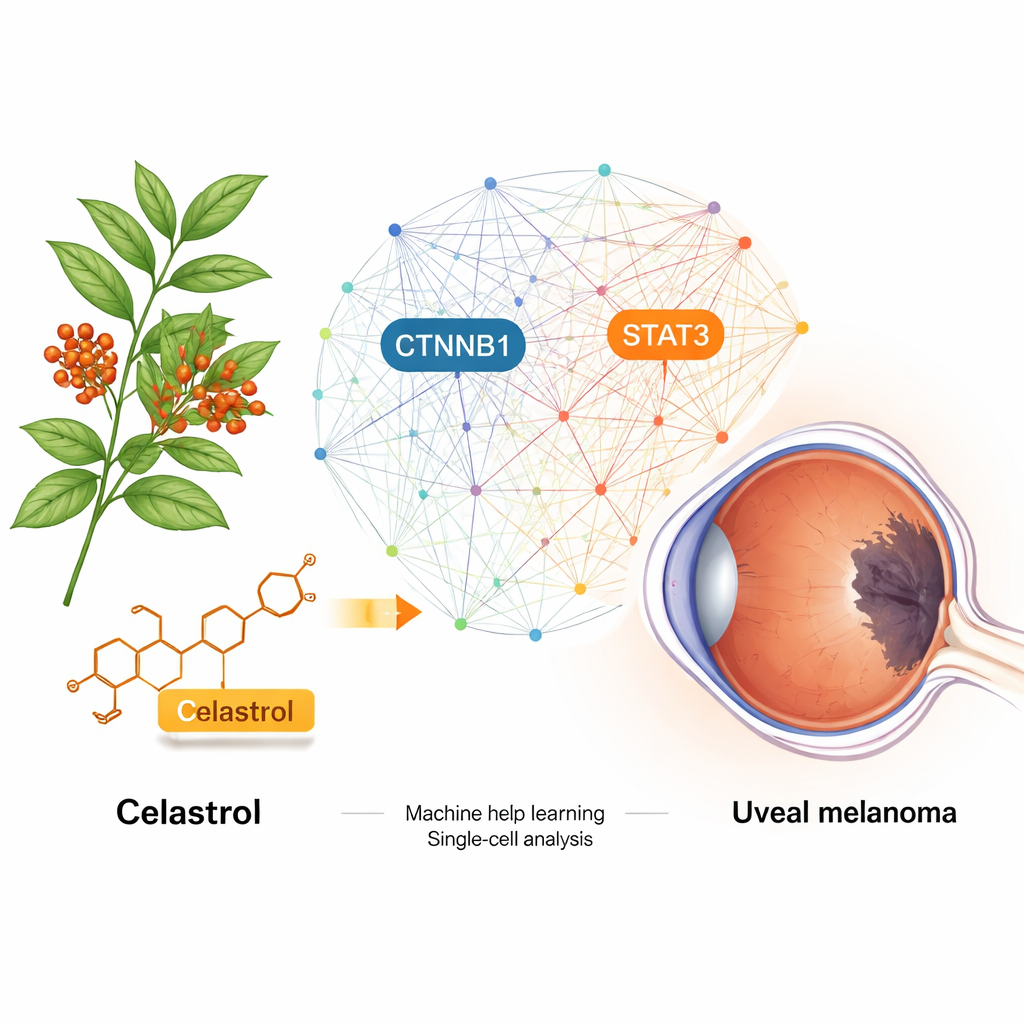
Ce qui rend cette tumeur oculaire si dangereuse
Le mélanome uvéal est le cancer primitif de l’œil le plus fréquent chez l’adulte, et environ la moitié des patients développent finalement des métastases, généralement au foie. À ce stade, la survie se compte souvent en mois. Les traitements standards tels que la chirurgie, la radiothérapie et les thérapies locales peuvent contrôler la tumeur oculaire principale, mais les médicaments systémiques ont eu un succès limité et peuvent provoquer des effets indésirables graves. Les scientifiques cherchent donc des médicaments capables à la fois de freiner la croissance tumorale et d’être mieux tolérés — un domaine où les produits naturels comme le célastrol suscitent un vif intérêt.
Un composé naturel passé au crible
Le célastrol provient de Tripterygium wilfordii, une plante utilisée depuis longtemps en médecine traditionnelle chinoise. Des travaux antérieurs ont montré qu’il peut ralentir la croissance de plusieurs cancers, mais son mode d’action dans le mélanome uvéal restait incertain. L’équipe a commencé par exploiter de nombreuses bases de données biomédicales pour prédire quelles protéines humaines le célastrol pourrait cibler et quelles protéines sont fortement associées au mélanome uvéal. En comparant ces listes, ils ont identifié 46 candidats communs. À l’aide d’outils informatiques cartographiant les interactions entre protéines, ils ont réduit ce nombre à quelques « hubs » moléculaires situés aux points de contrôle de voies majeures de croissance et de survie tumorales.
Se concentrer sur deux commutateurs maîtres
Pour identifier les acteurs les plus critiques, les chercheurs ont combiné les données géniques tumorales de patients du Cancer Genome Atlas avec trois méthodes d’apprentissage automatique différentes. Les trois approches ont convergé vers deux gènes : CTNNB1, composante centrale de la voie Wnt qui stimule la croissance cellulaire, et STAT3, régulateur clé de l’inflammation, de la survie et de l’évasion immunitaire. Des analyses supplémentaires d’échantillons tumoraux en vrac et de séquençage ARN monocellulaire ont montré que ces gènes sont fortement actifs dans les cellules du mélanome uvéal, en particulier dans des sous-groupes cellulaires plus agressifs, et sont liés à des modifications des cellules immunitaires environnantes. En bref, CTNNB1 et STAT3 apparaissent comme des commutateurs maîtres aidant la tumeur à prospérer tout en maintenant le système immunitaire à distance.
Des modèles informatiques aux cellules vivantes
L’équipe a ensuite utilisé le dock moléculaire et de longues simulations de dynamique moléculaire pour tester si le célastrol pouvait se lier physiquement à CTNNB1 et STAT3. Les expériences virtuelles ont suggéré une liaison forte et stable, soutenue par plusieurs liaisons hydrogène et un emballage serré autour du médicament. Ensuite, en laboratoire, ils ont traité des cellules humaines de mélanome uvéal et une lignée de mélanome murin apparentée avec du célastrol. Dans les deux cas, le célastrol a fortement réduit la survie cellulaire et la formation de colonies, ralenti la migration dans des tests de cicatrisation, et déclenché la mort cellulaire programmée. Il a aussi provoqué un blocage des cellules à des points spécifiques du cycle cellulaire, les empêchant de se diviser. Lorsque les chercheurs ont mesuré l’activité génique et les niveaux protéiques, ils ont constaté que le célastrol diminuait nettement CTNNB1 et STAT3, confirmant qu’il atteint ses cibles prédictes à l’intérieur des cellules vivantes.
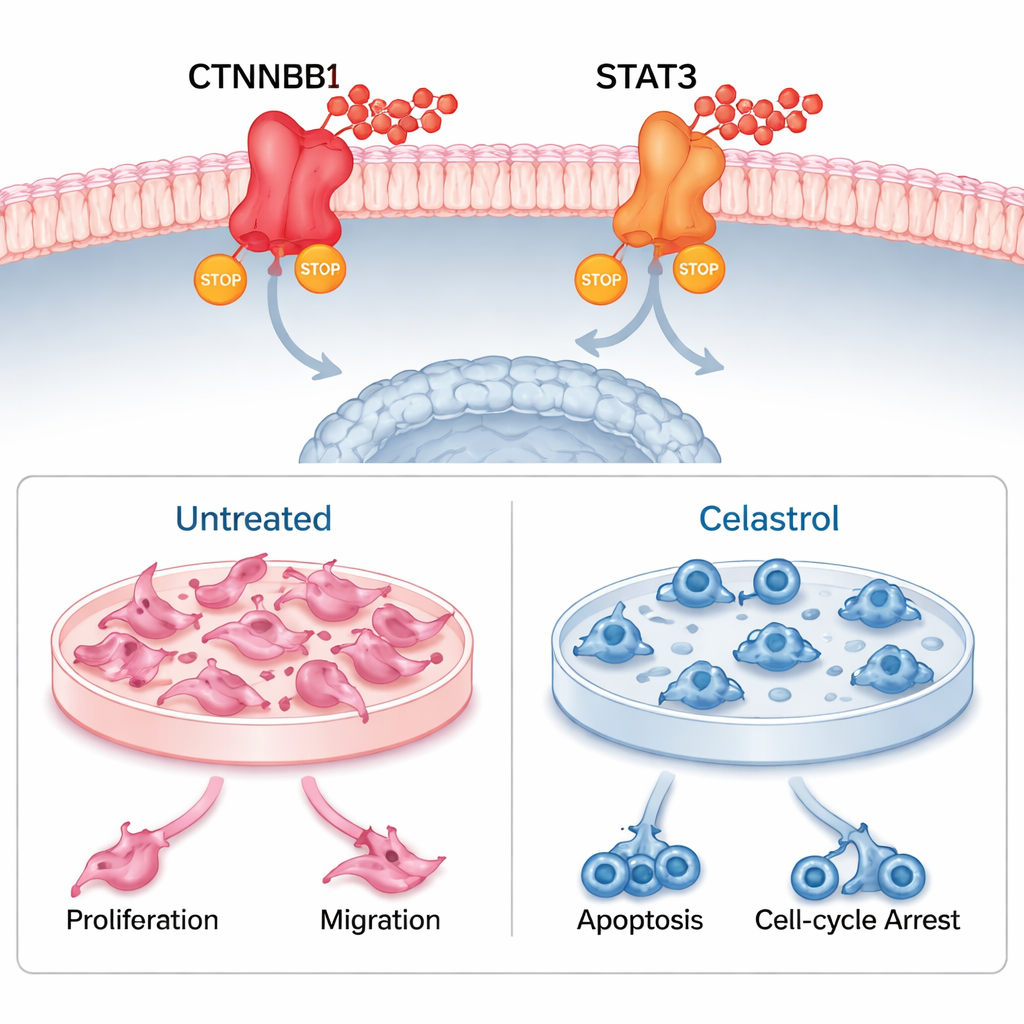
Ce que cela pourrait signifier pour les traitements futurs
Pris ensemble, les résultats suggèrent que le célastrol combat le mélanome uvéal en désactivant simultanément CTNNB1 et STAT3. Cette action double ralentit non seulement la croissance et la dissémination tumorales, mais peut aussi remodeler le microenvironnement immunitaire de la tumeur de manière à favoriser une réponse anticancéreuse. Bien que ces travaux aient été réalisés sur des modèles cellulaires et informatiques — pas encore chez l’homme ni chez l’animal — ils établissent une base solide pour des tests ultérieurs. Pour le grand public, le message clé est qu’un composé issu de la médecine traditionnelle apparaît comme un candidat scientifiquement plausible pour une nouvelle classe de traitements du cancer de l’œil, ciblant à la fois la tumeur et l’écosystème cellulaire qui l’entoure.
Citation: Li, Z., Xi, R., Han, X. et al. Research on the molecular mechanism of celastrol targeting CTNNB1/STAT3 to inhibit uveal melanoma based on network pharmacology and multi-omics analysis. Sci Rep 16, 6140 (2026). https://doi.org/10.1038/s41598-026-37061-5
Mots-clés: mélanome uvéal, célastrol, cancer de l’œil, signalisation du cancer, microenvironnement tumoral