Clear Sky Science · fr
Biomarqueurs potentiels pour l’inflammation parodontale précoce : examen des lymphocytes B CD5+, des cytokines salivaires et du microbiome buccal
Pourquoi vos gencives comptent pour tout votre corps
Les saignements des gencives sont faciles à négliger, mais l’inflammation qui en est la cause peut discrètement éroder l’os qui maintient les dents et est associée aux maladies cardiaques, au diabète et à d’autres affections. Cette étude s’est demandée si des signes avant-coureurs de ce type de dommage peuvent être détectés dans un échantillon quotidien — la salive — ainsi que dans certains globules immunitaires du sang et dans l’ensemble de bactéries cachées sous la ligne gingivale. Trouver des marqueurs précoces fiables pourrait aider les dentistes à repérer les patients à risque bien avant que la perte irréversible des dents n’apparaisse.
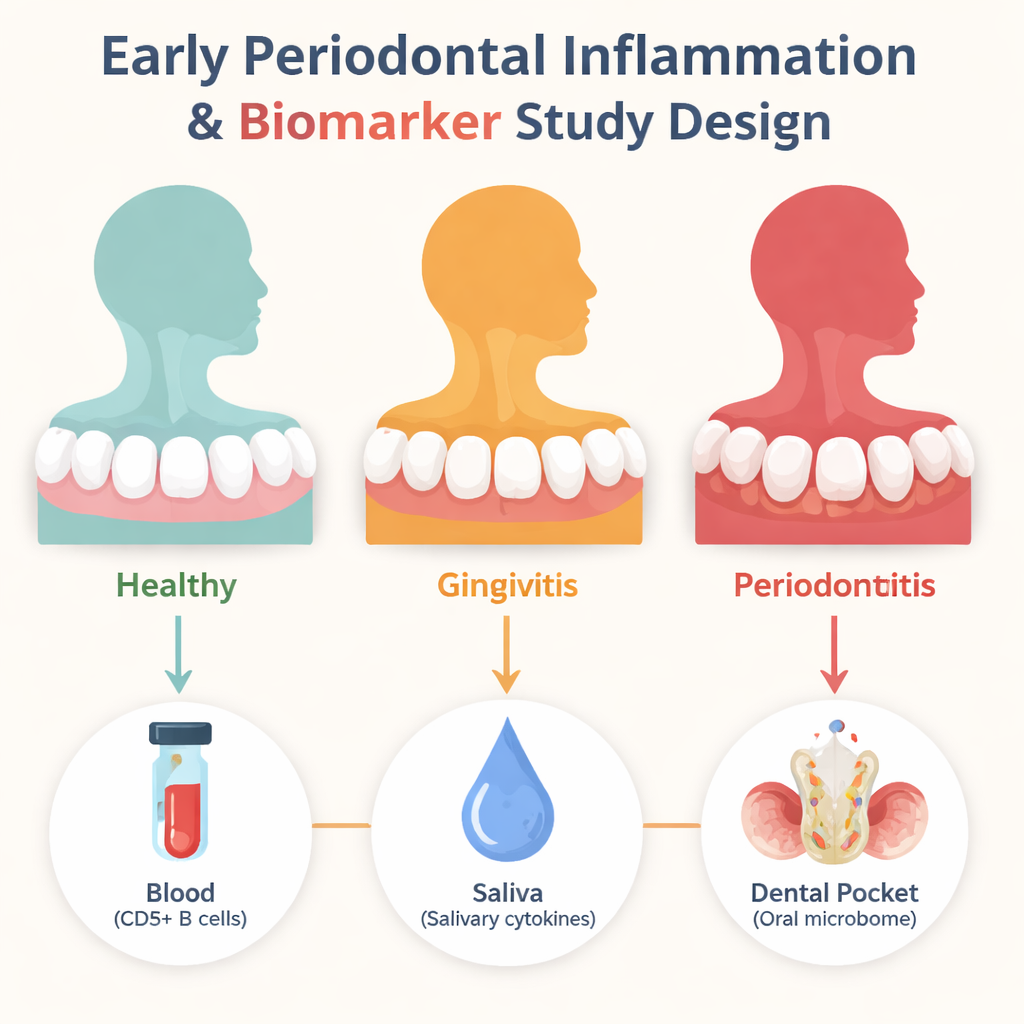
À la recherche de voyants d’alerte précoces
Les chercheurs se sont concentrés sur trois types d’indices. D’abord, ils ont examiné un groupe particulier de cellules immunitaires dans le sang appelées lymphocytes B CD5 positifs, qui, dans les formes sévères de maladie des gencives et dans la polyarthrite rhumatoïde, ont été associés à la dégradation osseuse et à des attaques auto-immunes. Ensuite, ils ont mesuré des dizaines de protéines de signalisation, ou cytokines, dans la salive, qui agissent comme des alarmes chimiques lorsque les tissus sont irrités. Enfin, ils ont séquencé l’ADN bactérien du liquide prélevé dans les poches gingivales pour voir comment le microbiome buccal évolue lorsque la santé cède la place à la gingivite puis à une parodontite chronique modérée. Soixante adultes non-fumeurs ont été soigneusement classés en groupes sains, gingivite ou parodontite chronique modérée selon la profondeur gingivale, le saignement et les scores de plaque.
Les cellules immunitaires sanguines restent calmes
Au vu des travaux antérieurs sur les maladies avancées, l’équipe s’attendait à ce que les personnes atteintes de parodontite présentent déjà des niveaux accrus de lymphocytes B CD5 positifs dans le sang, indiquant une réaction systémique à l’infection gingivale chronique. De manière surprenante, les comptes totaux de ces cellules étaient essentiellement identiques dans les trois groupes, tournant autour d’un cinquième de tous les lymphocytes B. Même lorsque les scientifiques les ont ventilés selon les stades de développement — immatures, naïfs et plusieurs types de cellules mémoires — aucun schéma clair n’a atteint une signification statistique. Certaines cellules mémoires, en particulier celles associées aux réponses de longue durée, avaient tendance à être moins nombreuses chez les personnes malades, laissant entendre qu’elles pourraient quitter le sang pour s’accumuler dans les tissus gingivaux enflammés, mais des études plus importantes seront nécessaires pour confirmer cette tendance subtile.
La salive et les bactéries racontent une histoire plus nette
En revanche, la salive et la communauté bactérienne sous les gencives reflétaient clairement le stade de la maladie. Les personnes atteintes de parodontite présentaient à peu près le double du niveau médian de la chimiokine IL-8 dans la salive comparé aux participants sains ou atteints de gingivite, et avaient bien plus de chances d’avoir une IL-17A détectable ainsi que des signes d’activité d’IL-6 et d’IL-1β. Ces molécules recrutent des cellules immunitaires et stimulent des processus de résorption osseuse, leur augmentation suggère donc que des circuits inflammatoires sont déjà actifs même en cas de maladie modérée. Parallèlement, le séquençage de l’ADN montrait que les bouches saines étaient dominées par des bactéries inoffensives et aérobies telles que Rothia et Streptococcus. Avec la gingivite et surtout la parodontite, l’équilibre se déplaçait vers des espèces anaérobies, à Gram négatif, y compris Tannerella, Fusobacterium, Treponema et Fretibacterium, connues ou de plus en plus pointées du doigt dans la dégradation gingivale.
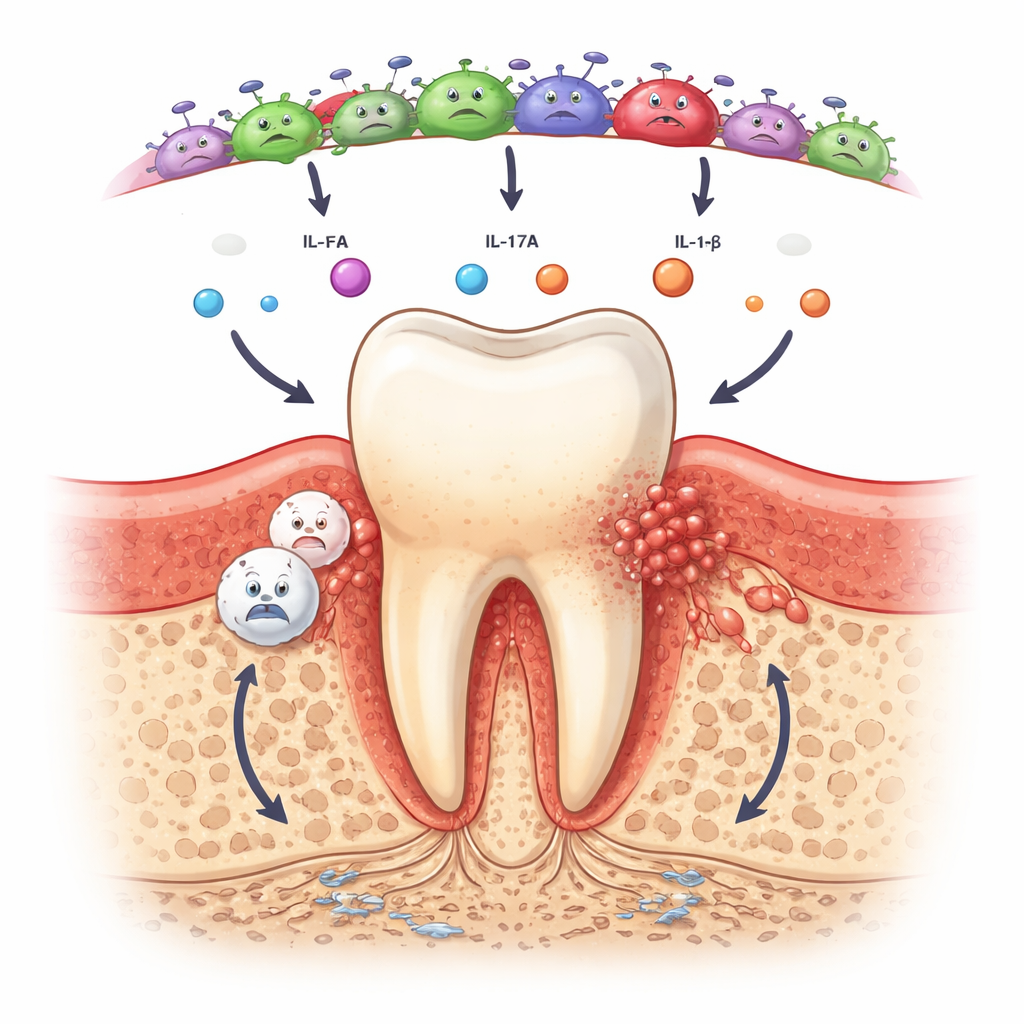
Premiers indices d’un profil à haut risque
En combinant statistiques et apprentissage automatique, l’équipe a identifié des groupes bactériens qui différenciaient le mieux les sites sains des sites malades. Deux souches de Tannerella forsythia et plusieurs espèces de Fretibacterium se sont révélées particulièrement informatives, tandis qu’une espèce de Rothia signalait des gencives en meilleure santé. Une observation intrigante est venue du groupe gingivite : les niveaux d’IL-8 dans la salive suivaient de près l’abondance d’un genre bactérien appelé Megasphaera. Ce lien n’apparaissait ni dans les bouches saines ni dans la parodontite avancée, ce qui suggère que Megasphaera associé à l’IL-8 pourrait servir d’indicateur de stade précoce quand les lésions sont encore limitées et potentiellement réversibles. Cependant, la taille de l’échantillon était modeste, et les auteurs insistent sur le fait que de tels patterns doivent être testés dans des études plus larges et longitudinales avant de pouvoir orienter la prise en charge.
Ce que cela signifie pour les patients
Pour les personnes inquiètes de l’état de leurs gencives, la leçon est que l’organisme envoie des signaux biochimiques précoces de problème, mais ceux-ci apparaissent davantage dans la salive locale et le microbiome gingival que dans les cellules immunitaires circulantes quand la maladie est encore modérée. Les tests sanguins de routine pour les lymphocytes B CD5 positifs ont peu de chances de détecter une parodontite précoce. À la place, l’approche la plus prometteuse pourrait être un panel salivaire et microbiomique combiné qui suive plusieurs cytokines — en particulier IL-8 et IL-17A — ainsi que des espèces bactériennes clés comme Tannerella, Fretibacterium et Megasphaera. Si cela est validé, un test simple basé sur la bouche pourrait aider les dentistes à repérer plus tôt les patients à risque, à adapter les nettoyages et les traitements, et peut‑être à prévenir à la fois la perte dentaire et certains des problèmes de santé plus larges liés à l’inflammation gingivale chronique.
Citation: Gottschalk, E.C., Chabanovska, O., Vasudevan, P. et al. Potential biomarkers for early periodontal inflammation: investigating CD5+ B cells, salivary cytokines and oral microbiome. Sci Rep 16, 7192 (2026). https://doi.org/10.1038/s41598-026-37044-6
Mots-clés: maladie des gencives, microbiome buccal, biomarqueurs salivaires, parodontite, inflammation