Clear Sky Science · fr
Prédiction, par apprentissage automatique, de la transformation hémorragique après thrombectomie à partir d’angiographie numérique quantitative
Pourquoi cela compte pour les patients victimes d’un AVC
Lorsqu’une personne subit un AVC majeur, les médecins peuvent parfois retirer le caillot de l’artère principale du cerveau à l’aide d’un dispositif miniature lors d’une procédure appelée thrombectomie mécanique. Cette technique a transformé la prise en charge des AVC, mais de nombreux patients présentent encore de mauvais résultats, car certains développent un nouveau saignement cérébral. L’étude à l’origine de cet article pose une question simple mais cruciale : peut-on utiliser les données déjà collectées en salle d’opération, couplées aux méthodes modernes d’apprentissage automatique, pour prédire quels patients ont le plus de risque de saigner et nécessiter des précautions supplémentaires ?
Aller au-delà du « artère ouverte ou fermée »
Aujourd’hui, le succès après une thrombectomie est généralement évalué par l’aspect de l’artère sur l’angiographie, une sorte de film radiologique en temps réel des vaisseaux sanguins. Mais cette évaluation grossière ne révèle pas ce qui se passe dans les petits vaisseaux en aval du cerveau, là où surviennent réellement les lésions et les hémorragies. Certains patients dont les grosses artères semblent parfaitement rouverte développent néanmoins une hémorragie cérébrale grave, dite transformation hémorragique. Les auteurs ont émis l’hypothèse que des mesures plus fines du flux sanguin dans ces petits vaisseaux, extraites de la même angiographie, pourraient contenir des indices cachés sur le risque.
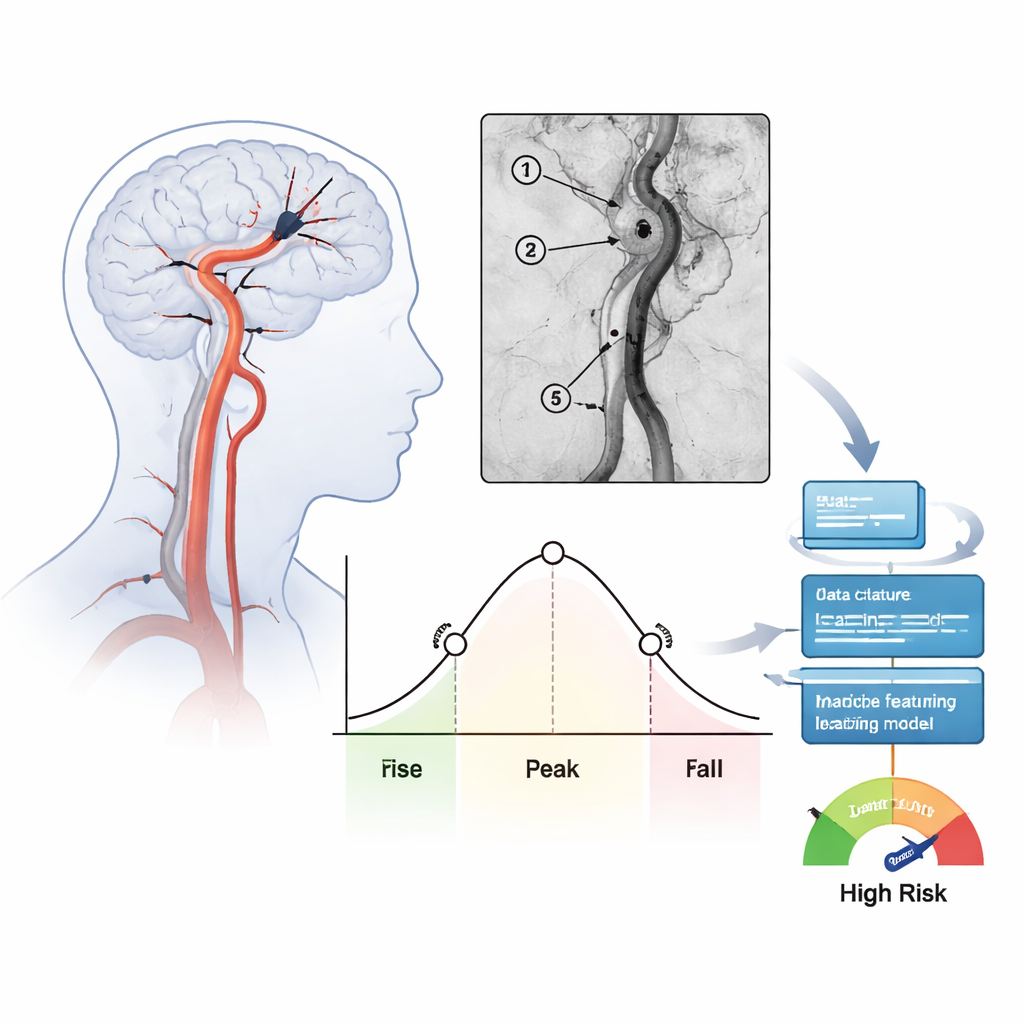
Transformer les films angiographiques en chiffres
L’équipe a étudié 171 personnes traitées pour des AVC sévères de la partie antérieure du cerveau sur une période d’un an dans un même hôpital. Après l’extraction du caillot et la restauration du flux, les médecins ont enregistré des vues d’angiographie standard, puis analysé la manière dont le produit de contraste injecté entrait et sortait de plusieurs sites clés le long de l’artère traitée. Pour chaque région, ils ont calculé des mesures temporelles telles que le temps moyen de transit et la largeur de la crête de contraste à mi-hauteur (full width at half maximum). Ces nombres résument si le sang circule lentement et régulièrement ou s’il traverse rapidement en une pulsation étroite. Au total, 39 caractéristiques de flux ont été extraites pour chaque patient et vérifiées pour leur cohérence entre opérateurs indépendants.
Apprendre à l’ordinateur à reconnaître les profils à risque
Les chercheurs ont ensuite utilisé un ensemble de méthodes d’apprentissage automatique courantes pour déterminer si ces caractéristiques de flux, seules ou combinées à des données cliniques de base comme l’âge et la sévérité de l’AVC, pouvaient distinguer les patients qui ont développé ultérieurement une hémorragie cérébrale de ceux qui ne l’ont pas fait. Pour éviter le surapprentissage, ils ont d’abord appliqué cinq techniques de sélection de caractéristiques différentes pour retenir les mesures les plus informatives, puis ont largement partagé les données en ensembles d’apprentissage et de test par validation croisée. Parmi les nombreuses combinaisons testées, un modèle relativement simple — régression logistique, optimisée avec un filtre de caractéristiques de type « Elastic Net » — s’est révélé le plus performant. Lorsqu’il reposait uniquement sur des mesures de flux dérivées de l’angiographie, il séparait correctement les patients avec et sans hémorragie avec une aire sous la courbe ROC d’environ 0,81 en moyenne. En ajoutant des facteurs cliniques, la performance montait autour de 0,86, ce qui suggère que le modèle pourrait constituer un solide outil d’aide à la décision.
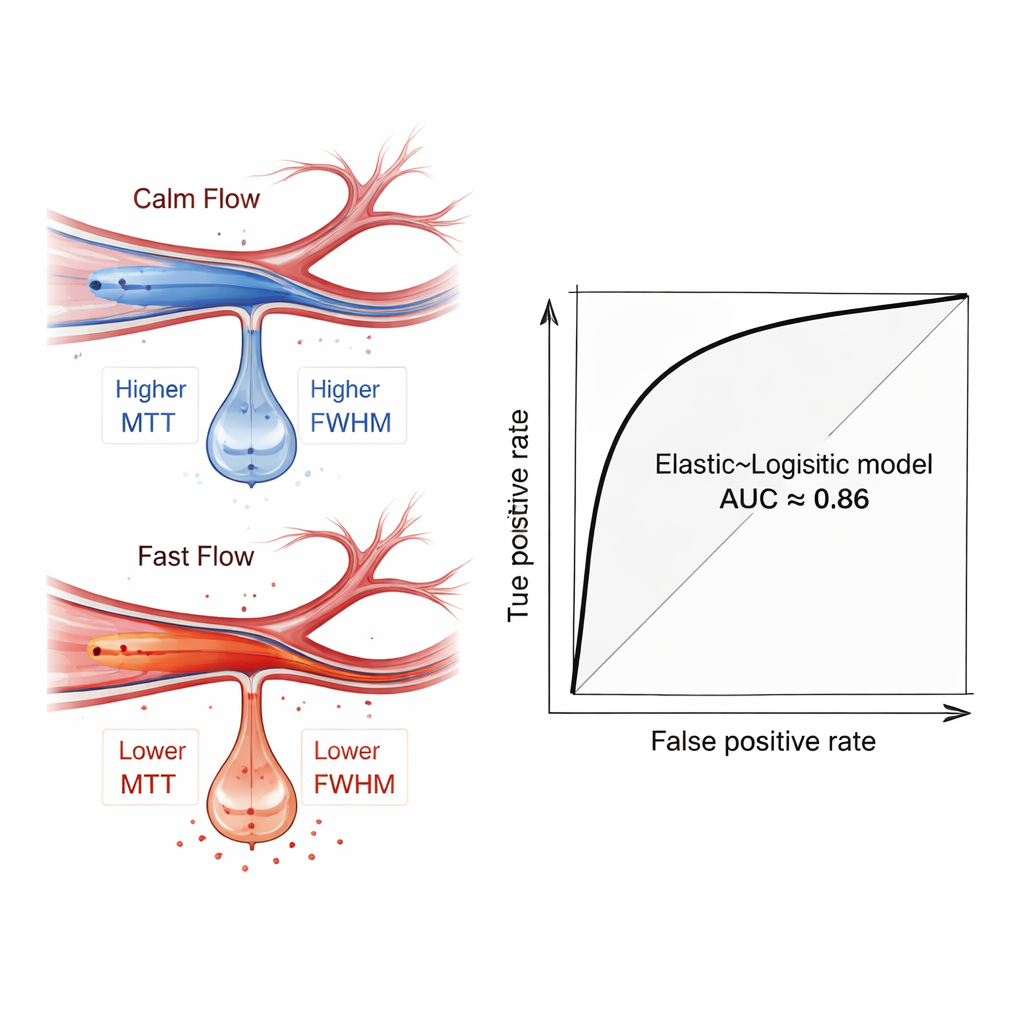
Ce que révélaient les signaux de flux sanguin
En explorant les modèles entraînés, les auteurs ont utilisé une technique d’interprétabilité appelée SHAP pour identifier les caractéristiques les plus déterminantes. Les mesures reflétant la durée et l’étalement de la pulsation de flux — en particulier dans une branche plus distale de l’artère cérébrale moyenne — sont apparues comme des prédicteurs clés. Les patients qui ont saigné par la suite présentaient tendanciellement un flux plus rapide et plus focalisé dans ces vaisseaux distaux, traduit par des temps de transit plus courts et des pics plus étroits. Ce profil hémodynamique est la marque d’une « hyperperfusions » : un état où un tissu cérébral fragile, brutalement reperfusé après une ischémie, est plus susceptible de fuir et de saigner. Il est important de noter que ce signal est apparu même lorsque des comparaisons de groupes simples n’affichaient pas de différences statistiques marquées, ce qui souligne la valeur d’une analyse multicaractéristiques pilotée par machine.
Comment cela pourrait changer la prise en charge au chevet
Puisque la méthode utilise des images déjà acquises pendant la thrombectomie, elle ne requiert pas d’examens supplémentaires, de contraste ou de radiation. Une fois les régions d’intérêt tracées — une étape qui prend actuellement quelques minutes — l’ordinateur peut calculer automatiquement les mesures de flux et produire une estimation personnalisée du risque hémorragique. En théorie, cela pourrait aider les médecins à adapter les objectifs tensionnels, décider de l’intensité d’utilisation des anticoagulants et programmer des scanners CT plus précoces pour les patients identifiés à haut risque. Les auteurs précisent que leur étude est rétrospective et monocentrique, et que des essais plus larges, impliquant plusieurs hôpitaux, sont nécessaires avant que l’outil puisse guider la pratique courante. Néanmoins, cela constitue une preuve de concept claire : en transformant les angiogrammes d’AVC en données numériques riches et en laissant l’apprentissage automatique les analyser, on peut dépasser la question « l’artère est-elle ouverte ? » pour demander « la microcirculation cérébrale est-elle sûre ? » — un changement susceptible, à terme, d’épargner davantage de patients d’hémorragies post‑traitement dangereuses.
Citation: Li, H., Pang, C., Guo, X. et al. Machine learning-enabled prediction of hemorrhagic transformation post-thrombectomy using quantitative DSA. Sci Rep 16, 6008 (2026). https://doi.org/10.1038/s41598-026-37036-6
Mots-clés: AVC, thrombectomie mécanique, hémorragie cérébrale, apprentissage automatique, angiographie