Clear Sky Science · fr
Impact des traitements systémiques spécifiques des néoplasmes neuroendocrines sur l’expression et la fonction de CXCR4 dans les cellules tumorales neuroendocrines
Pourquoi cela compte pour les soins du cancer à venir
Lorsque certains cancers rares de l’intestin et du pancréas deviennent plus agressifs, ils cessent souvent de répondre aux traitements ciblés standard. Médecins et chercheurs ont un besoin urgent de nouvelles façons de visualiser et d’attaquer ces tumeurs plus résistantes. Cette étude pose une question pratique aux implications importantes : les chimiothérapies et médicaments ciblés déjà administrés aux patients modifient-ils un marqueur tumoral clé appelé CXCR4, en cours de développement à la fois comme « balise » diagnostique et comme cible thérapeutique ?
Une cible qui évolue sur les cellules tumorales agressives
Les néoplasmes neuroendocrines sont des cancers rares issus de cellules productrices d’hormones, le plus souvent dans l’intestin et le pancréas. Dans leur forme initiale, plus ordonnée, ces tumeurs présentent généralement une molécule de surface appelée récepteur de la somatostatine 2, que les médecins peuvent imager et traiter avec des médicaments radioactifs spécialisés. Quand la maladie devient plus agressive, ces tumeurs ont tendance à perdre ce marqueur, ce qui les rend plus difficiles à détecter et à cibler. En parallèle, bon nombre d’entre elles activent une autre molécule de surface, un récepteur nommé CXCR4, associé à une croissance plus rapide, à la dissémination vers des organes distants et à une survie plus faible. Parce que CXCR4 peut être imagé avec un traceur TEP et potentiellement attaqué par des agents radiopharmaceutiques ou des anticorps, il est apparu comme une « cible de secours » prometteuse lorsque les options standard échouent.
Tester des médicaments du monde réel sur des modèles cellulaires tumoraux
Les chercheurs ont voulu savoir comment les médicaments déjà utilisés pour traiter les tumeurs neuroendocrines de haut grade affectent CXCR4 lui‑même. Si ces médicaments réduisent par inadvertance CXCR4, ils pourraient affaiblir les futures imageries ou thérapies basées sur CXCR4 — mais ils pourraient aussi contribuer à freiner l’agressivité du cancer. L’équipe a travaillé avec trois lignées cellulaires tumorales humaines représentant des formes agressives de la maladie, dont une lignée hybride qui imite de près des tumeurs particulièrement difficiles à traiter. Ils ont exposé ces cellules à six agents courants : les chimiothérapies cisplatine, étoposide, streptozotocine, 5‑fluorouracile, le médicament oral temozolomide, et l’inhibiteur ciblé de mTOR everolimus. Après traitement, ils ont mesuré CXCR4 au niveau génétique et protéique et évalué la capacité des cellules à capturer un traceur TEP ciblant CXCR4.
Certains médicaments réduisent le signal CXCR4
Les résultats montrent que tous les médicaments anticancéreux n’agissent pas de la même façon sur ce récepteur. Le cisplatine a clairement réduit l’activité génétique de CXCR4 dans deux des trois lignées cellulaires et a significativement diminué la captation du traceur dans deux d’entre elles, ce qui signifie qu’il y avait moins de récepteurs fonctionnels pour la liaison du traceur. Le temozolomide et l’everolimus ont également abaissé les niveaux génétiques et protéiques de CXCR4 dans plusieurs types cellulaires, bien que cela ne se soit pas toujours traduit par une baisse statistiquement nette de la captation du traceur. En revanche, l’étoposide et la streptozotocine ont eu peu d’effet sur CXCR4, tandis que le 5‑fluorouracile a entraîné des modifications modestes qui n’ont pas fortement altéré la liaison du traceur. Dans l’ensemble, le schéma suggère que le cisplatine, le temozolomide et l’everolimus peuvent tous atténuer CXCR4 dans ces cellules tumorales agressives, tandis que les autres agents le laissent principalement inchangé.
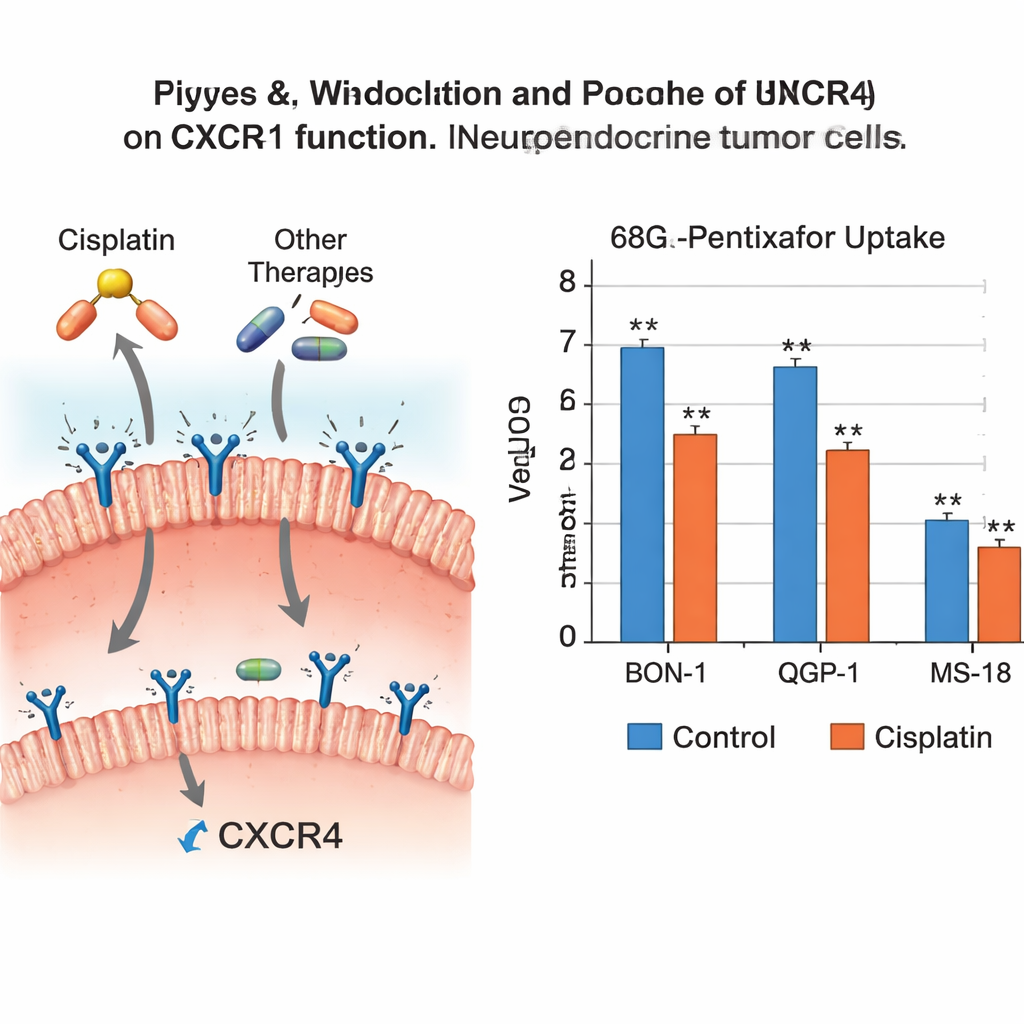
Ce que cela signifie pour les examens d’imagerie et le calendrier des traitements
Ces constats portent un double message pour la prise en charge future des patients. D’une part, la réduction de CXCR4 peut faire partie du mécanisme par lequel des médicaments comme le cisplatine, le temozolomide et l’everolimus ralentissent la dissémination tumorale, car un fort taux de CXCR4 est lié à l’invasion et aux métastases. D’autre part, si CXCR4 d’une tumeur est supprimé par un traitement en cours, les TEP basés sur CXCR4 peuvent sous‑estimer l’étendue de la maladie, et les thérapies radiopharmaceutiques ciblant CXCR4 peuvent disposer de moins de sites d’ancrage. L’étude suggère que combiner directement des traitements ciblant CXCR4 avec ces médicaments systémiques est peu susceptible d’améliorer l’efficacité des thérapies centrées sur CXCR4, et pourrait même les affaiblir.
Un nouvel élément du puzzle pour une thérapie personnalisée
Pour les non‑spécialistes, l’idée principale est qu’un seul marqueur tumoral peut jouer deux rôles à la fois : il peut être un signe d’alerte d’une maladie agressive et, en même temps, une poignée utile pour l’imagerie et le traitement ciblé. Cette recherche montre que certains médicaments anticancéreux établis peuvent ajuster discrètement ce marqueur à la hausse ou à la baisse. En pratique, cela pourrait influencer le moment choisi pour programmer des examens et des thérapies basés sur CXCR4 — idéalement lorsque le récepteur est le plus abondant — et aider à expliquer pourquoi certains traitements sont efficaces contre les tumeurs neuroendocrines à croissance rapide. Bien que ces résultats proviennent de modèles cellulaires et doivent être confirmés chez les patients, ils constituent une étape importante vers un ordonnancement plus éclairé des thérapies pour les personnes atteintes de ces cancers difficiles.
Citation: Däubler, C., Böttcher, C., Landwehr, LS. et al. Impact of neuroendocrine neoplasm-specific systemic treatments on expression and function of CXCR4 in neuroendocrine tumor cells. Sci Rep 16, 4339 (2026). https://doi.org/10.1038/s41598-026-37026-8
Mots-clés: tumeurs neuroendocrines, CXCR4, cisplatine, everolimus, imagerie ciblée