Clear Sky Science · fr
Un biocapteur électrochimique M13 modifié–rGO pour la détection rapide de protéines virales dans des matrices complexes
Pourquoi les tests rapides de virus restent importants
La pandémie de COVID-19 a montré combien il est crucial de détecter rapidement les virus, non seulement chez les patients mais aussi dans des lieux tels que les eaux usées et les lignes de production alimentaire. Les tests de laboratoire actuels sont puissants mais peuvent être lents, coûteux et dépendants d'ingrédients biologiques fragiles difficiles à expédier et à stocker. Cette étude présente un nouveau type de capteur électronique miniature qui utilise des virus modifiés et une feuille de matériau carboné avancé pour détecter une protéine clé du SARS-CoV-2 en moins d'une seconde, même dans des échantillons réels complexes comme le sérum sanguin, le lait et les eaux usées.
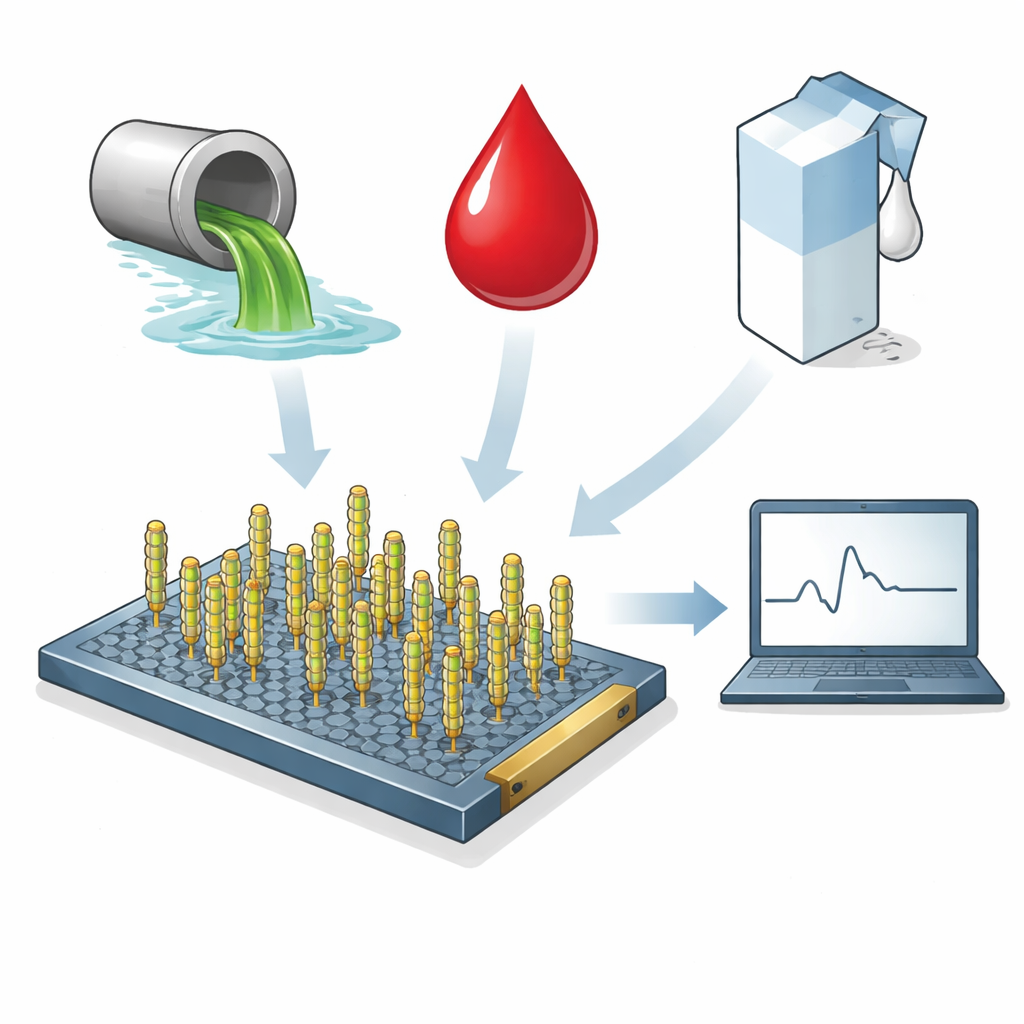
Transformer un virus inoffensif en détecteur intelligent
Au cœur de l'appareil se trouve le M13, un virus inoffensif qui infecte normalement les bactéries. Son corps long et cylindrique est recouvert de nombreuses protéines de capside identiques que les scientifiques peuvent reprogrammer génétiquement. L'équipe a inséré un court peptide personnalisé sur l'une de ces protéines afin que les particules de M13 reconnaissent et s'attachent au fragment S1 de la protéine de spicule du coronavirus. Une seconde version du virus, portant un peptide « brouillé », a servi de témoin pour montrer que la réponse provient d'une reconnaissance spécifique plutôt que d'une simple adhésion aléatoire.
S'appuyer sur une feuille de carbone d'un atome d'épaisseur
Pour transformer ce virus programmable en capteur, les chercheurs l'ont fixé sur un film plat d'oxyde de graphène réduit, une forme hautement conductrice de carbone obtenue en traitant chimiquement le graphite. Après avoir étalé de l'oxyde de graphène sur de petites puces de verre et chauffé pour le convertir en oxyde de graphène réduit, ils ont ajouté une molécule de liaison qui adhère à la surface carbonée et se lie aussi aux groupes amine du virus. Cela a créé une couche dense de particules de M13 ancrées à la feuille conductrice. La microscopie électronique et la microscopie à force atomique ont confirmé que chaque étape de fabrication modifiait la surface comme prévu, et les mesures électriques ont montré qu'ajouter le lien puis le virus augmentait progressivement la résistance, signe d'un enrobage réussi de la surface.
Lire la liaison virale comme une impulsion électrique
À la différence de nombreux biocapteurs qui nécessitent des réactifs chimiques ou des pièces mobiles, cette plateforme fonctionne comme une simple résistance sous une très faible tension constante. Lorsque la protéine S1 atterrit sur la surface recouverte de virus et se lie au peptide affiché, elle modifie légèrement la manière dont la charge circule à travers la couche de graphène. Cela se manifeste par un bref pic de courant électrique qui apparaît environ 300 millisecondes après le dépôt d'une goutte d'échantillon sur la puce, puis s'estompe à mesure que le système se stabilise. En réglant la tension appliquée, l'équipe a trouvé une zone optimale autour de -0,8 millivolt, où le signal provenant de la liaison spécifique au S1 était fort tandis que le bruit de fond et les réponses à des protéines non liées, comme l'albumine sérique bovine, restaient faibles.
Fonctionner dans des échantillons réels et complexes
Les chercheurs ont ensuite mis le capteur au défi avec des mélanges complexes qui font souvent échouer des réactifs de laboratoire délicats. Ils ont testé l'appareil en tampon, en eaux usées municipales, en sérum fœtal bovin (un substitut du sang) et en lait pasteurisé, avec et sans ajout de protéine S1. En utilisant un seuil statistiquement défini pour marquer un résultat positif, le capteur a détecté des niveaux de protéine extrêmement faibles en tampon — jusqu'à environ 10⁻⁴ picogramme par millilitre — comparables ou supérieurs à de nombreux systèmes basés sur des anticorps. Dans les eaux usées, l'appareil signalait de manière fiable des niveaux plus élevés de S1, tandis que dans le sérum et le lait il détectait aussi de faibles concentrations, le tout en une fraction de seconde. De manière importante, un capteur témoin construit avec le virus au peptide brouillé montrait peu de réponse au S1, confirmant que le signal dépend de la séquence de liaison ingénierée. Un capteur parallèle utilisant un anticorps conventionnel sur la même plateforme en graphène a donné des performances similaires, ce qui suggère que le système à base de virus peut égaler la sensibilité des anticorps tout en étant potentiellement moins coûteux et plus facile à produire.

Ce que cela pourrait signifier pour les tests quotidiens
Les anticorps, piliers de nombreux diagnostics, sont coûteux à fabriquer, sensibles à la chaleur et nécessitent généralement une chaîne du froid de l'usine à la clinique. À l'inverse, les virus M13 peuvent être cultivés dans des bactéries comme une simple culture, tolèrent des conditions plus rudes et peuvent être reprogrammés en réécrivant leur code génétique. En mariant cette robustesse et cette flexibilité à une lecture électronique rapide et à faible consommation sur graphène, l'étude trace une voie vers des dispositifs portables et peu coûteux qui pourraient être adaptés pour détecter de nombreux marqueurs de maladie ou contaminants simplement en changeant le peptide affiché. Le travail en est encore au stade de la preuve de concept et n'a pas encore été testé sur des échantillons cliniques humains, mais il ouvre la perspective d'un avenir où des capteurs portatifs pourraient dépister des protéines virales et d'autres biomarqueurs dans les cabinets, les égouts ou même les produits alimentaires en quelques secondes, sans la logistique des tests traditionnels basés sur des anticorps.
Citation: Alshehhi, H.Y., Tizani, L., Palanisamy, S. et al. An engineered M13 phage–rGO electrochemical biosensor for rapid detection of viral protein in complex matrices. Sci Rep 16, 9279 (2026). https://doi.org/10.1038/s41598-026-37008-w
Mots-clés: biocapteur, graphène, bactériophage, SARS-CoV-2, détection électrochimique