Clear Sky Science · fr
L’imagerie du temps de vie de fluorescence sans marqueur peut distinguer le cancer du tissu sain dans des tumeurs buccales canines survenant spontanément
Voir le cancer sous un nouveau jour
Les cancers de la bouche, chez l’homme comme chez les animaux de compagnie, sont notoirement difficiles à retirer complètement. Les chirurgiens doivent pratiquer des marges de sécurité larges autour d’une tumeur pour éviter de laisser des cellules cancéreuses invisibles, mais dans la cavité buccale cela peut entraîner la perte d’os, de dents et de tissus mous essentiels à la mastication et à la parole. Cette étude explore une méthode d’imagerie basée sur la lumière utilisée pendant la chirurgie chez des chiens de compagnie qui pourrait aider les chirurgiens à distinguer en temps réel le tissu cancéreux du tissu sain — épargnant potentiellement davantage de tissu normal tout en contrôlant la maladie.
Pourquoi il est si difficile de trouver les bords des tumeurs
Lors des interventions pour cancers de la tête et du cou, les médecins s’appuient souvent sur l’analyse rapide de tissus congelés pour juger si les bords d’une tumeur excisée sont réellement indemnes de cancer. Ce procédé est lent, n’analyse qu’un petit nombre de zones et peut manquer des foyers de maladie. Des défis similaires compliquent le traitement des chiens atteints de tumeurs buccales, où la récidive locale reste fréquente. Faute d’une méthode fiable pour « voir » le cancer microscopique pendant l’opération, les chirurgiens enlèvent habituellement des marges généreuses, ce qui peut nuire à la mastication, à la déglutition et à l’apparence. Les auteurs ont voulu tester une approche d’imagerie non invasive susceptible de tracer une ligne plus nette entre tissu tumoral et tissu normal directement au bloc opératoire.
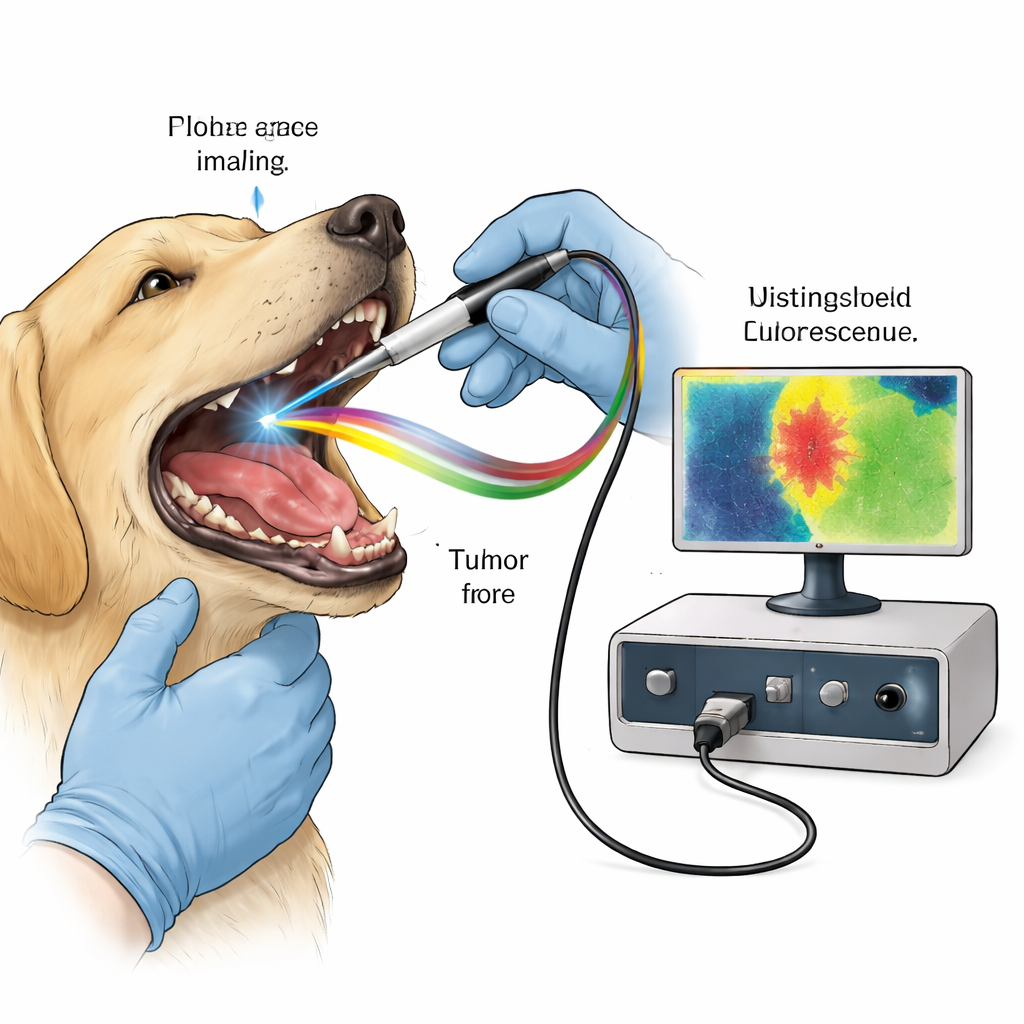
Utiliser la luminescence naturelle comme guide chirurgical
De nombreuses molécules présentes dans nos tissus émettent naturellement une faible fluorescence après excitation par une brève impulsion laser. Le collagène du tissu conjonctif et des molécules liées au métabolisme cellulaire comme le NADH et le FAD possèdent chacune des couleurs et des durées caractéristiques lorsqu’elles s’allument et s’éteignent. Le cancer perturbe la structure tissulaire et l’utilisation d’énergie, modifiant subtilement cette empreinte fluorescente. L’imagerie du temps de vie de fluorescence (FLIm) ne mesure pas seulement l’intensité de la fluorescence, elle mesure la durée de cette émission en milliardièmes de seconde, une propriété moins dépendante des conditions d’observation. L’équipe a utilisé une sonde portative sur mesure qui émet de rapides impulsions ultraviolettes dans la région tumorale de chiens anesthésiés et enregistre la fluorescence renvoyée sur trois canaux spectraux accordés au collagène, aux molécules métaboliques et à un composé émettant dans le rouge appelé protoporphyrine IX (PpIX).
Ajouter un colorant qui cible le cancer : aide ou battage ?
La PpIX peut s’accumuler dans de nombreuses tumeurs lorsqu’on administre aux patients un précurseur, l’acide 5-aminolévulinique (5-ALA), par voie orale. Sous lumière bleue, les zones riches en PpIX brillent souvent en rose vif et sont utilisées par les chirurgiens pour repérer le cancer. Les chercheurs ont d’abord confirmé, dans des lignées cellulaires de cancers buccaux canins, que le 5-ALA entraînait une forte fluorescence de la PpIX et ont montré que des gènes impliqués dans la production et l’importation du 5-ALA étaient plus actifs dans les cellules cancéreuses. Ils ont ensuite inclus 15 chiens de compagnie atteints de tumeurs buccales survenant naturellement et leur ont administré du 5-ALA quelques heures avant la chirurgie. Au bloc opératoire, la plupart des tumeurs fluoresçaient visiblement, mais certaines lésions inflammatoires ou virales non cancéreuses s’éclairaient aussi, suggérant que la seule couleur visible pourrait ne pas marquer de façon fiable les limites tumorales.
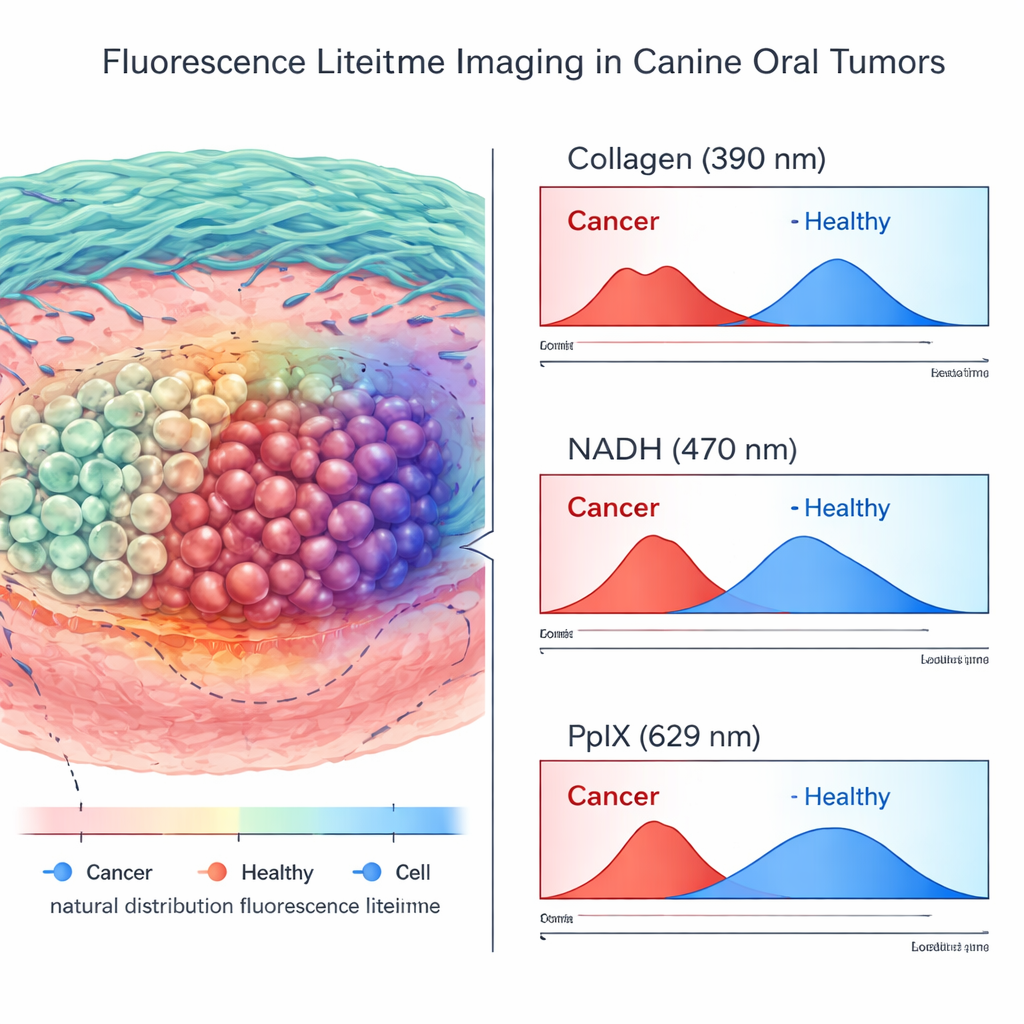
Ce que les images de durée de vie ont révélé
Sur plus de 200 000 points de mesure de haute qualité provenant de tumeurs et de tissus normaux voisins, l’équipe a comparé les signaux FLIm aux cartes pathologiques détaillées. Ils ont constaté que de nombreuses caractéristiques de durée de vie et d’intensité différaient significativement entre tissu cancéreux et tissu sain. Cependant, la séparation la plus forte et la plus cohérente provenait des canaux sans marqueur : des durées de vie plus courtes dans la bande sensible au collagène et des décalages caractéristiques dans la bande sensible au NADH étaient étroitement liés au cancer. En revanche, le canal PpIX — celui renforcé par le 5-ALA administré — apportait des informations moins fiables in vivo. Ses mesures variaient largement dans les régions normales, probablement parce que les gencives et les muqueuses enflammées accumulaient soit du 5-ALA soit contenaient des porphyrines naturellement fluorescentes mimant le signal tumoral.
Du bloc opératoire au laboratoire et retour
Lorsque les chercheurs ont imagé les spécimens excisés sur la table de travail, le tableau a légèrement changé. Hors du corps, certaines caractéristiques basées sur la PpIX sont devenues plus utiles pour distinguer le cancer du tissu sain, suggérant un rôle potentiel pour les contrôles marginaux « au fauteuil ». Néanmoins, lorsque des modèles statistiques sophistiqués et l’apprentissage automatique ont été appliqués, les classificateurs les plus performants pour les données peropératoires et exopératoires s’appuyaient fortement sur les signaux d’autofluorescence naturels plutôt que sur le colorant ajouté. La FLIm sans marqueur a atteint une précision respectable pour différencier tissu cancéreux et tissu normal par elle-même, tandis que l’inclusion de la PpIX apportait peu et introduisait parfois de la confusion.
Ce que cela signifie pour les chirurgies futures
Pour les propriétaires d’animaux et, en fin de compte, pour les patients humains, le message clé est que les chirurgiens pourraient un jour disposer d’un outil optique aidant à voir où le cancer s’arrête et où le tissu sain commence, sans dépendre de médicaments ou de colorants supplémentaires. Ce travail chez le chien — modèle réaliste de grande taille du cancer buccal humain — montre que les signatures fluorescentes propres au corps peuvent suffire à guider les décisions au bloc opératoire. L’ajout de 5-ALA et de PpIX dans ce contexte n’a pas amélioré l’exactitude suffisamment pour justifier le coût, la complexité et les effets secondaires potentiels. Les auteurs concluent que les efforts futurs devraient se concentrer sur le perfectionnement de l’imagerie du temps de vie de fluorescence sans marqueur — éventuellement en adaptant l’analyse à des sites anatomiques spécifiques — plutôt que de poursuivre davantage d’agents de contraste. Si cette technologie réussit, elle pourrait réduire les reprises chirurgicales et préserver davantage de tissu normal tout en maintenant le contrôle tumoral.
Citation: Goldschmidt, S., Marcu, L., Ehrlich, K. et al. Label-free fluorescence lifetime imaging can distinguish cancer from healthy tissue in spontaneously occurring canine oral tumors. Sci Rep 16, 6077 (2026). https://doi.org/10.1038/s41598-026-37001-3
Mots-clés: imagerie du cancer buccal, tumeurs buccales canines, temps de vie de fluorescence, marges chirurgicales, 5-ALA PpIX