Clear Sky Science · fr
Séquençage d’amplisons avec Oxford Nanopore Technologies comme alternative diagnostique pour les lentivirus des petits ruminants chez le mouton
Infections cachées chez les moutons du quotidien
Dans le monde entier, les moutons portent discrètement des virus qui peuvent affaiblir leur santé, raccourcir leur durée de vie et coûter de l’argent aux éleveurs—souvent sans symptômes évidents pendant des années. Cette étude explore une nouvelle façon de détecter ces infections cachées en utilisant une technologie portable de séquençage de l’ADN, offrant une avancée potentielle dans la protection du bien‑être animal, des revenus agricoles et même de la sécurité alimentaire.
Une maladie lente, coûteuse et difficile à repérer
Le travail se concentre sur les lentivirus des petits ruminants (SRLV), un groupe de virus qui infectent les moutons et les chèvres. Chez le mouton, ils provoquent la maladie Maedi‑Visna, une infection de longue durée pouvant entraîner des problèmes respiratoires, de l’arthrite, des atteintes cérébrales et une mammite chronique. De nombreux animaux infectés ne présentent jamais de signes clairs, pourtant le virus réduit la production laitière, augmente la mortalité des agneaux et conduit à des mises à mort précoces. Dans certains troupeaux laitiers européens, notamment en Espagne et en Grèce, environ la moitié des animaux peut être infectée, faisant de cette maladie l’une des plus importantes en élevage intensif.
Pourquoi les tests actuels ratent de nombreux animaux infectés
Aujourd’hui, les élevages s’appuient principalement sur des tests sanguins qui recherchent des anticorps (ELISA) ou sur des tests ADN standards (qPCR) pour décider quels animaux sont infectés et devraient être retirés du troupeau. Mais les SRLV mutent et recombinent rapidement, générant de nombreux variants viraux légèrement différents. Certains variants sont mal reconnus par les tests sérologiques, et certains moutons infectés ne développent jamais de réponses anticorps fortes. La qPCR, qui cible de courts segments très spécifiques de l’ADN viral, peut également échouer si ces régions cibles changent. En conséquence, de nombreux animaux réellement infectés donnent un résultat négatif et restent dans le troupeau, propageant silencieusement le virus.
Utiliser la lecture d’ADN en temps réel pour détecter le virus
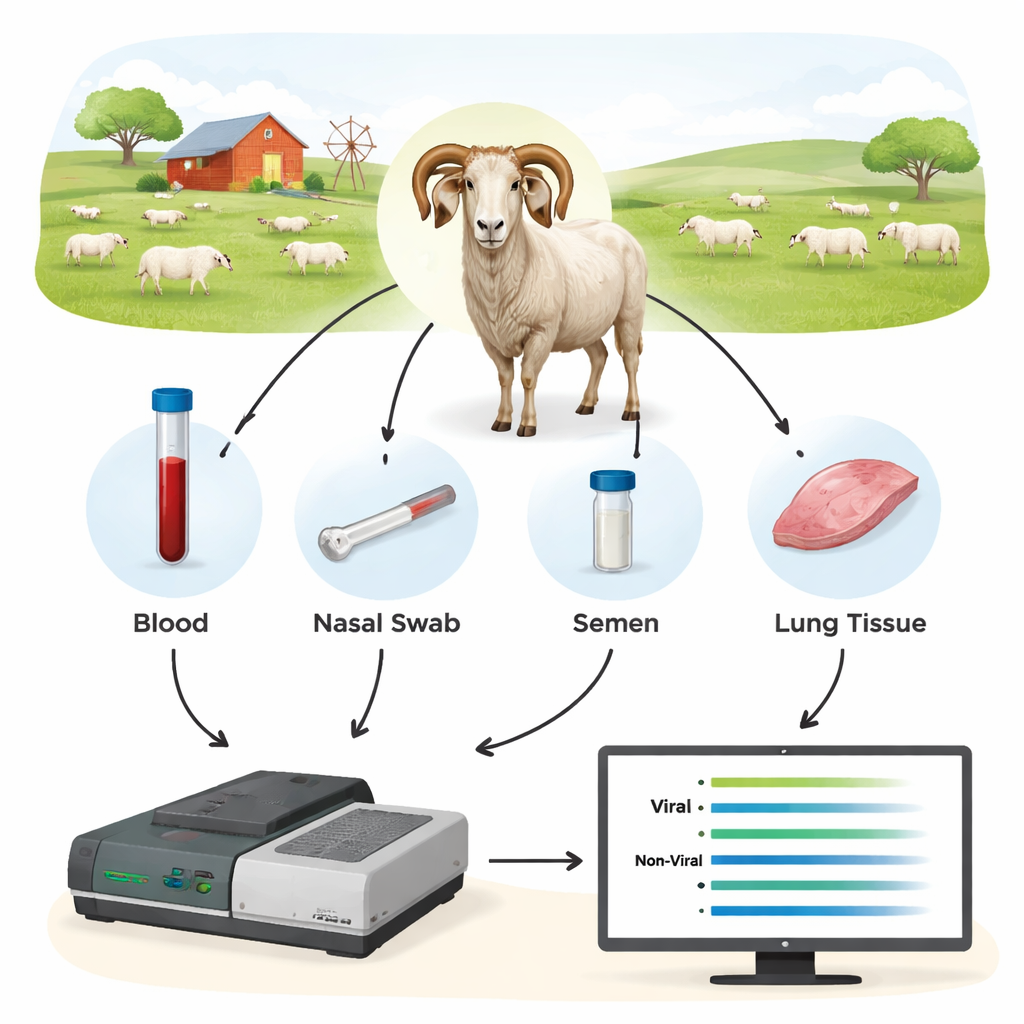
Les chercheurs ont testé une méthode de troisième génération appelée séquençage Oxford Nanopore comme nouvel outil diagnostique. Plutôt que de rechercher un seul et minuscule fragment d’ADN viral, ils ont d’abord amplifié des segments plus longs de gènes viraux clés à partir des échantillons animaliers, puis séquencé ces fragments en temps réel sur un appareil Nanopore. Ils ont collecté du sang, des écouvillons nasaux, du sperme et des cellules provenant du sang et des poumons de 44 béliers et d’autres moutons, dont beaucoup avaient déjà été testés par des méthodes conventionnelles. En ciblant des régions virales relativement conservées mais suffisamment longues pour révéler la souche exacte, l’équipe a pu à la fois détecter l’infection et identifier les types viraux présents.
Le sang fonctionne le mieux—et trouve ce que les autres tests manquent
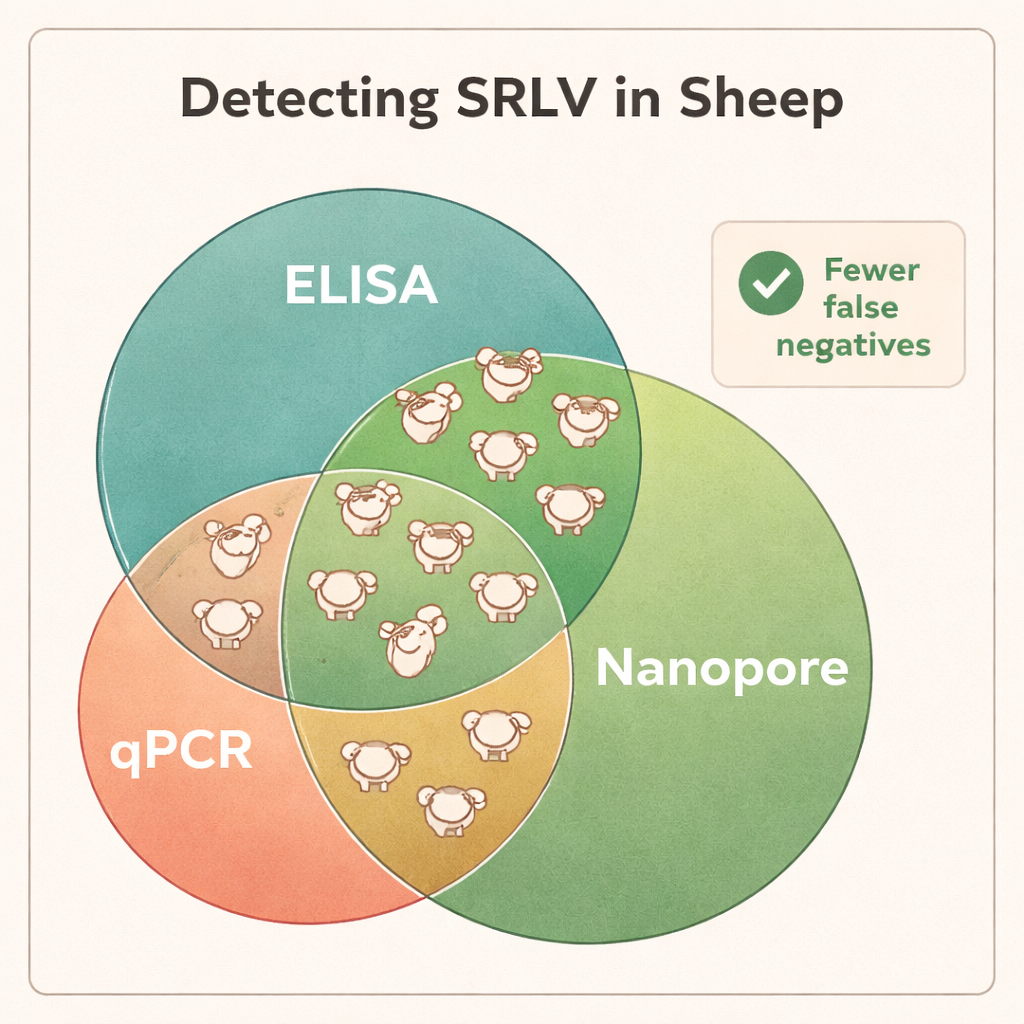
Le séquençage a montré que l’ADN du sang total était le matériau le plus fiable pour détecter les SRLV, même si le virus réside principalement dans un sous‑ensemble restreint de leucocytes. Le tissu pulmonaire provenant d’animaux fortement infectés fournissait des quantités très élevées d’ADN viral, mais de tels échantillons ne sont disponibles qu’après abattage. En revanche, les écouvillons nasaux, le sperme et les leucocytes purifiés offraient trop peu de matériel viral pour obtenir un diagnostic constant. Lorsque les scientifiques ont comparé les résultats Nanopore aux tests standard ELISA et qPCR, les différences étaient frappantes : le séquençage Nanopore a confirmé l’infection chez tous les béliers positifs à l’ELISA mais a également révélé que de nombreux animaux négatifs à l’ELISA étaient en réalité infectés. Selon les troupeaux, environ 40–45 % des animaux étiquetés « négatifs » par ELISA se sont révélés porteurs du virus, et la qPCR a manqué une fraction encore plus importante. Les données de séquençage ont aussi mis au jour des co‑infections par différents types de SRLV chez certains béliers, une information que les tests traditionnels ne fournissent pas facilement.
Du simple oui/non à des connaissances plus profondes
Parce que Nanopore lit les séquences virales elles‑mêmes, il peut aller au‑delà d’un diagnostic binaire. L’équipe a utilisé les données pour comparer les souches virales, construire des arbres généalogiques des virus circulant dans leurs troupeaux et étudier des différences subtiles dans les protéines virales qui pourraient expliquer pourquoi certains animaux échappent à la détection par les kits ELISA classiques. Ils ont montré que certaines versions d’une protéine virale clé, ciblée par les tests d’anticorps commerciaux, diffèrent notablement entre animaux anticorps‑positifs et anticorps‑négatifs. Avec le temps, ces informations pourraient aider à affiner à la fois les tests sérologiques et les programmes de sélection visant à privilégier des animaux naturellement plus résistants à l’infection.
Ce que cela signifie pour les éleveurs et la santé animale
Pour les non‑spécialistes, le message principal est simple : en lisant directement des fragments plus longs d’ADN viral, le séquençage Nanopore peut découvrir davantage de moutons infectés, plus tôt et avec plus de précision que les tests de routine actuels. Il indique aussi quelles souches virales exactes sont présentes dans un troupeau. Bien que cette approche soit encore plus complexe et coûteuse qu’un simple test sanguin, la technologie devient plus rapide, moins chère et plus portable. Si elle est intégrée aux programmes de contrôle, elle pourrait réduire fortement le nombre de porteurs « cachés », améliorer la conception de vaccins et de tests, et soutenir la sélection d’animaux plus résistants—rendant l’élevage ovin plus durable et plus respectueux du bien‑être animal.
Citation: Serrano, M., González, C., Roy, R. et al. Amplicon sequencing with Oxford nanopore technologies as a diagnostic alternative for small ruminant lentiviruses in sheep. Sci Rep 16, 6212 (2026). https://doi.org/10.1038/s41598-026-36989-y
Mots-clés: santé ovine, lentivirus, séquencage nanopore, diagnostic vétérinaire, Maedi-Visna