Clear Sky Science · fr
Évaluation de la valeur pronostique de HIST1H4C dans le cancer du sein : implications pour la thérapie néoadjuvante
Pourquoi cette recherche est importante
Pour de nombreuses femmes atteintes d’un cancer du sein, la chimiothérapie administrée avant l’intervention chirurgicale — appelée thérapie néoadjuvante — peut réduire la taille des tumeurs et rendre les opérations plus sûres et plus efficaces. Mais tout le monde n’en bénéficie pas de la même manière, et ce traitement peut entraîner des effets secondaires importants. Cette étude examine si un seul gène, nommé HIST1H4C, mesuré dans des échantillons tumoraux, peut aider les médecins à prédire qui est le plus susceptible de bien répondre à ce traitement pré-opératoire et qui pourrait présenter un risque plus élevé de récidive.
Un gène caché dans l’emballage de la tumeur
HIST1H4C appartient à une famille de gènes qui aident à empaqueter l’ADN à l’intérieur des cellules, un peu comme des bobines autour desquelles le fil est enroulé. Ces protéines « d’emballage », connues sous le nom d’histones, font plus que simplement organiser l’ADN ; elles influencent les gènes qui sont activés ou réprimés et peuvent donc moduler l’agressivité d’un cancer et sa réponse aux médicaments. Des travaux antérieurs utilisant le séquençage unicellulaire ont suggéré que HIST1H4C est particulièrement actif dans les tumeurs mammaires de haut grade — celles qui paraissent plus anormales au microscope et qui ont tendance à être plus agressives. Cela a posé une question clé : HIST1H4C pourrait-il être un marqueur faisant le lien entre l’agressivité tumorale, la réponse à la chimiothérapie et le pronostic à long terme des patientes ?
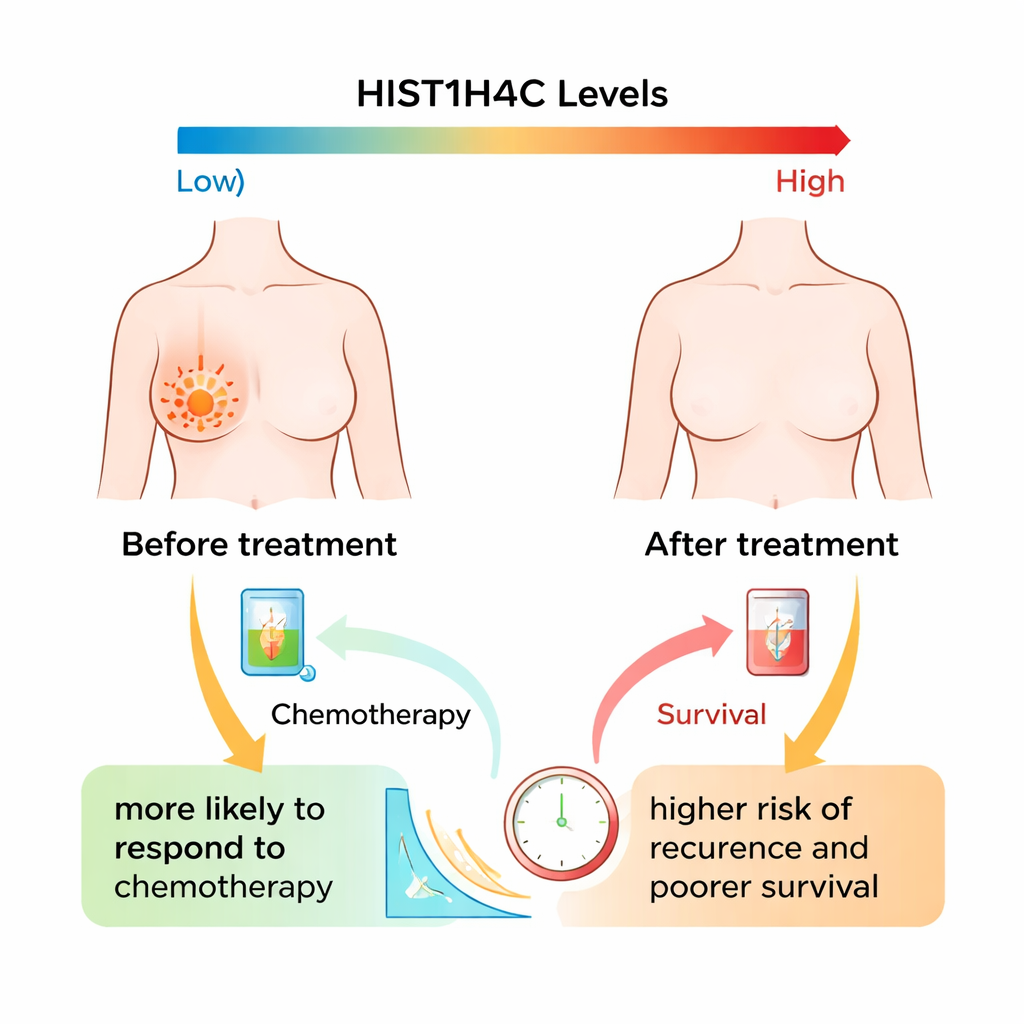
Tester les tumeurs avant et après le traitement
Les chercheurs ont suivi plus d’une centaine de femmes atteintes d’un cancer du sein de stade II ou plus, traitées dans un centre médical de Guangzhou, en Chine, entre 2019 et 2022. Toutes les patientes ont reçu une chimiothérapie néoadjuvante standard, incluant des médicaments à base d’anthracyclines et de taxanes, et certaines ont également bénéficié d’une thérapie ciblée pour les tumeurs HER2‑positives. Des échantillons tumoraux ont été prélevés avant le traitement puis à nouveau après la chirurgie. L’équipe a mesuré la quantité d’ARNm de HIST1H4C — indicateur du niveau d’expression du gène — présente dans chaque échantillon, puis a comparé ces niveaux à la qualité de la réponse tumorale, au degré de réduction (complète ou partielle) et à la durée pendant laquelle les patientes sont restées indemnes de maladie.
Un signal surprenant à deux volets
Les résultats ont révélé un schéma intriguant. Avant le traitement, les tumeurs des patientes qui ont bien répondu — celles ayant eu une régression complète ou partielle — présentaient en réalité des niveaux de HIST1H4C plus élevés que celles des mauvaises répondantes. Autrement dit, des niveaux initiaux plus élevés de ce gène étaient associés à une plus grande sensibilité à la chimiothérapie, même si ces tumeurs présentaient souvent d’autres caractéristiques à haut risque comme la négativité des récepteurs hormonaux, une implication ganglionnaire plus importante et un statut triple négatif. Après le traitement, toutefois, l’histoire s’est inversée : les patientes dont les tumeurs présentaient encore des niveaux élevés de HIST1H4C avaient tendance à conserver des résidus tumoraux plus importants et à présenter une survie sans progression plus courte. Dans l’ensemble, les niveaux de HIST1H4C ont généralement diminué après la thérapie, mais cette baisse a été beaucoup plus marquée chez les bonnes répondantes que chez les mauvaises répondantes.
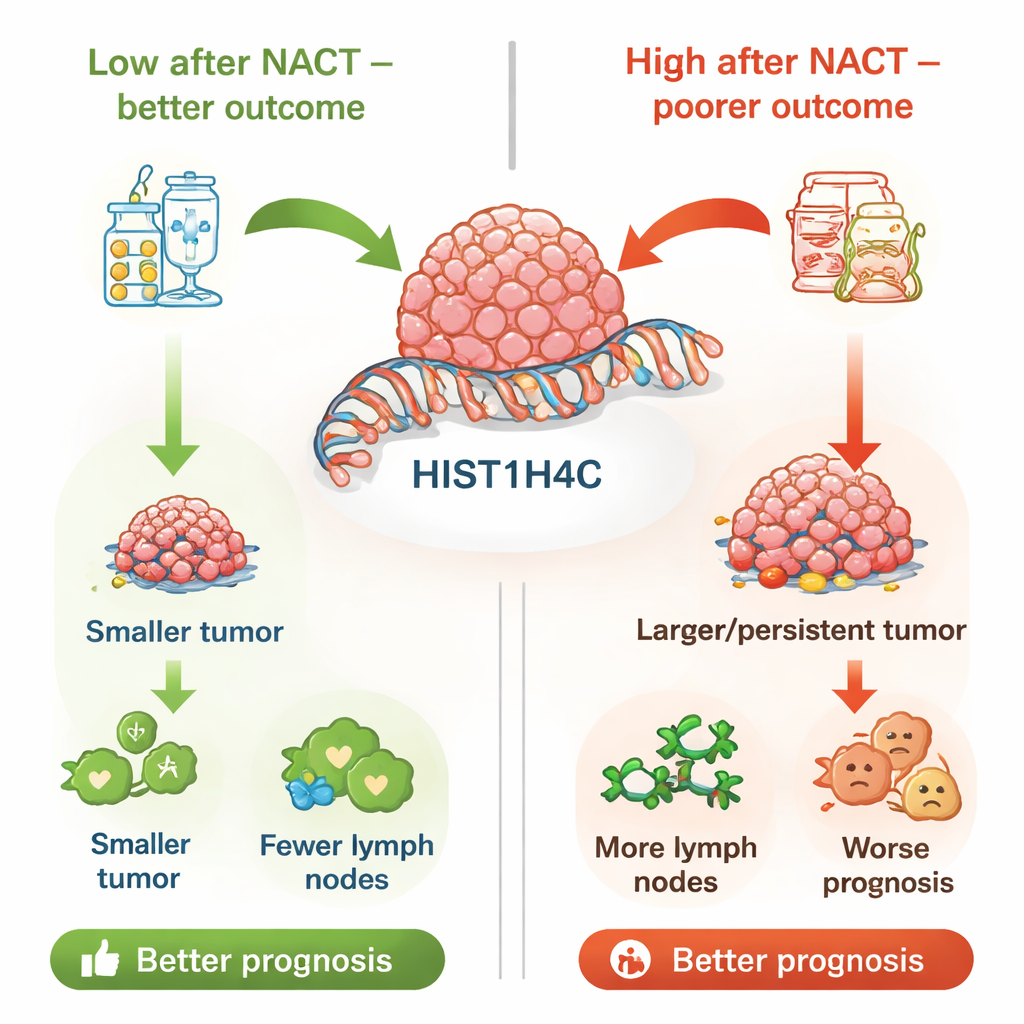
Relier les niveaux du gène au pronostic à long terme
Pour vérifier si ces observations tenaient dans un contexte plus large, les auteurs ont analysé des données d’une grande base publique sur le cancer du sein connue sous le nom de base de données Curtis. Là aussi, une forte expression de HIST1H4C était associée à un grade tumoral plus avancé, à des tumeurs plus volumineuses, à davantage de métastases ganglionnaires et à des types tumoraux défavorables tels que les cancers triple négatifs et les cancers négatifs pour les récepteurs hormonaux. Plus important encore, les patientes présentant des niveaux élevés de HIST1H4C dans cet ensemble externe avaient des survies plus courtes. Ensemble, la cohorte hospitalière et l’analyse à grande échelle convergent vers HIST1H4C comme marqueur de maladie plus agressive et de pronostic plus défavorable, en particulier lorsque ses niveaux restent élevés après le traitement.
Vers des décisions thérapeutiques mieux ajustées
Pour le grand public, le message essentiel est qu’un test de laboratoire simple mesurant HIST1H4C dans le tissu tumoral pourrait un jour aider les médecins à mieux adapter la thérapie néoadjuvante à la patiente. Un niveau élevé de HIST1H4C avant le traitement pourrait signaler des cancers agressifs mais susceptibles de régresser sous chimiothérapie, tandis qu’un maintien de niveaux élevés après le traitement pourrait indiquer un risque accru de rechute et la nécessité d’un suivi plus étroit ou de traitements complémentaires. Comme le test repose sur des méthodes d’expression génique standard déjà courantes dans de nombreux hôpitaux, les auteurs soutiennent qu’il pourrait constituer un outil pratique et économique, notamment dans les contextes à ressources limitées. Bien qu’une validation supplémentaire soit nécessaire, ce travail suggère que l’analyse de « l’emballage » de l’ADN tumoral peut fournir des indices puissants sur les cancers du sein qui répondront au traitement préopératoire et sur l’évolution probable des patientes à long terme.
Citation: Qian, L., Ge, R., Haihu, Z. et al. Evaluating the prognostic significance of HIST1H4C in breast cancer: implications for neoadjuvant therapy. Sci Rep 16, 6792 (2026). https://doi.org/10.1038/s41598-026-36983-4
Mots-clés: cancer du sein, chimiothérapie néoadjuvante, biomarqueurs, HIST1H4C, réponse au traitement