Clear Sky Science · fr
Nanoparticules antimicrobiennes à large spectre et faible toxicité pour prévenir la formation de biofilms sur les dispositifs urologiques
Pourquoi les implants médicaux se retournent parfois contre nous
La médecine moderne repose sur des tubes et des implants en plastique pour drainer l’urine, soutenir des reins obstrués et restaurer la fonction sexuelle. Pourtant, ces mêmes dispositifs peuvent attirer les bactéries, qui forment des communautés protectrices visqueuses appelées biofilms. Une fois qu’un biofilm s’installe, les infections sont difficiles à traiter, obligeant souvent les médecins à retirer ou remplacer le dispositif. Cette étude explore un nouveau type de revêtement microscopique, composé d’or et d’argent enveloppés dans une coque de carbone, conçu pour empêcher la formation de biofilms dès le départ.
Le problème caché des germes adhérents
Les cathéters, les stents urétéraux et les prothèses péniennes gonflables aident des centaines de milliers de patients, mais ils offrent aussi un terrain idéal pour les microbes. Les bactéries s’attachent à la surface du dispositif et sécrètent une matrice collante de sucres, de protéines et de lipides, formant une forteresse qui les protège des antibiotiques et du système immunitaire. En conséquence, les infections liées aux dispositifs représentent plus d’un quart des infections nosocomiales et coûtent des centaines de millions de dollars chaque année. Les revêtements actuels à base d’antibiotiques ou d’argent simple peinent à prévenir durablement les biofilms et peuvent contribuer à l’augmentation de la résistance aux antibiotiques.
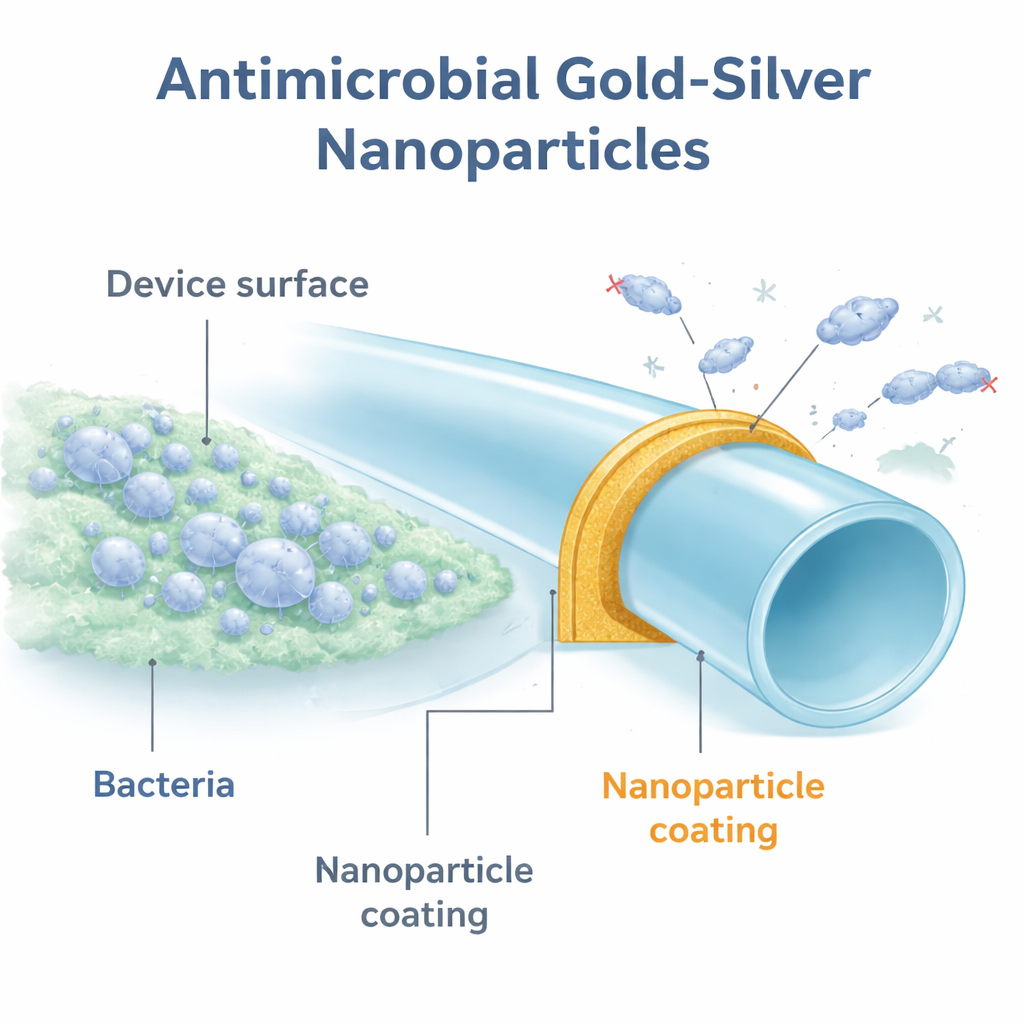
Une nouvelle sorte d’armure protectrice
Les chercheurs se sont concentrés sur de minuscules particules métalliques de seulement quelques milliardièmes de mètre de largeur. Ces nanoparticules ont été construites autour d’un matériau en cage de carbone appelé polyhydroxy fullerène, connu pour être non toxique et pour améliorer les performances de certains métaux. Ils ont créé plusieurs variantes avec différents métaux, puis ont enduit de petits disques de polyuréthane, un plastique couramment utilisé dans les dispositifs urologiques. Lors des tests contre une souche standard d’Escherichia coli, seules les particules contenant de l’argent ont montré de forts effets antibactériens. Le meilleur résultat est venu d’une combinaison or–argent, appelée GSNPs, qui a réduit le nombre de bactéries jusqu’à 100 000 fois par rapport au plastique non revêtu.
Arrêter les germes urologiques du monde réel
Pour vérifier si cet effet se confirmait au-delà d’une souche de laboratoire, l’équipe a testé son meilleur revêtement contre six types de bactéries prélevées directement sur des stents urétéraux et des prothèses péniennes infectés. Il s’agissait d’espèces à Gram positif et Gram négatif connues pour provoquer des infections tenaces. À des concentrations bactériennes similaires à celles observées chez les patients, les surfaces revêtues de GSNP ont obtenu une réduction de 100 % des bactéries à la fois en suspension et attachées à la surface pour chaque souche testée. Dans des expériences séparées, les chercheurs ont exposé les bactéries à différentes concentrations de nanoparticules en solution et estimé la quantité de GSNP nécessaire pour arrêter la croissance. Toutes les souches ont été complètement inhibées à 3 microgrammes de GSNP par millilitre de solution ou moins, certaines espèces à Gram positif nécessitant des quantités légèrement supérieures.
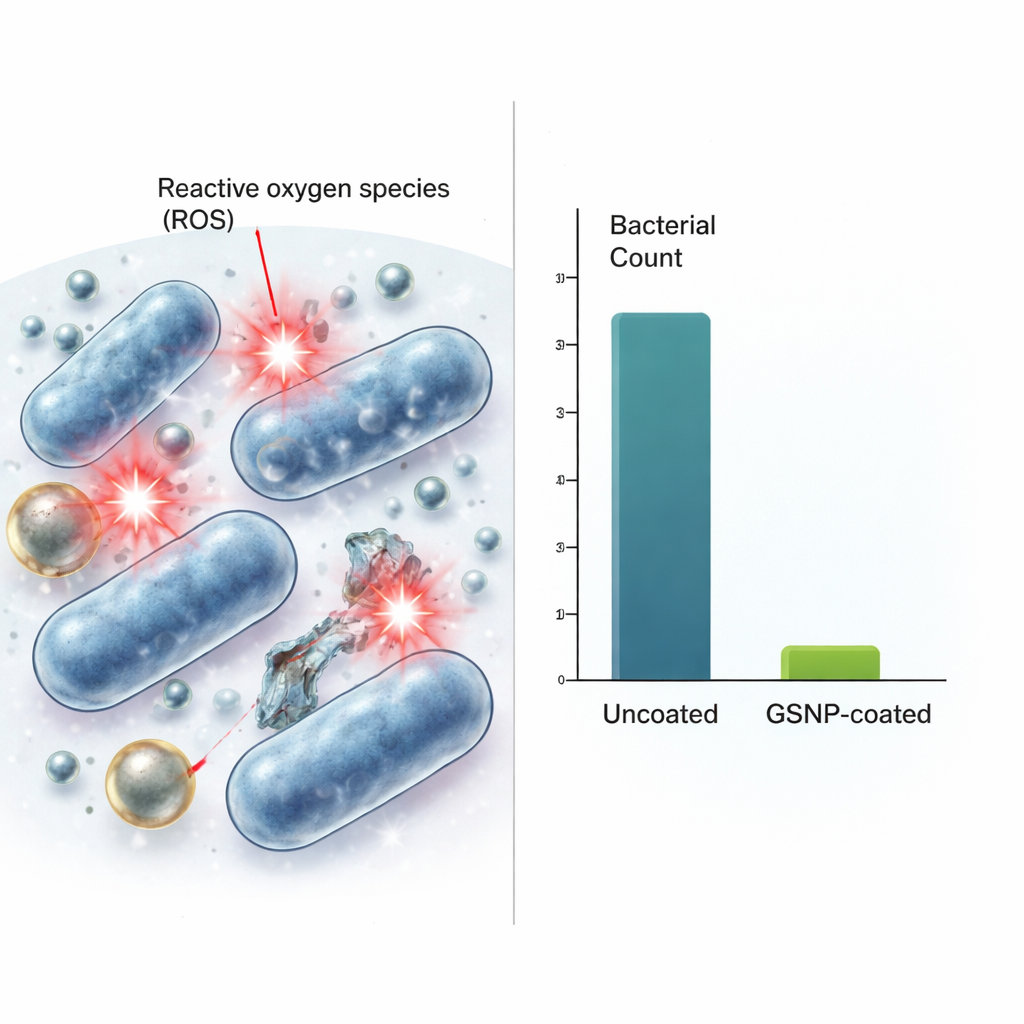
Comment elles agissent et quel est leur niveau de sécurité
L’équipe a ensuite examiné comment ces revêtements tuent les bactéries et s’ils pourraient aussi nuire aux cellules humaines. Leurs données indiquent que des espèces réactives de l’oxygène — des formes chimiquement réactives de l’oxygène — constituent une partie clé du mécanisme de destruction. Si les nanoparticules seules ne génèrent pas ces molécules réactives, les bactéries exposées aux GSNP ont produit des niveaux beaucoup plus élevés que les bactéries non traitées, ce qui suggère que les particules déclenchent une chimie dommageable à l’intérieur ou à proximité des microbes. Lorsque des cellules de fibroblastes de souris ont été exposées à des concentrations de GSNP similaires ou supérieures à la dose antibactérienne, plus de 80 % des cellules sont restées viables au pire des cas. Autrement dit, les niveaux qui éliminent les bactéries n’avaient qu’un impact modéré sur les cellules des mammifères. Les GSNP se sont également révélés nettement plus efficaces qu’un produit commercial de nanoparticules or–argent testé en parallèle, obtenant environ un million de fois plus de réduction bactérienne à doses équivalentes.
Ce que cela pourrait signifier pour les patients
Bien que ces travaux aient été réalisés en laboratoire et pas encore chez l’animal ou l’humain, les résultats indiquent une stratégie prometteuse pour des implants médicaux plus sûrs. Une fine couche de GSNP sur un cathéter ou une prothèse pourrait offrir une protection large contre de nombreuses bactéries, réduire la nécessité de retirer un dispositif, et ce sans recourir aux antibiotiques traditionnels. Le revêtement utilise de faibles quantités de métal, montre une toxicité relativement faible dans les premiers tests et est simple à fabriquer. Avec des améliorations d’ingénierie pour la stabilité à long terme et des essais rigoureux dans des modèles réalistes, ces revêtements de nanoparticules or–argent pourraient aider à maintenir en fonctionnement les dispositifs urologiques essentiels pour les patients plutôt que de devenir une base d’infection.
Citation: Rodriguez-Alvarez, J.S., Xu, Y., Gutierrez-Aceves, J. et al. Broad spectrum antimicrobial nanoparticles with low toxicity to prevent biofilm formation on urologic devices. Sci Rep 16, 7333 (2026). https://doi.org/10.1038/s41598-026-36969-2
Mots-clés: biofilm, dispositifs urologiques, revêtement antimicrobien, nanoparticules, or-argent