Clear Sky Science · fr
Analyse protéomique quantitative du plasma après conditionnement ischémique à distance en cas d'accident ischémique aigu
Pourquoi comprimer un bras pourrait aider à protéger le cerveau
Lorsqu'une personne fait un AVC dû à l'obstruction d'un vaisseau sanguin, chaque minute de perte d'apport sanguin met en danger les cellules cérébrales. Les traitements standards visent à rouvrir l'artère bouchée, mais de nombreux patients arrivent trop tard ou ne sont pas éligibles. Les chercheurs explorent une thérapie additionnelle étonnamment simple : interrompre brièvement le flux sanguin vers un bras ou une jambe à l'aide d'un brassard de tension artérielle, une stratégie appelée conditionnement ischémique à distance (RIC). Cette étude pose une question cruciale pour transformer cette idée en thérapie réelle : que change exactement le RIC dans le sang des patients ayant eu un AVC, et ces changements pourraient-ils indiquer qui bénéficierait le plus?
Un signal de stress léger envoyé du membre vers le cerveau
Le RIC consiste à gonfler et dégonfler à plusieurs reprises un brassard sur un membre pendant quelques minutes, créant de courtes et inoffensives périodes de faible circulation. Des expériences animales et des essais cliniques précoces suggèrent que ce « stress contrôlé » peut envoyer des signaux à des organes distants, y compris le cerveau, pour activer des programmes protecteurs. Dans un grand essai clinique appelé RICAMIS, des patients atteints d'un AVC ischémique modéré ayant reçu le RIC en plus des soins habituels ont présenté de meilleurs résultats à 90 jours que ceux ayant reçu uniquement les soins habituels. Un autre essai (RESIST) n'a cependant pas observé ce bénéfice, laissant les cliniciens incertains quant au moment et aux patients pour lesquels le RIC fonctionne réellement. L'étude en cours analyse le sang des patients à la recherche d'indices moléculaires : des protéines mesurables, ou biomarqueurs, qui évoluent au fil du temps sous l'effet du RIC.
Suivre le sang des patients pendant leur hospitalisation
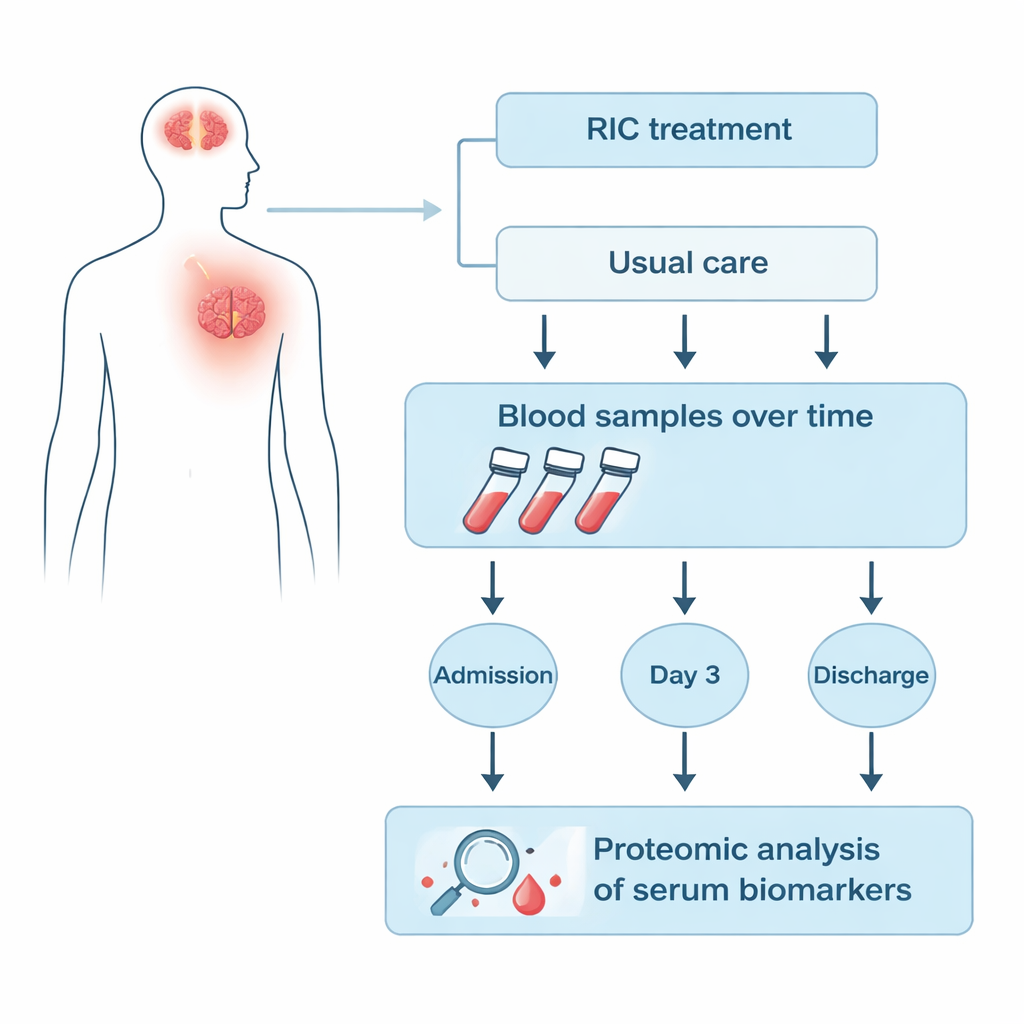
Les chercheurs se sont concentrés sur 25 patients de l'essai RICAMIS qui avaient des échantillons sanguins prélevés à trois moments : à l'admission, trois jours après l'attribution du traitement et à la sortie de l'hôpital. Neuf patients ont reçu le RIC en plus des soins habituels, tandis que seize ont reçu uniquement les soins habituels. À l'aide d'une technique appelée protéomique quantitative, l'équipe a mesuré simultanément des centaines de protéines dans la fraction sérique du sang, plutôt que d'examiner seulement quelques marqueurs pré-sélectionnés. Ils ont ensuite comparé comment le niveau de chaque protéine augmentait ou diminuait au fil du temps dans le groupe RIC par rapport au groupe témoin pour identifier des signatures spécifiquement liées au RIC.
Neuf signaux marquants dans la circulation sanguine
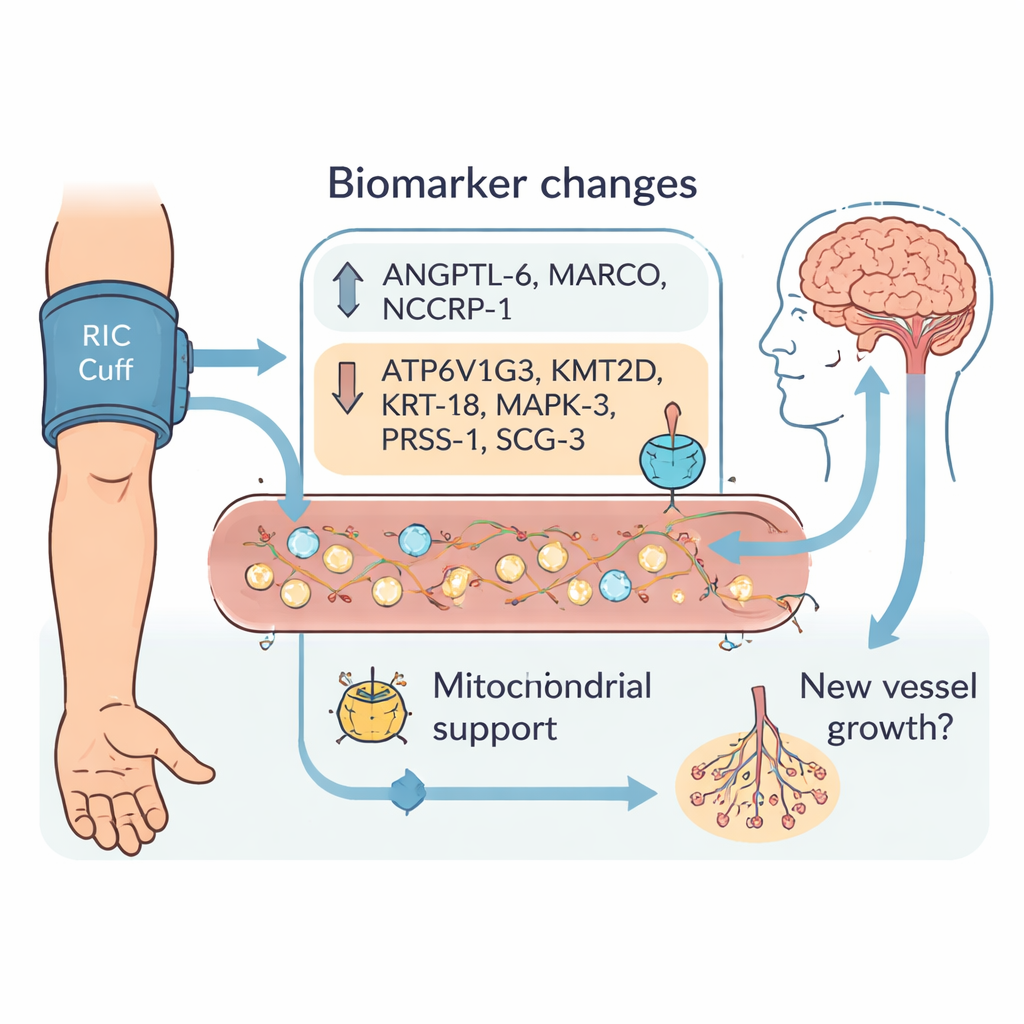
Au cours de l'hospitalisation, des dizaines de protéines ont évolué différemment entre les deux groupes. Après un filtrage attentif, l'équipe a mis en évidence neuf biomarqueurs dont les variations entre l'admission, le jour 3 et la sortie séparaient clairement les patients traités par RIC des témoins. Trois protéines — ANGPTL‑6, MARCO et NCCRP‑1 — ont augmenté davantage avec le RIC. Six autres — ATP6V1G3, KMT2D, KRT‑18, MAPK‑3, PRSS‑1 et SCG‑3 — ont eu tendance à diminuer. Bon nombre de ces molécules participent à la gestion de l'énergie au sein des mitochondries, les petites centrales énergétiques des cellules, ou à la croissance et au remodelage des nouveaux vaisseaux. Cela correspond à l'idée selon laquelle le RIC ne se contente pas de protéger les neurones de la lésion, mais pourrait aider les régions cérébrales blessées à se réorganiser, à réparer leur vascularisation et à récupérer des fonctions sur des jours à des semaines.
Indices sur l'utilisation d'énergie et la néovascularisation
Pour mieux comprendre le rôle possible de ces neuf protéines, les auteurs les ont cartographiées dans des voies biologiques connues. Deux d'entre elles, KMT2D et MAPK‑3, sont reliées à la façon dont l'ADN est emballé et à la régulation de l'expression des gènes, notamment dans des programmes liés à la croissance vasculaire. D'autres, comme ATP6V1G3 et KRT‑18, ont été associées dans des travaux antérieurs au maintien de mitochondries saines et à la protection du tissu cardiaque après une lésion. Ensemble, ces profils suggèrent que le RIC oriente l'organisme vers une utilisation plus efficace de l'énergie et favorise la croissance ou le remodelage des vaisseaux sanguins — améliorant potentiellement la circulation autour de la zone endommagée par l'AVC. Parallèlement, certains marqueurs, tels que NCCRP‑1 et MARCO, peuvent refléter la réponse aiguë au stress et la réponse immunitaire déclenchées par la procédure de gonflage du brassard, soulignant que le RIC provoque une réaction corporelle complexe et systémique.
Ce que cela signifie pour la prise en charge future des AVC
Cette petite étude exploratoire ne peut pas prouver exactement comment le RIC protège le cerveau, et elle a porté sur seulement 25 patients d'un seul pays, si bien que les résultats doivent être confirmés dans des cohortes beaucoup plus nombreuses et diversifiées. Néanmoins, l'identification d'une courte liste de neuf protéines qui évoluent de façon contraire selon la présence ou l'absence de RIC constitue une étape importante. À l'avenir, ces biomarqueurs pourraient aider les médecins à déterminer rapidement si le RIC a « pris effet » chez un patient donné, guider le choix des candidats au traitement, ou même inspirer des médicaments reproduisant ses effets bénéfiques sans le brassard. Pour l'instant, ce travail renforce une idée simple mais puissante : en soumettant en sécurité une partie du corps à un stress contrôlé, on peut encourager le cerveau à devenir plus résilient et mieux à même de guérir après un AVC.
Citation: Cui, Y., Liu, F., Cai, JR. et al. Quantitative proteomic analysis of plasma after remote ischemic conditioning in acute ischemic stroke. Sci Rep 16, 6106 (2026). https://doi.org/10.1038/s41598-026-36968-3
Mots-clés: accident ischémique aigu, conditionnement ischémique à distance, biomarqueurs sériques, analyse protéomique, neuroprotection