Clear Sky Science · fr
Anomalies rénales fœtales structurelles et fonctionnelles comme mécanisme de l’oligoamnios dans un modèle de restriction de croissance chez le cobaye
Pourquoi l’eau de l’utérus compte
Tard dans la grossesse, le fœtus baigne dans un liquide protecteur qui amortit les mouvements et reflète son état de santé. Quand ce réservoir diminue trop — une condition appelée faible volume de liquide amniotique — cela signale un problème et augmente le risque de complications à la naissance. Les cliniciens savent que les petits fœtus atteints de restriction de croissance ont souvent trop peu de liquide, mais la cause précise était restée floue. Cette étude, réalisée chez des cobayes gravides, montre que, au‑delà des problèmes placentaire et circulatoire, les reins du fœtus peuvent être endommagés structurellement, réduisant la production d’urine et contribuant à l’assèchement de ce réservoir vital.
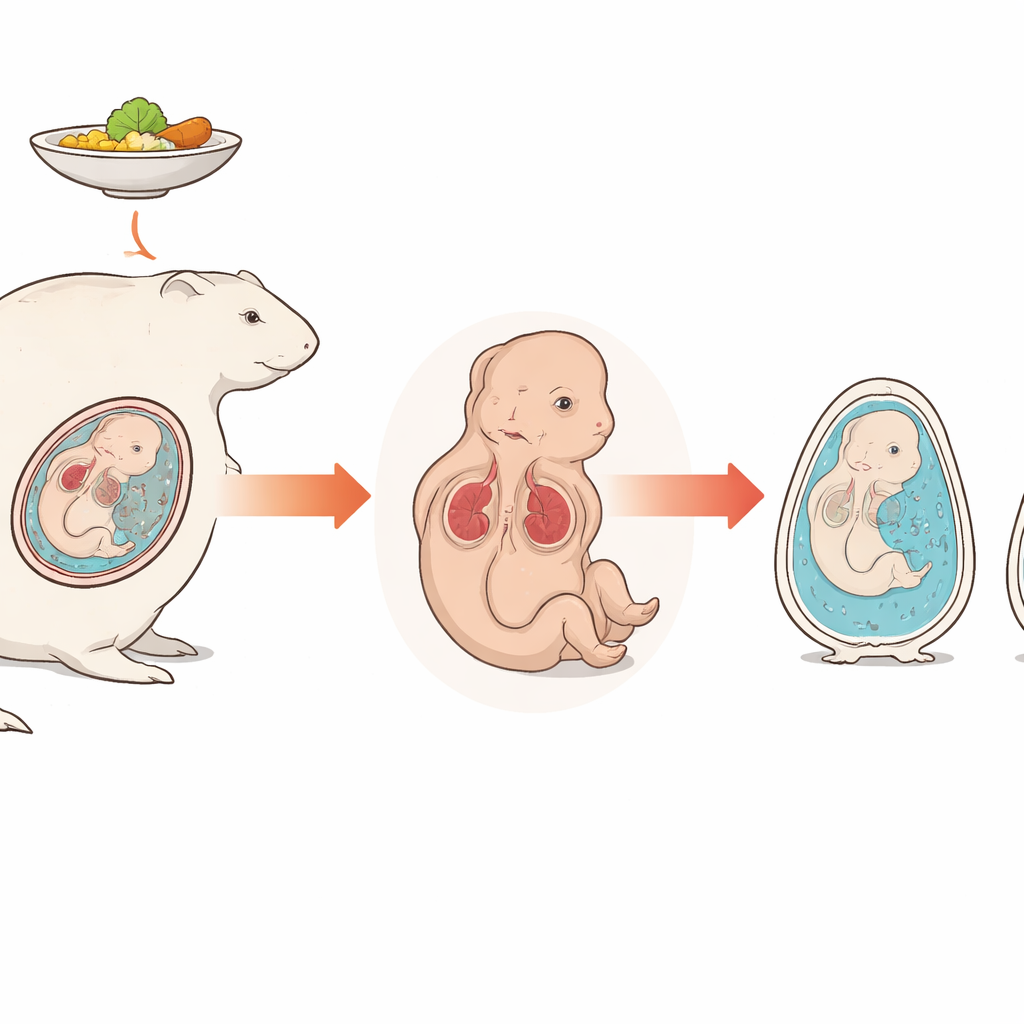
Petits fœtus et diminution du volume de liquide
Les chercheurs ont mis au point un modèle de mauvaise croissance fœtale en limitant modérément l’alimentation des cobayes gravides. Par rapport aux mères bien nourries, les mères sous‑alimentées avaient des fœtus et des placentas plus petits, reproduisant la restriction de croissance humaine. Fait essentiel, le volume de liquide entourant ces fœtus a chuté d’environ moitié, même en tenant compte de leur poids corporel plus faible. Comme la majeure partie du liquide amniotique en fin de grossesse provient de l’urine fœtale, cette baisse nette suggère que le problème provient du fonctionnement rénal fœtal, et pas seulement d’un apport sanguin réduit.
Examen des petits reins au microscope
Pour savoir ce qui se passait au niveau tissulaire, l’équipe a examiné les reins fœtaux au microscope. Chez les fœtus bien développés, les unités de filtration et les petits tubules collecteurs étaient bien organisés et intacts. En revanche, chez les fœtus en restriction de croissance, le tissu rénal présentait des signes évidents de lésion : les tubules étaient aplatis et enflés, les cellules avaient perdu leur noyau et des débris s’étaient accumulés à l’intérieur des espaces tubulaires. L’imagerie en forte résolution a montré que des cellules clés du filtre à la surface des glomérules s’étaient amincies ou étaient disparues, et que les membranes de soutien des filtres et des tubules étaient effilochées ou rompues. Ensemble, ces altérations indiquent des filtres qui fuient et des tubules incapables de réabsorber correctement l’eau et d’autres substances utiles.
Indices chimiques dans le liquide environnant
L’équipe a également recherché dans le liquide amniotique des empreintes chimiques de lésion rénale. Ils ont mesuré trois protéines qui, normalement, sont exclues de l’urine ou réabsorbées par des tubules sains. Dans le groupe en restriction de croissance, les trois étaient sensiblement plus élevées après ajustement sur la créatinine, méthode standard pour corriger la concentration. L’albumine élevée suggère que les filtres rénaux laissent passer des protéines. Les taux accrus de cystatine C et d’une protéine appelée L‑FABP indiquent des cellules tubulaires stressées et lésées, dépassées par leur charge de travail. Les tests sanguins fœtaux montraient une urée augmentée, autre signe d’une fonction rénale globale mise à l’épreuve, même si un marqueur plus stable, la créatinine, n’était pas encore élevé.
Des reins qui réagissent au stress
Au‑delà des dommages structurels, les chercheurs ont cherché des signes d’inflammation et de réparation dans les reins. Ils ont trouvé des quantités accrues de deux messagers immunitaires, IL‑6 et IL‑10, et l’activation d’une protéine de signalisation en aval, STAT3, surtout dans les tubules rénaux. Dans d’autres maladies rénales, ces signaux peuvent jouer un rôle protecteur, aidant les tissus à faire face aux blessures. Leur présence ici suggère que les reins fœtaux ne sont pas seulement endommagés par la sous‑nutrition et la réduction d’oxygène, mais qu’ils déclenchent aussi une réponse biologique susceptible de limiter ou de remodeler les lésions, avec des conséquences inconnues après la naissance.
Ce que cela signifie pour les grossesses à risque
Pris ensemble, ces résultats dessinent un tableau dans lequel le faible volume de liquide amniotique dans les grossesses avec restriction de croissance n’est pas simplement la conséquence d’un moindre apport sanguin aux reins. Les reins eux‑mêmes sont compromis structurellement et fonctionnellement : ils filtrent et gèrent l’urine moins efficacement, et la production d’urine globale diminue. Les mêmes molécules qui ont fuité dans le liquide entourant les fœtus de cobayes pourraient servir de signaux d’alerte précoces chez l’humain, aidant les cliniciens à identifier les fœtus dont les reins sont en souffrance. En fin de compte, reconnaître le rôle du rein fœtal — et pas seulement du placenta — dans le faible volume de liquide amniotique pourrait ouvrir la voie à de nouvelles approches pour surveiller et protéger les grossesses vulnérables.
Citation: Inatomi, A., Katsura, D., Tokoro, S. et al. Structural and functional foetal renal abnormalities as a mechanism of oligohydramnios in a guinea pig model of growth restriction. Sci Rep 16, 8285 (2026). https://doi.org/10.1038/s41598-026-36964-7
Mots-clés: restriction de croissance fœtale, liquide amniotique, lésion rénale, sous‑alimentation maternelle, complications de la grossesse