Clear Sky Science · fr
Analyse du protéome et du phosphoprotéome basée sur Orbitrap Astral identifie des protéines candidates associées à la phosphatidate phosphatase MoPah1 chez Magnaporthe oryzae
Pourquoi l’enzyme d’une maladie du riz compte
Le riz est un aliment de base pour des milliards de personnes, pourtant un seul champignon microscopique, Magnaporthe oryzae, provoque la maladie de la brûlure du riz qui peut ravager des parcelles entières. Cette étude explore la chimie interne de ce champignon, en se concentrant sur une enzyme, MoPah1, qui régule les lipides et les molécules de signalisation de la cellule. En cartographiant des milliers de protéines et leurs interrupteurs biochimiques, les chercheurs révèlent comment cette enzyme relie le métabolisme fondamental à la capacité du champignon d’infecter les plants de riz.
Un champignon qui infiltre les plants de riz
Magnaporthe oryzae infecte les feuilles de riz à l’aide d’une structure spécialisée appelée appressorium, qui accumule une énorme pression interne pour percer la surface foliaire. Pour alimenter ce processus, le champignon dépense rapidement ses réserves de sucres et de lipides. Des travaux antérieurs ont montré que MoPah1, une enzyme qui convertit une molécule grasse appelée acide phosphatidique en diacylglycérol, est essentielle à ce mode de vie : la suppression du gène MoPah1 affaiblit le champignon et réduit sa capacité à provoquer la maladie. Mais quelles autres protéines sont liées à MoPah1, et comment cette enzyme s’intègre dans des réseaux cellulaires plus larges, restait inconnu.
Utiliser une cartographie protéique de nouvelle génération
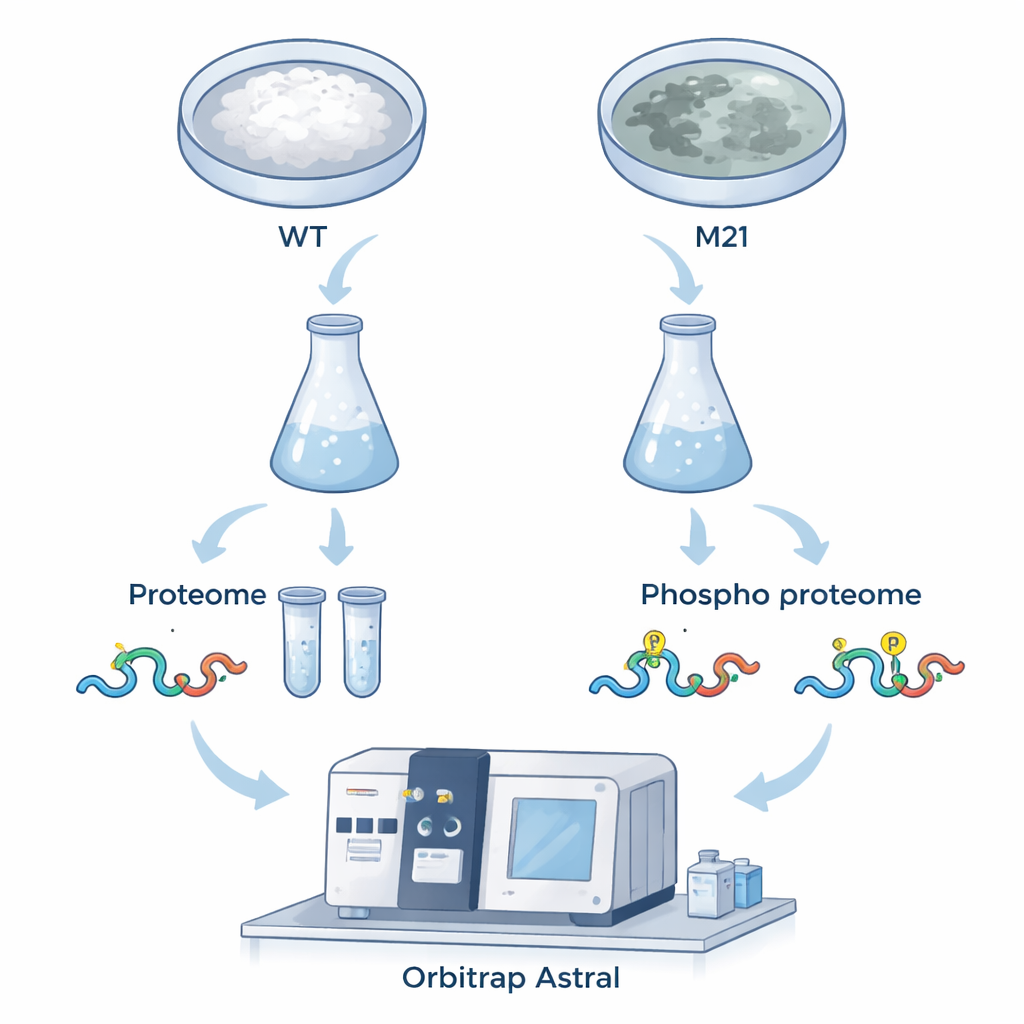
Pour répondre à ces questions, l’équipe a comparé des champignons normaux à un mutant dépourvu de MoPah1. Ils se sont concentrés sur la croissance filamenteuse (mycélium), car le mutant ne peut pas produire les spores habituellement utilisées pour les études d’infection. À l’aide d’un spectromètre de masse avancé appelé Orbitrap Astral et d’une stratégie d’acquisition indépendante des données (DIA), ils ont mesuré à la fois l’abondance des protéines et la présence de marques de phosphorylation qui fonctionnent comme des interrupteurs moléculaires. Au total, ils ont identifié 6 799 protéines et plus de 15 000 sites de phosphorylation, dont des centaines montraient des augmentations ou des diminutions nettes chez le mutant. Cet ensemble de données vaste et de haute qualité offre un instantané détaillé de la manière dont la suppression de MoPah1 transforme la cellule fongique.
Des changements dans l’utilisation de l’énergie et le recyclage cellulaire
Lorsque les chercheurs ont examiné les types de protéines modifiées, deux thèmes se sont distingués : le métabolisme des lipides membranaires et un processus d’« auto‑digestion » appelé autophagie, que les cellules utilisent pour recycler des composants et survivre au stress. De nombreuses protéines impliquées dans les glycérophospholipides — les éléments constitutifs des membranes cellulaires — et dans des voies énergétiques associées ont été altérées. Les protéines liées à l’autophagie ont présenté des changements particulièrement marqués dans leurs profils de phosphorylation, suggérant que MoPah1 affecte non seulement la synthèse et la dégradation des lipides, mais aussi la manière dont le champignon recycle son propre matériel pendant la croissance et l’infection. Un sous‑ensemble de 72 protéines a changé à la fois en quantité et en état de phosphorylation, les désignant comme des candidats privilégiés pour un contrôle direct ou indirect par MoPah1.
À la recherche des partenaires protéiques de MoPah1
Pour aller au‑delà des corrélations, l’équipe a cherché quelles protéines se lient physiquement à MoPah1. Ils ont produit une protéine MoPah1 fusionnée à une « poignée » (GST) dans des bactéries, puis l’ont utilisée comme appât pour récupérer des protéines interagissant depuis des extraits fongiques. La spectrométrie de masse a identifié 183 candidats, dont beaucoup s’organisent en grands complexes protéiques, renforçant l’idée que MoPah1 occupe une position centrale au sein de vastes réseaux cellulaires. Parmi ces partenaires, un s’est distingué : Pmk1, une protéine de signalisation clé de la voie MAPK qui contrôle la formation de l’appressorium, la croissance à l’intérieur de la plante et les réponses au stress. Des tests complémentaires de type levure deux‑hybrides ont confirmé que MoPah1 et Pmk1 peuvent interagir directement.
Relier le contrôle des lipides aux signaux d’infection
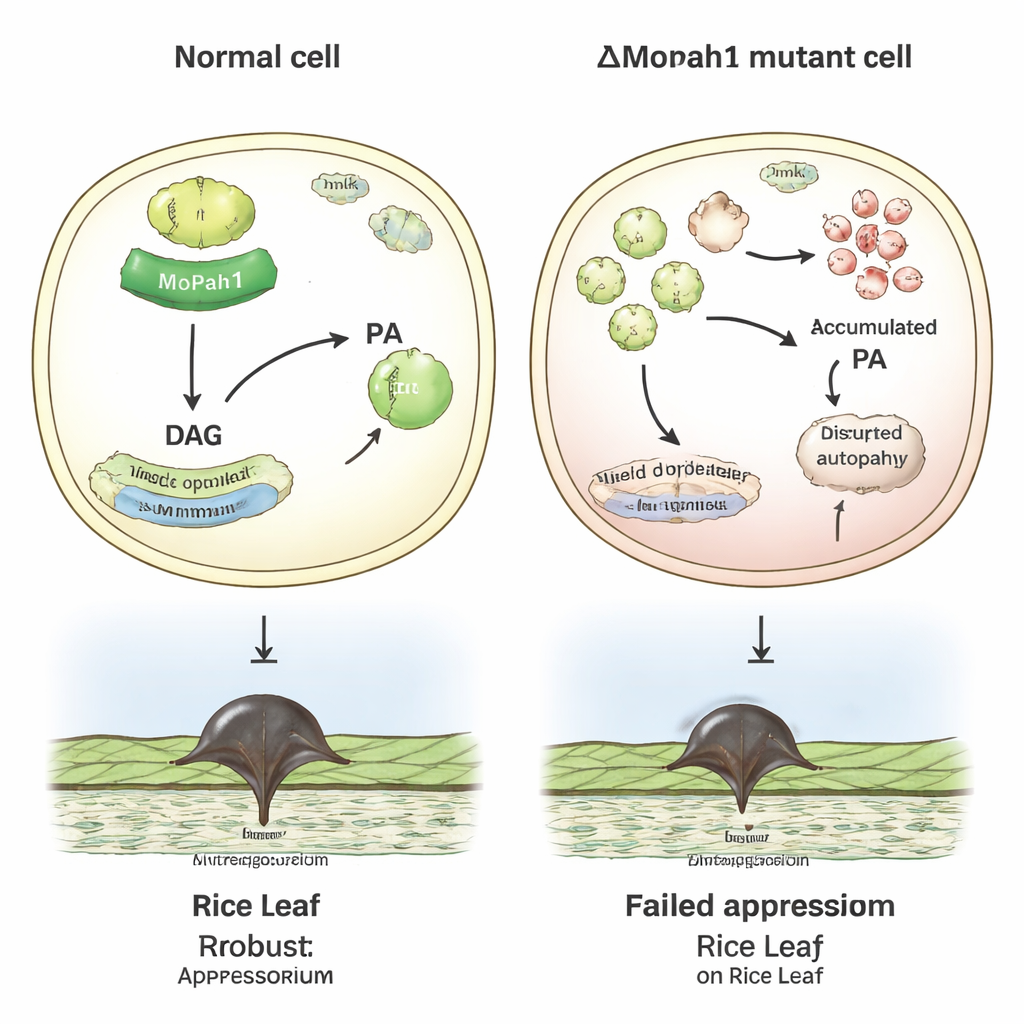
En réunissant ces éléments, les auteurs proposent que MoPah1 contribue à ajuster à la fois l’équilibre des lipides membranaires et les grandes voies de signalisation chez Magnaporthe oryzae. Chez les champignons dépourvus de MoPah1, de larges perturbations du métabolisme lipidique, du recyclage des protéines et de la signalisation MAPK semblent compromettre la formation et l’efficacité des structures d’infection nécessaires pour pénétrer les feuilles de riz. Bien que l’étude se soit limitée aux échantillons mycéliens — car le mutant ne peut pas former de spores — elle fournit néanmoins une riche ressource de données protéiques et de phosphorylation, ainsi qu’une liste restreinte de protéines les plus susceptibles d’agir aux côtés de MoPah1. Pour les non‑spécialistes, l’essentiel est que la régulation d’une seule enzyme chez un pathogène des cultures peut avoir des répercussions sur de nombreux systèmes cellulaires, offrant de nouveaux angles pour comprendre, et peut‑être un jour perturber, le champignon qui menace l’une des sources alimentaires les plus importantes au monde.
Citation: Zhao, J., Yang, L., Shi, X. et al. Orbitrap Astral–based proteome and phosphoproteome analysis identifies candidate proteins associated with the phosphatidate phosphatase MoPah1 in Magnaporthe oryzae. Sci Rep 16, 6901 (2026). https://doi.org/10.1038/s41598-026-36940-1
Mots-clés: champignon responsable de la brûlure du riz, Magnaporthe oryzae, réseaux protéiques, métabolisme des lipides, pathogénicité fongique