Clear Sky Science · fr
Une sous-population neutrophile pro-inflammatoire provoque une lésion d'ischémie–reperfusion intestinale via la voie du stress du réticulum endoplasmique médiée par ATF4
Quand la reprise du flux sanguin blesse l’intestin
Chirurgiens et réanimateurs se heurtent depuis longtemps à un paradoxe dangereux : lorsque l’apport sanguin à l’intestin est interrompu puis rétabli, c’est souvent la restauration de la circulation qui endommage sévèrement la muqueuse intestinale. Ce phénomène, appelé lésion d’ischémie–reperfusion intestinale, peut entraîner des complications mortelles comme la septicémie et l’insuffisance multiorganique. L’étude résumée ici montre que tous les globules blancs qui affluent sur le site ne se valent pas : une sous‑population particulièrement agressive joue un rôle majeur en faisant basculer une réponse salvatrice en un processus délétère.
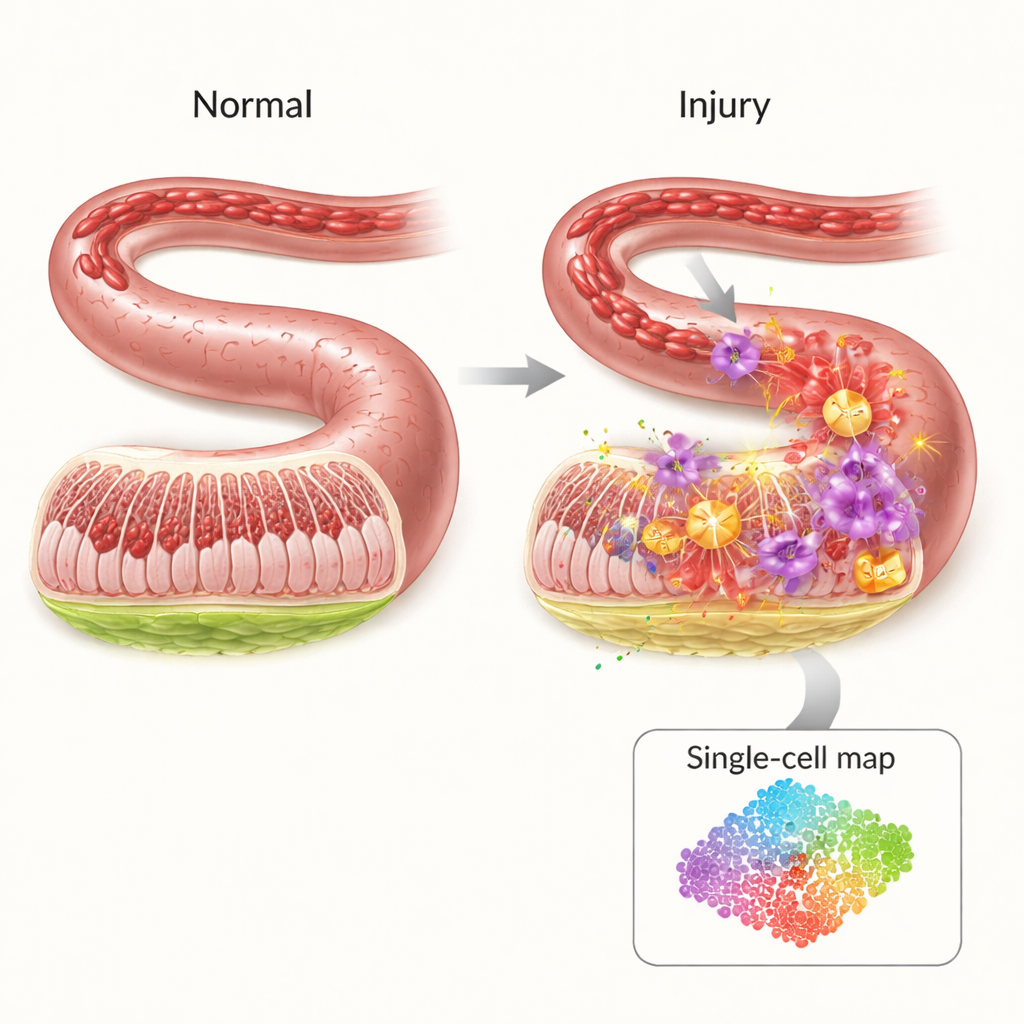
La paroi protectrice fragile de l’intestin
L’intérieur de l’intestin est tapissé d’une barrière mince mais hautement organisée qui maintien les bactéries et les toxines dans la lumière intestinale tout en laissant passer les nutriments. Lorsqu’un apport sanguin est interrompu — par exemple lors d’un choc, d’une chirurgie majeure ou d’un traumatisme sévère — cette barrière est privée d’oxygène. De façon contre‑intuitive, la majeure partie des dégâts survient non pas pendant l’ischémie mais au moment du rétablissement de la circulation. L’arrivée soudaine d’oxygène et de cellules immunitaires déclenche une tempête de signaux inflammatoires et de molécules réactives qui peuvent perforer la paroi intestinale, permettant aux germes de passer dans la circulation. Malgré son importance clinique, il existe aujourd’hui peu de traitements ciblés pour prévenir cette cascade.
Zoom sur les cellules individuelles
Pour comprendre qui fait quoi pendant cette crise, les auteurs ont utilisé le séquençage d’ARN unicellulaire, une technique qui révèle quels gènes sont actifs dans des milliers de cellules individuelles simultanément. Dans un modèle murin d’ischémie–reperfusion intestinale, ils ont comparé des intestins lésés à des intestins sains et cartographié 19 types cellulaires majeurs. Ils ont observé que certaines cellules immunitaires — en particulier les neutrophiles et les monocytes inflammatoires — augmentaient fortement après la lésion, tandis que des cellules protectrices comme les lymphocytes T, B et les cellules NK déclinaient. Les réseaux de communication entre types cellulaires ont aussi changé, les neutrophiles apparaissant comme des centres névralgiques émettant et recevant de nombreux signaux inflammatoires, ce qui les désigne comme des acteurs clés du dommage.
Une sous‑population nocive parmi les premiers intervenants
Les neutrophiles sont parmi les premiers intervenants les plus rapides de l’organisme, se précipitant dans la circulation pour combattre les infections et éliminer les débris. Mais cette étude montre qu’au sein de la population neutrophile, un sous‑groupe particulièrement agressif est responsable d’une grande partie des dommages collatéraux dans l’intestin. Lorsque les scientifiques ont épuisé les neutrophiles chez des souris avant d’induire l’ischémie–reperfusion, les animaux présentaient moins de raccourcissement intestinal, des taux plus faibles de marqueurs de lésion dans le sang, une apparence tissulaire meilleure au microscope et des protéines d’étanchéité de la muqueuse plus préservées. Dans des expériences en co‑culture, des neutrophiles prélevés sur des souris lésées endommageaient directement les cellules intestinales, réduisant leur survie, augmentant la mort cellulaire et perturbant les protéines en « fermeture éclair » essentielles au maintien de la barrière intestinale.
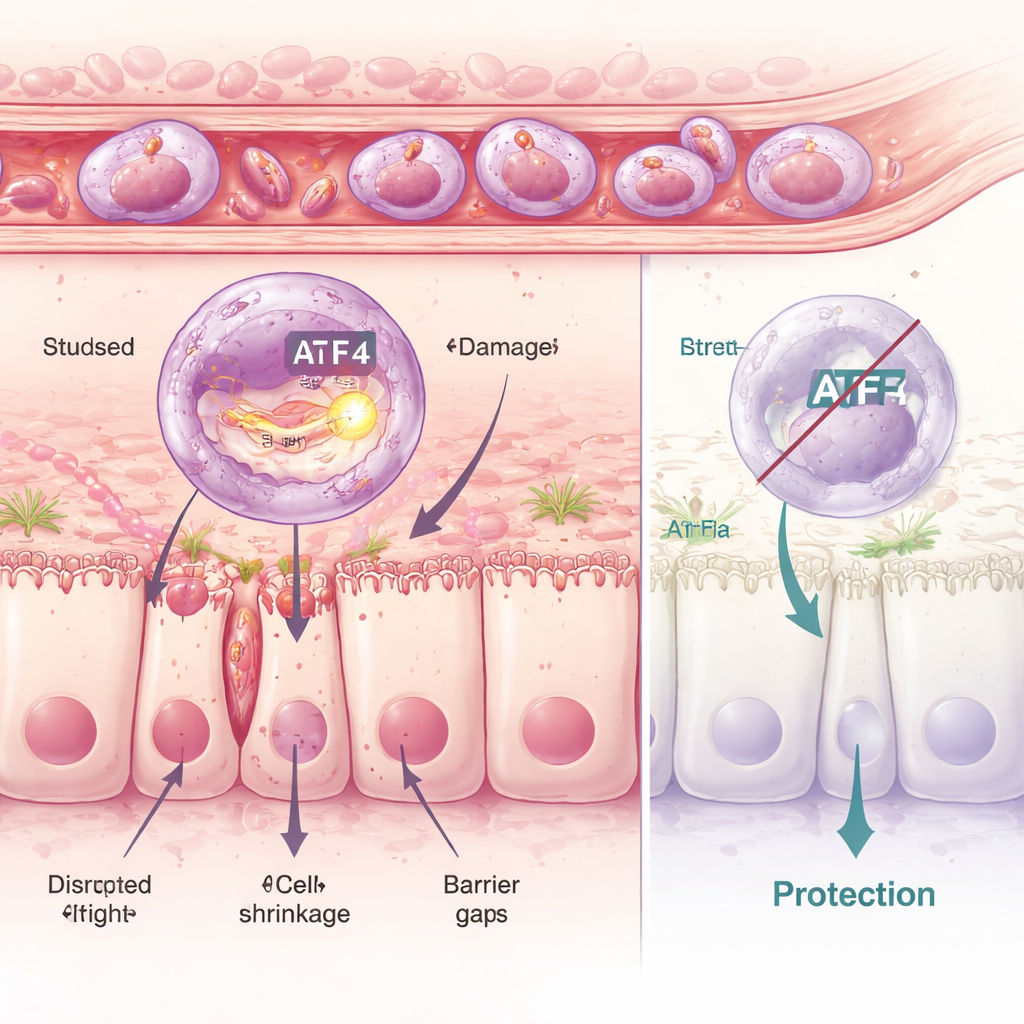
Stress intracellulaire : quand le contrôle qualité déraille
En approfondissant l’analyse, les chercheurs ont examiné les neutrophiles un par un et identifié six sous‑groupes distincts. L’un d’eux, nommé le cluster C5, se distinguait par son profil fortement inflammatoire et par l’activation d’un programme moléculaire de stress à l’intérieur d’une structure appelée réticulum endoplasmique, l’atelier de pliage des protéines de la cellule. Un contrôleur clé de ce programme est la protéine ATF4. Dans les cellules C5 nocives, ATF4 et ses gènes cibles étaient fortement actifs. En utilisant des médicaments qui augmentent ou atténuent cette réponse de stress interne, l’équipe a montré qu’un stress accru se traduisait par des lésions intestinales plus importantes, tandis que le blocage de cette voie préservait la barrière intestinale. Des souris génétiquement dépourvues d’ATF4 étaient en grande partie protégées : même lorsque des médicaments inducteurs de stress étaient administrés, leurs neutrophiles ne pouvaient plus pleinement exécuter leur programme délétère, et la muqueuse restait bien plus intacte.
Ce que cela implique pour les traitements futurs
Ensemble, ces résultats dessinent un tableau clair pour un public non spécialiste : parmi la nuée de cellules immunitaires qui envahissent l’intestin au retour du flux sanguin, une sous‑population spécifique de neutrophiles primée par le stress agit comme une équipe de nettoyage zélée qui détruit le bâtiment en même temps que les débris. Leur pouvoir destructeur dépend d’une voie de stress intracellulaire contrôlée par ATF4. Réduire l’activité de cette voie — sans éliminer tous les neutrophiles — pourrait offrir un moyen de protéger l’intestin lors d’événements à haut risque tels que les chirurgies majeures, les infections sévères ou les traumatismes. Bien que des travaux supplémentaires soient nécessaires pour confirmer ces résultats chez l’humain et trouver des médicaments sûrs et précis, l’étude ouvre une voie prometteuse vers des thérapies qui préservent la barrière intestinale quand les patients en ont le plus besoin.
Citation: Yang, Y., Zhou, Q., Liu, S. et al. A pro-inflammatory neutrophil subpopulation drives intestinal ischemia–reperfusion injury via the ATF4-mediated endoplasmic reticulum stress pathway. Sci Rep 16, 6117 (2026). https://doi.org/10.1038/s41598-026-36938-9
Mots-clés: barrière intestinale, ischémie reperfusion, neutrophiles, stress du réticulum endoplasmique, ATF4