Clear Sky Science · fr
Nanoli posomes à longue circulation conjugués au peptide CKAAKN pour la délivrance ciblée d'oridonine aux cancers du pancréas
Pourquoi cette recherche compte
Le cancer du pancréas fait partie des cancers les plus mortels, en partie parce qu’il est généralement découvert tard et résiste souvent à la chimiothérapie standard. Cette étude explore une façon plus intelligente d’acheminer un composé anti‑cancer d’origine végétale, l’oridonine, directement vers les tumeurs pancréatiques à l’aide de minuscules bulles lipidiques appelées nanoliposomes. En permettant à une plus grande quantité de médicament d’atteindre la tumeur tout en épargnant les tissus sains, ce travail ouvre la voie à des traitements plus doux et potentiellement plus efficaces pour un cancer qui en a cruellement besoin.
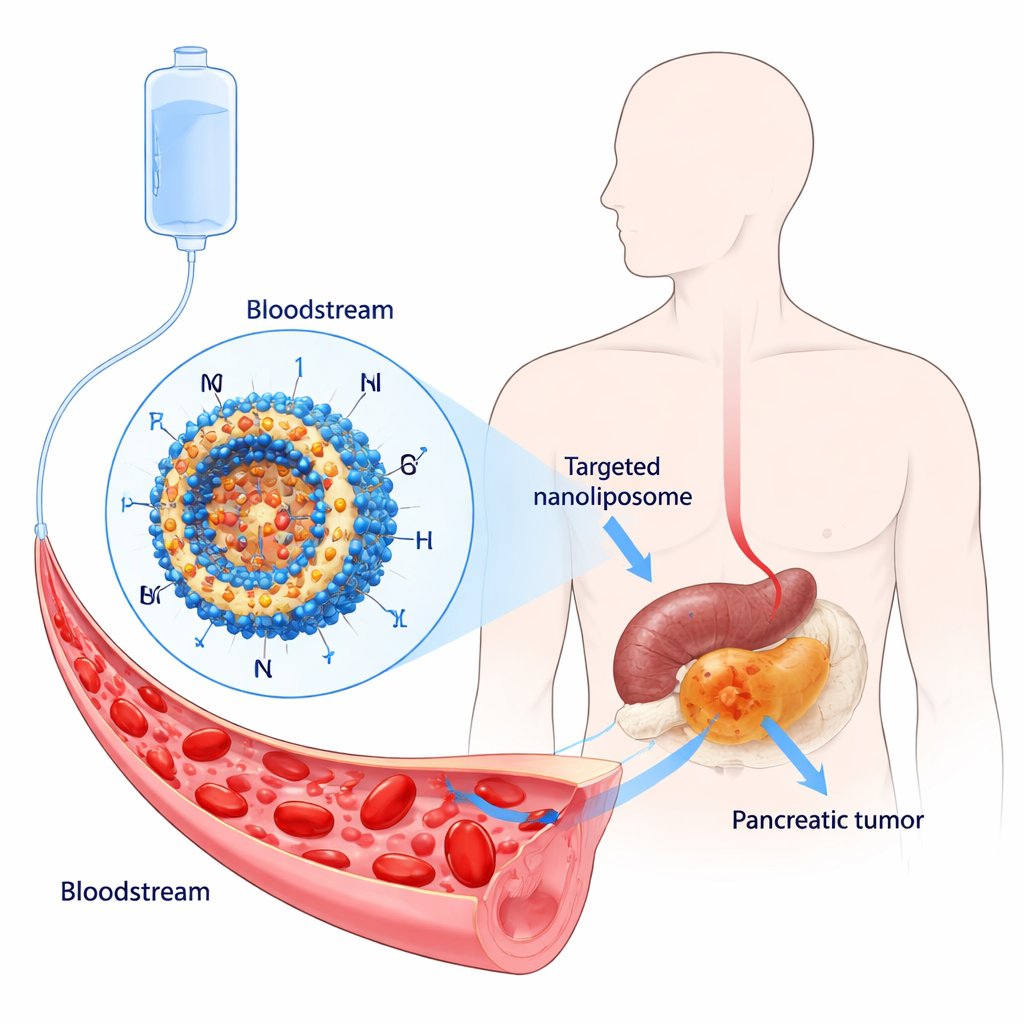
Un cancer meurtrier difficile à traiter
Le cancer du pancréas s’est attiré le surnom sinistre de « roi des cancers » car les taux de survie restent à un seul chiffre pour la plupart des patients. Seule une petite fraction des personnes est éligible à la chirurgie, et même dans ce cas, de nombreuses tumeurs récidivent. Des médicaments de chimiothérapie tels que le paclitaxel et le cisplatine peuvent ralentir la maladie, mais ils provoquent des effets secondaires importants et les tumeurs deviennent souvent résistantes. Les chercheurs cherchent donc des médicaments à la fois plus précis et moins toxiques, ainsi que des systèmes de délivrance capables de concentrer le traitement dans la tumeur plutôt que de diffuser dans tout l’organisme.
Transformer une molécule végétale en médicament moderne
L’oridonine est un composé naturel extrait de la plante médicinale chinoise traditionnelle Rabdosia rubescens. Des études en laboratoire ont montré qu’elle peut tuer ou ralentir la croissance de nombreux types de cellules cancéreuses, y compris celles du pancréas, en perturbant la division cellulaire et en déclenchant l’apoptose. Toutefois, l’oridonine seule est difficile à utiliser comme médicament : elle se dissout mal dans l’eau, est peu absorbée et peut être toxique à des doses élevées. Pour exploiter son potentiel, les auteurs ont cherché à encapsuler l’oridonine dans des nanoliposomes — de minuscules sphères composées de lipides similaires à ceux des membranes cellulaires — conçus pour transporter le médicament en toute sécurité dans la circulation sanguine et le libérer lentement au niveau tumoral.
Conception d’un emballage « furtif » et ciblé pour le médicament
L’équipe a mis au point un système de délivrance à deux couches. D’abord, ils ont fabriqué des liposomes à longue circulation en recouvrant leur surface de polyéthylène glycol (PEG), un polymère hydrophile et flexible qui aide les particules à échapper aux cellules immunitaires et à rester plus longtemps dans le sang. Ils ont ensuite ajouté un court peptide, CKAAKN, qui fait office d’étiquette homing pour le cancer du pancréas. Ce peptide mime une partie de la voie de signalisation Wnt, souvent anormalement active dans de nombreuses tumeurs pancréatiques, permettant aux liposomes modifiés (appelés ORI@CPD‑Lipo) de se fixer aux cellules cancéreuses présentant des récepteurs correspondants. Les particules finales mesuraient environ 100 nanomètres de diamètre, contenaient de fortes quantités d’oridonine et libéraient le médicament lentement sur plusieurs heures plutôt que tout d’un coup.
Comportement des particules ciblées in vitro et in vivo
Dans des tests en culture cellulaire, les liposomes marqués par CKAAKN ont été internalisés beaucoup plus efficacement par des cellules cancéreuses pancréatiques humaines que par des cellules pancréatiques normales, surtout durant les premières heures de contact. Lorsque du peptide CKAAKN libre en excès a été ajouté en tant que leurre, les cellules cancéreuses ont absorbé moins de particules, soutenant l’hypothèse d’une étape de liaison spécifique. Les liposomes vides ont montré une faible toxicité et n’ont pas endommagé les globules rouges, suggérant une bonne sécurité. Chargés d’oridonine, les liposomes ciblés ont tué les cellules cancéreuses plus efficacement que l’oridonine libre ou des liposomes non ciblés, et ont davantage ralenti la migration des cellules cancéreuses à travers une « blessure » en raclage dans une plaque. Chez des souris porteuses de tumeurs pancréatiques, des liposomes ciblés marqués fluorescentement se sont accumulés dans la tumeur pendant jusqu’à 48 heures et s’y sont déposés davantage que les liposomes non ciblés, tout en étant majoritairement éliminés par le foie et la rate comme prévu.
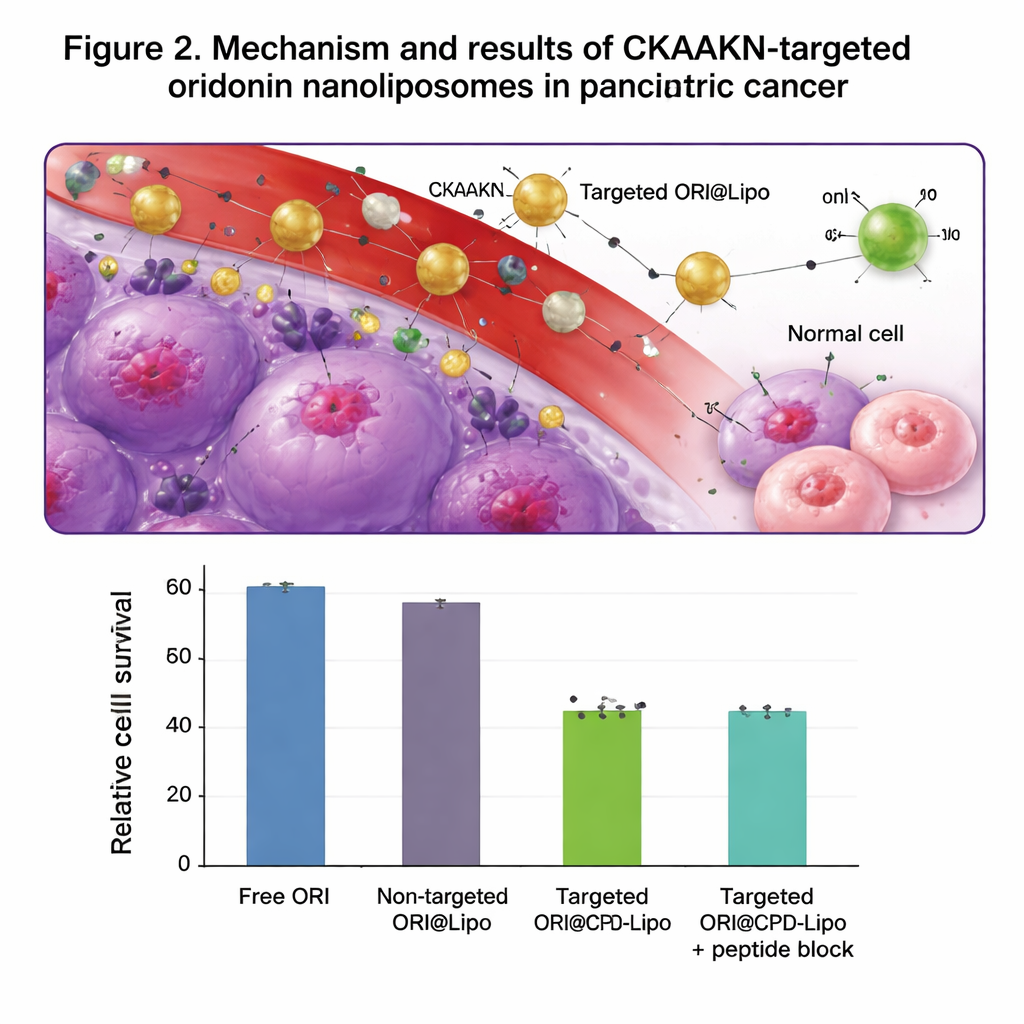
Ce que cela pourrait signifier pour les traitements futurs
Pris ensemble, les résultats montrent que combiner un composé traditionnel d’origine végétale avec un vecteur de délivrance moderne et de précision peut considérablement renforcer son pouvoir anti‑tumoral dans des modèles précliniques. Les nanoliposomes à longue circulation décorés par CKAAKN dirigent davantage d’oridonine vers les cellules cancéreuses du pancréas tout en limitant l’exposition des tissus normaux, augmentant la mort cellulaire tumorale et réduisant les mouvements susceptibles de favoriser la dissémination. Bien que ces conclusions restent précliniques et que les auteurs soulignent la nécessité d’études animales complètes et d’essais cliniques, ce travail pose une base solide pour les approches de nanomédecine ciblée contre le cancer du pancréas et suggère une stratégie générale pour transformer d’autres molécules naturelles prometteuses en médicaments capables de chercher les tumeurs.
Citation: Zhang, F., Luo, K., Xuan, S. et al. CKAAKN peptide-conjugated long-circulating nanoliposomes for the targeted delivery of oridonin to pancreatic cancers. Sci Rep 16, 6065 (2026). https://doi.org/10.1038/s41598-026-36920-5
Mots-clés: cancer du pancréas, nanoliposomes, administration ciblée de médicaments, oridonine, peptide homing tumoral