Clear Sky Science · fr
La métadynamique révèle une stabilisation conformationnelle médiée par la lutéoline contre le PDGFRα D842V/G680R résistant à l’avapritinib dans les GIST
Pourquoi cela compte pour le traitement du cancer
Les médicaments anticancéreux ciblés peuvent être remarquablement efficaces—jusqu’à ce que les tumeurs trouvent des moyens d’y échapper. Cet article explore comment un composé végétal courant, la lutéoline, pourrait aider à restaurer l’efficacité d’un médicament important utilisé contre certains GIST (tumeurs stromales gastro-intestinales). À l’aide de simulations informatiques avancées, les chercheurs montrent comment la lutéoline pourrait stabiliser une protéine déformée dans les cellules cancéreuses pour que le médicament existant puisse de nouveau s’y lier, suggérant une nouvelle façon de combattre la résistance aux médicaments sans réinventer complètement les traitements. 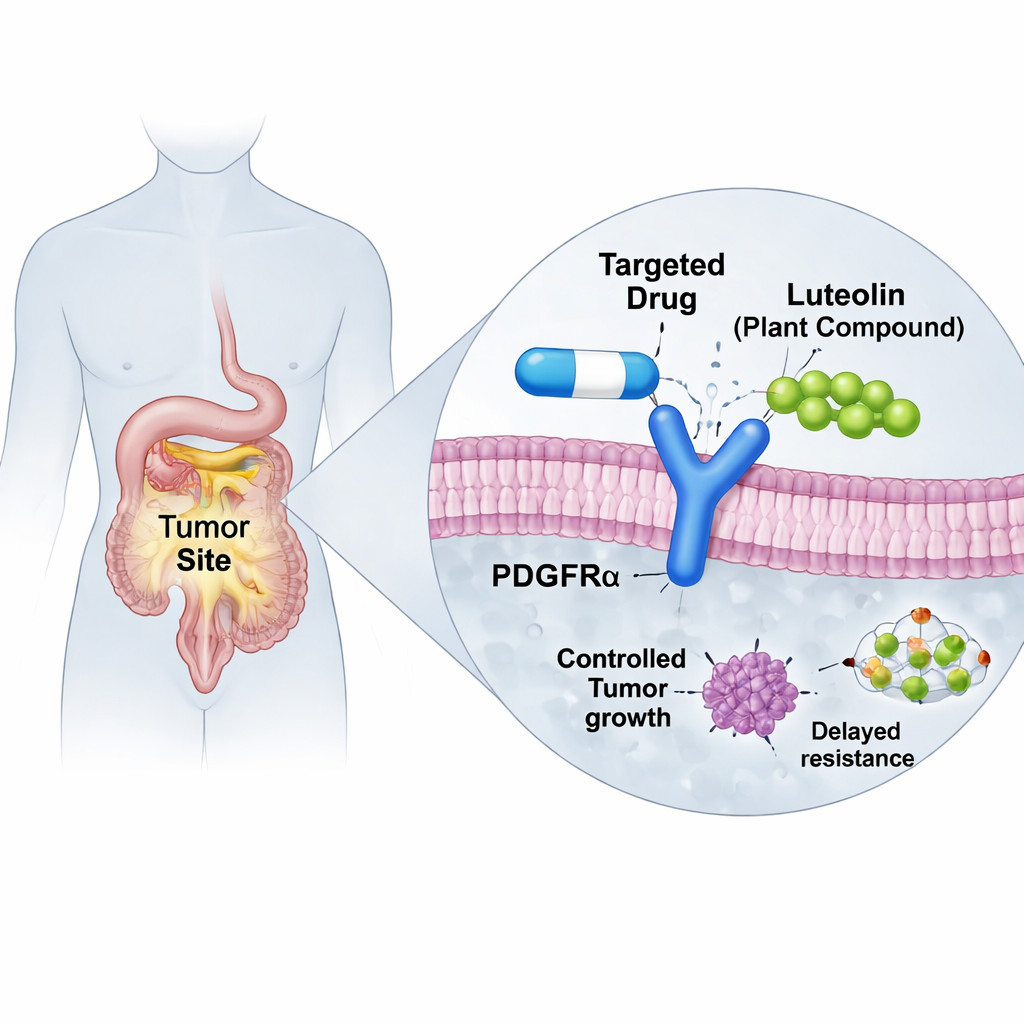
Le problème des tumeurs qui apprennent à esquiver les médicaments
Les GIST croissent souvent à cause d’un « interrupteur » défaillant dans des protéines de surface cellulaire connues sous les noms KIT ou PDGFRα, qui génèrent des signaux de croissance constants. Les médicaments modernes appelés inhibiteurs de tyrosine kinase ont été conçus pour couper ces interrupteurs et ont transformé le pronostic de nombreux patients. Mais une mutation fréquente de PDGFRα, appelée D842V, rend l’ancien médicament imatinib largement inefficace. Un médicament plus récent, l’avapritinib, a été développé spécifiquement pour maîtriser ce mutant récalcitrant et a montré un succès notable en essais cliniques. Malheureusement, les tumeurs peuvent encore s’adapter. Certains patients développent des altérations supplémentaires de PDGFRα, comme une mutation secondaire G680R, qui bloquent physiquement l’emplacement de liaison de l’avapritinib, forçant le médicament à se détacher et favorisant l’apparition de la résistance.
Une molécule végétale à la forme intrigante
Les produits naturels sont une riche source d’idées thérapeutiques, et les flavonoïdes — composés colorés présents dans de nombreux fruits, légumes et plantes médicinales — interagissent souvent avec des protéines contrôlant la croissance cellulaire. La lutéoline, un de ces flavonoïdes présent dans un arbuste méditerranéen appelé Retama monosperma, a déjà été étudiée pour ses propriétés anticancéreuses et anti-inflammatoires et semble sûre à des doses atteignables par supplémentation orale. Sur la base de criblages antérieurs, les auteurs ont supposé que la lutéoline pourrait se fixer à PDGFRα à un endroit proche, mais non chevauchant, du site de liaison habituel du médicament. Si c’était le cas, la lutéoline pourrait agir comme une sorte d’attelle subtile, incitant la protéine à adopter une conformation qui accueille de nouveau l’avapritinib.
Simuler un partenariat moléculaire
Pour tester cette idée in silico, l’équipe a construit des modèles informatiques tridimensionnels détaillés de la protéine PDGFRα résistante portant à la fois les mutations D842V et G680R. Ils ont simulé le comportement de l’avapritinib seul et en présence de lutéoline à proximité, suivant les mouvements atomiques sur des centaines de nanosecondes — des milliards de secondes en temps réel. Lorsque seul l’avapritinib était lié, le médicament dérivait progressivement hors de sa poche alors que la volumineuse mutation G680R le repoussait, finissant complètement détaché de la protéine. En revanche, lorsque la lutéoline était également liée à un site « allostérique » séparé à côté d’une hélice clé, l’avapritinib restait majoritairement en place. La protéine dans son ensemble fléchissait moins, des segments structuraux essentiels conservaient leur conformation, et les contacts importants entre le médicament et la protéine persistaient beaucoup plus longtemps. 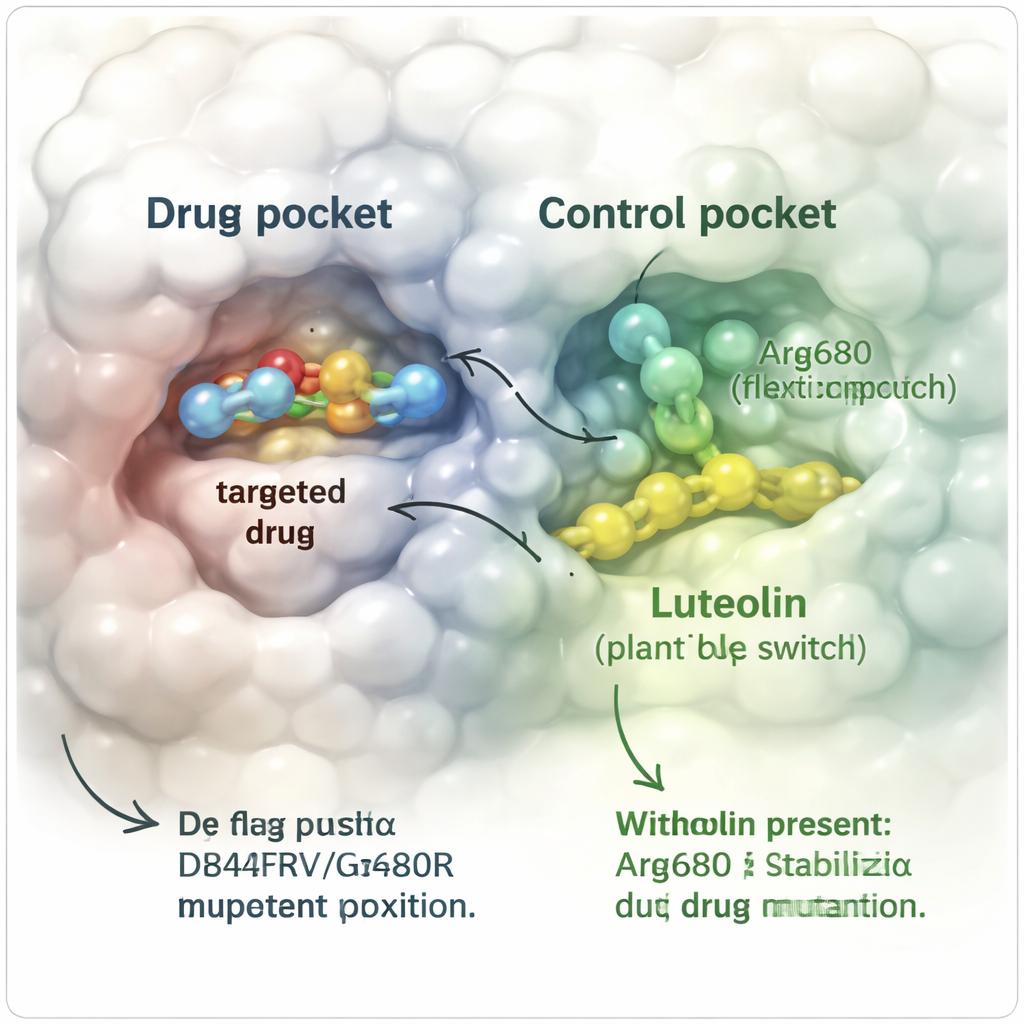
Bloquer un interrupteur moléculaire errant
Les simulations classiques manquent encore des changements de conformation rares mais importants, aussi les chercheurs ont eu recours à une approche améliorée appelée métadynamique pour explorer plus complètement la façon dont la protéine peut se tordre et se plier. Ils se sont concentrés sur le comportement de l’acide aminé modifié Arg680, qui agit comme un petit bras flexible près de la poche de liaison du médicament. Sans lutéoline, ce bras explorait de nombreuses positions et le médicament glissait facilement, avec des barrières d’énergie relativement faibles pour s’échapper. Avec la lutéoline en place, Arg680 était maintenu dans une orientation spécifique qui n’entrait plus en collision avec le médicament. Le paysage énergétique a changé : le système préférait désormais des conformations dans lesquelles l’avapritinib restait lié, et la « colline » énergétique que le médicament devrait gravir pour s’échapper s’est élevée de plusieurs kilocalories, rendant la dissociation beaucoup moins probable.
Ce que cela pourrait signifier pour les patients
Pour faire simple, l’étude suggère que la lutéoline peut agir comme une attelle moléculaire, stabilisant une protéine cancéreuse déformée pour qu’un comprimé ciblé existant puisse de nouveau l’atteindre. Plutôt que de concevoir un médicament entièrement nouveau pour chaque mutation de résistance, associer le traitement actuel à un composé auxiliaire soigneusement choisi pourrait en restaurer l’efficacité. Les travaux reposent sur des méthodes informatiques puissantes mais purement in silico, aussi des études en laboratoire et chez l’animal sont encore nécessaires pour confirmer si la lutéoline, ou une molécule apparentée optimisée pour de meilleures propriétés pharmacologiques, améliore réellement l’action de l’avapritinib in vivo. Néanmoins, le concept d’utiliser de petits auxiliaires allostériques pour re-stabiliser des cibles cancéreuses résistantes pourrait ouvrir une nouvelle voie pour prolonger la durée d’efficacité des thérapies de précision actuelles.
Citation: El Khattabi, K., Akachar, J., Lemriss, S. et al. Metadynamics reveals luteolin-mediated conformational stabilization against avapritinib-resistant PDGFRα D842V/G680R GIST. Sci Rep 16, 6534 (2026). https://doi.org/10.1038/s41598-026-36898-0
Mots-clés: résistance aux médicaments, tumeur stromale gastro-intestinale, inhibiteurs de tyrosine kinase, lutéoline, modulation allostérique