Clear Sky Science · fr
Synthèse et évaluation anticancéreuse de nouveaux dérivés thioimidazoles portant un motif triméthoxyphényle
Nouveaux outils chimiques dans la lutte contre le cancer
Les médicaments de chimiothérapie endommagent souvent les cellules saines en même temps que les tumeurs, entraînant des effets secondaires sévères. Cette étude explore une nouvelle famille de molécules synthétiques visant à toucher les cellules cancéreuses beaucoup plus fortement que les tissus normaux. En associant astucieusement deux blocs chimiques déjà reconnus pour leur efficacité en médecine, les chercheurs ont créé des composés montrant une destruction marquée et ciblée des cellules cancéreuses dans des modèles en éprouvette et en 3D, tout en épargnant dans une large mesure les cellules saines.
Construire des molécules anticancéreuses plus intelligentes
L’équipe s’est concentrée sur deux structures « privilégiées » qui réapparaissent fréquemment dans des médicaments efficaces. La première est l’imidazole, un petit cycle qui s’insère bien dans de nombreuses cibles biologiques. La seconde est le groupe triméthoxyphényle (TMP), une disposition de trois substituants oxygénés sur un noyau aromatique, au cœur de plusieurs médicaments anticancéreux perturbant la division cellulaire. En incorporant un atome de soufre dans le noyau d’imidazole (formant un thioimidazole) et en le liant à un groupe TMP, les chimistes espéraient ajuster le devenir des molécules dans l’organisme et leur affinité pour des protéines liées au cancer. À l’aide d’une synthèse étape par étape, ils ont établi une bibliothèque de composés apparentés, chacun légèrement modifié pour sonder les caractéristiques les plus importantes pour l’activité anticancéreuse. 
Tester les cellules cancéreuses tout en épargnant les tissus sains
Les nouvelles molécules ont été évaluées sur quatre lignées cellulaires cancéreuses humaines — ostéosarcome (os), cancer du col, du côlon et du poumon — ainsi que sur des fibroblastes pulmonaires non cancéreux. Beaucoup de composés ont ralenti ou arrêté la croissance des cellules cancéreuses, mais l’un d’eux en particulier, nommé 13b, s’est distingué. Il a tué les cellules d’ostéosarcome et du cancer du col à des concentrations très faibles, tout en ne montrant aucune toxicité détectable vis‑à‑vis des fibroblastes normaux, même à des doses plus de 60 fois supérieures. Plusieurs autres composés étaient modérément puissants mais moins sélectifs, soulignant comment de petits changements structurels — comme l’ajout d’un atome de chlore ou d’un groupe nitro à des positions spécifiques — peuvent faire basculer l’équilibre entre toxicité large et action ciblée sur le cancer.
Comment le composé principal pousse les cellules cancéreuses à l’autodestruction
Pour comprendre ce que fait réellement le 13b à l’intérieur des cellules, les chercheurs ont recherché les signes caractéristiques de la mort cellulaire programmée, ou apoptosis. Les cellules cancéreuses traitées par le 13b sont devenues positives pour l’Annexine V et ont activé les enzymes caspase‑3 et caspase‑7, marqueurs classiques indiquant qu’une cellule a été entraînée dans un programme d’autodestruction ordonné plutôt que dans une lyse brutale. La microscopie a révélé des points lumineux de γH2AX, signe de cassures de l’ADN, dans les noyaux des cellules traitées. Au fil du temps, le cytosquelette interne des cellules a commencé à se réorganiser et à se désagréger, en particulier dans les cellules du cancer du col qui se sont arrondies et détachées — indices visuels que l’apoptose était bien engagée. Ensemble, ces observations montrent que le 13b endommage l’ADN des cellules cancéreuses puis les pousse vers une voie de mort contrôlée.
Des couches cellulaires plates aux mini‑tumeurs 3D
La plupart des tests en laboratoire font croître les cellules cancéreuses en couches minces, qui n’imitaient pas entièrement la structure dense et stratifiée des tumeurs réelles. Pour remédier à cela, l’équipe a cultivé les cellules cancéreuses en sphéroïdes tridimensionnels — de petits amas sphériques qui ressemblent mieux à l’architecture tumorale et aux défis de pénétration des médicaments. Lorsque ces sphéroïdes ont été traités par le 13b, ils ont rétréci de façon dépendante de la dose. Les sphéroïdes d’ostéosarcome étaient particulièrement sensibles, devenant petits, lâches et fragmentés à des concentrations élevées du composé. La coloration fluorescente a montré des vagues d’apoptose se propageant de l’extérieur vers l’intérieur du sphéroïde à mesure que la concentration augmentait, prouvant que le 13b peut pénétrer et tuer les cellules au sein de ces structures compactes. 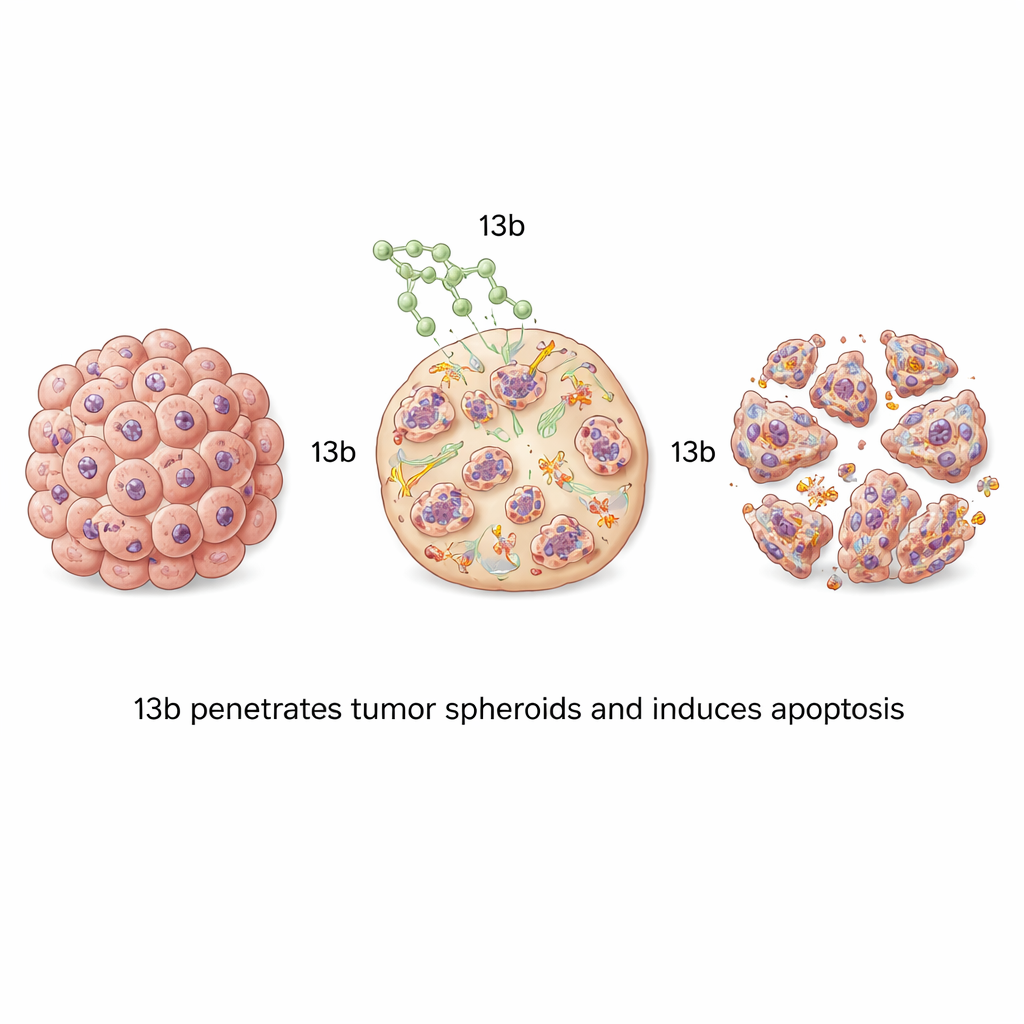
Pourquoi ce travail compte pour les futurs traitements contre le cancer
Pour un non‑spécialiste, le message clé est que les chercheurs ont créé une nouvelle classe de petites molécules qui combinent les meilleures caractéristiques de deux composants médicamenteux éprouvés en un seul hybride. Leur composé principal, le 13b, reconnaît et détruit efficacement les cellules cancéreuses tout en épargnant largement les cellules saines dans les essais en laboratoire, et il reste actif même dans des modèles tumoraux 3D plus réalistes. Bien que de nombreuses étapes restent à franchir — comme l’identification précise de ses cibles moléculaires, l’amélioration de sa solubilité et les essais in vivo — cette étude montre que l’association des cadres thioimidazole et TMP est une stratégie prometteuse pour concevoir des agents anticancéreux plus sélectifs et plus puissants.
Citation: Maciejewska, N., Grybaitė, B., Anusevičius, K. et al. Synthesis and anticancer evaluation of novel thioimidazole derivatives bearing a trimethoxyphenyl moiety. Sci Rep 16, 6271 (2026). https://doi.org/10.1038/s41598-026-36890-8
Mots-clés: agents anticancéreux, dérivés d’imidazole, triméthoxyphényle, apoptose, sphéroïdes tumoraux 3D