Clear Sky Science · fr
Modifications de volume et de fonction du pancréas résiduel après différents types de pancréatectomie : explorer le potentiel régénératif
Pourquoi chirurgiens et patients se préoccupent d’un pancréas “restant”
Lorsqu’une partie du pancréas est retirée chirurgicalement — pour traiter un cancer, des kystes ou une inflammation sévère — les patients se demandent souvent ce qu’il advient du segment qui demeure. Reprend‑il du volume, régresse‑t‑il ou s’adapte‑t‑il d’une autre manière ? Et surtout, quel est l’impact sur le risque de développer un diabète par la suite ? Cette étude a suivi des personnes pendant deux ans après deux interventions pancréatiques courantes pour observer comment le pancréas résiduel évoluait en taille et dans sa capacité à produire de l’insuline, l’hormone qui régule la glycémie.
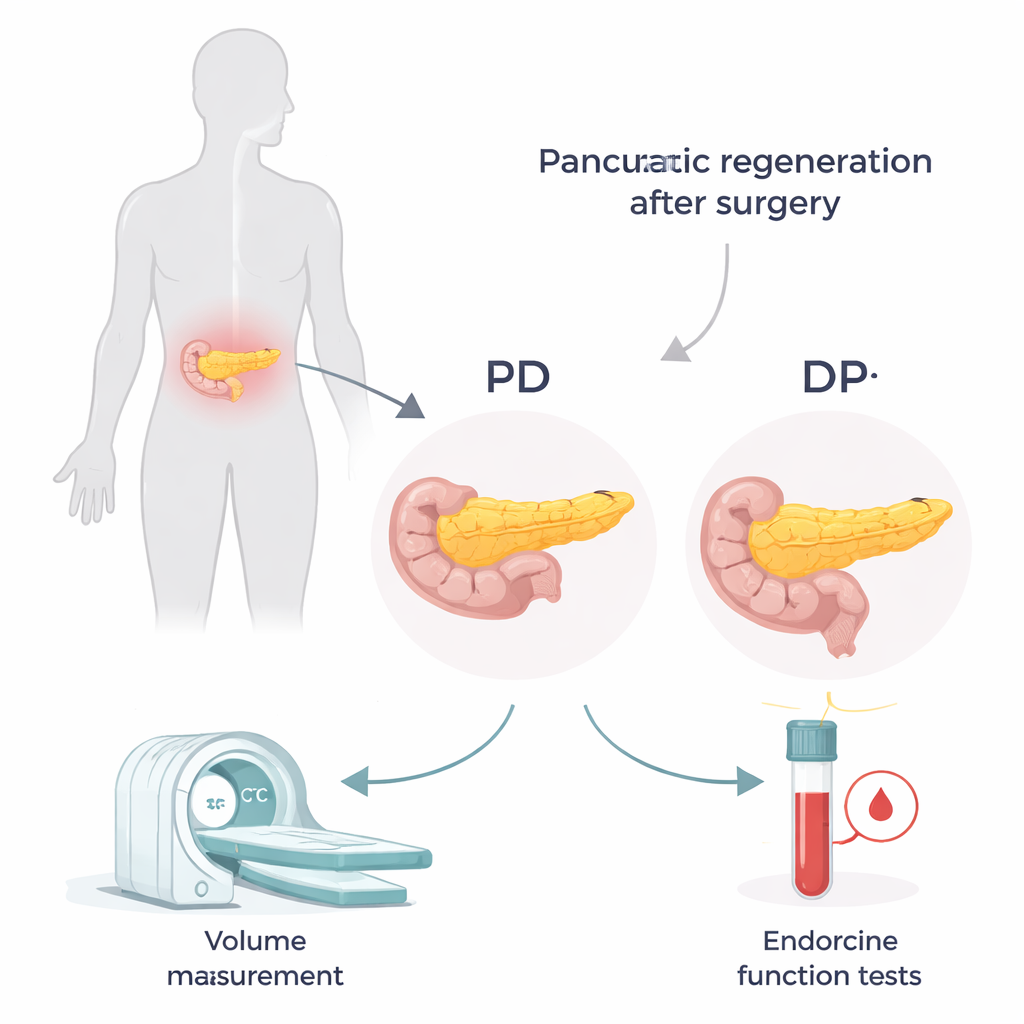
Deux opérations différentes, deux restes différents
Le pancréas est situé profondément dans l’abdomen et s’étend de droite à gauche. Les chirurgiens choisissent entre deux interventions principales selon la localisation de la maladie. Lors d’une pancréaticoduodénectomie (PD, souvent appelée procédure de Whipple), la partie droite dite « tête » est retirée, laissant le « corps et queue » médiaux et gauches. Lors d’une pancréatectomie distale (DP), la portion gauche, la « queue », est retirée, laissant principalement la tête. La tête et la queue ne sont pas identiques : la queue est plus riche en petits îlots cellulaires producteurs d’insuline. Perdre la queue peut donc avoir un impact plus important sur le contrôle glycémique, même si la quantité totale de pancréas enlevée semble similaire.
Mesurer la taille et la puissance hormonale au fil du temps
Pour suivre l’adaptation pancréatique après chirurgie, les chercheurs ont revu les dossiers de 135 patients traités dans un seul hôpital entre 2009 et 2017. Ils ont utilisé des tomodensitogrammes avec contraste pour mesurer le volume du pancréas entier avant l’intervention puis celui du reliquat à 3 mois, 1 an et 2 ans après l’opération. Lors des mêmes consultations, ils ont contrôlé des tests sanguins liés au métabolisme glucidique, y compris le peptide C — marqueur de la production d’insuline par l’organisme. En combinant le peptide C avec la glycémie dans un indice simple, ils ont pu estimer l’efficacité de fonctionnement du tissu pancréatique résiduel.
Quand plus gros ne signifie pas mieux
Les deux interventions ont produit des schémas de régénération et d’atrophie nettement différents. Après pancréatectomie distale, la région résiduelle de la tête a souvent augmenté de volume au fil du temps : en moyenne, son volume atteignait environ 110 % de sa taille post‑opératoire immédiate au bout de deux ans, et près des trois quarts de ces patients présentaient une hypertrophie nette, c’est‑à‑dire un agrandissement. Après pancréaticoduodénectomie, l’inverse s’est observé : le corps et la queue résiduels s’atrophiaient progressivement pour atteindre environ les deux‑tiers de leur taille initiale, et une véritable augmentation était rare. La dilatation du canal pancréatique principal — signe que la connexion de drainage peut être rétrécie — était associée à une plus grande atrophie chez les patients opérés par PD. Pourtant, malgré la conservation d’un plus grand volume de tissu, les patients DP se portaient moins bien sur le plan métabolique : environ un tiers des patients initialement non diabétiques après DP ont développé un nouveau diabète, et aucun des patients diabétiques préexistants n’est entré en rémission.
La force cachée des cellules productrices d’insuline restantes
Une analyse plus fine de la sécrétion hormonale a montré pourquoi la seule taille ne rendait pas tout compte. Dans les deux groupes, la production d’insuline diminuait à trois mois puis se rétablissait partiellement. Lorsque les chercheurs ont ajusté la production d’insuline en fonction de la quantité de pancréas restante, ils ont constaté que le pancréas après PD devenait étonnamment efficace : chaque unité de tissu produisait davantage d’insuline au fil du temps. En revanche, les patients ayant perdu la queue riche en îlots après DP présentaient une récupération endocrine plus faible, même si leur pancréas résiduel était plus volumineux et parfois hypertrophié. Cela corrobore des études anatomiques montrant que la queue contient environ deux fois plus de cellules productrices d’insuline que la tête, et suggère que les cellules survivantes peuvent « travailler plus dur » pour compenser quand c’est nécessaire.
Conséquences pour la chirurgie et la santé à long terme
Pour les patients et les chirurgiens, ces résultats soulignent que l’important n’est pas seulement la quantité de pancréas préservée, mais quelle partie est conservée. L’ablation de la queue distale, riche en îlots, entraîne un risque plus élevé de diabète que l’ablation de la tête, même lorsque davantage de tissu total est sauvé. Le rétrécissement du canal pancréatique après une procédure de Whipple peut en outre endommager le reliquat en provoquant cicatrisation et atrophie. Les auteurs concluent que les interventions pour des tumeurs bénignes ou à faible risque devraient être planifiées de façon à préserver autant que possible les cellules productrices d’insuline — en privilégiant parfois des techniques qui épargnent la queue — afin d’offrir aux patients les meilleures chances de maintenir une glycémie saine dans les années suivant la chirurgie.
Citation: Lu, WH., Tsai, HM., Liao, TK. et al. Volume and functional changes of remnant pancreas after different types of pancreatectomy: Exploring the regenerative potential. Sci Rep 16, 6947 (2026). https://doi.org/10.1038/s41598-026-36886-4
Mots-clés: pancréatectomie, régénération pancréatique, diabète pancréatogénique, fonction endocrine, pancréaticoduodénectomie vs pancréatectomie distale