Clear Sky Science · fr
Bénéfice et risque associés à l’administration d’un inhibiteur du récepteur de l’interleukine‑6 lors de formes sévères de COVID‑19 : une étude multicentrique rétrospective
Pourquoi cela compte pour les patients et leurs familles
Pendant la pandémie de COVID‑19, les médecins avaient un besoin urgent de traitements pour aider les patients les plus gravement atteints à survivre, en particulier ceux en détresse respiratoire. Une option prometteuse était une classe de médicaments bloquant l’interleukine‑6 (IL‑6), un médiateur puissant de l’inflammation dans l’organisme. Ces médicaments, comme le tocilizumab et le sarilumab, peuvent calmer une réponse immunitaire trop active — mais ils peuvent aussi affaiblir les défenses de l’organisme contre les microbes. Cette étude pose une question simple mais cruciale : lorsqu’ils sont utilisés dans des hôpitaux en situation réelle pour des cas sévères de COVID‑19, ces médicaments apportent‑ils plus d’avantages que de risques ?
Comment l’étude a été conçue
Des chercheurs à Paris ont examiné rétrospectivement les dossiers médicaux de 2 587 adultes hospitalisés pour un COVID‑19 sévère ou critique entre mars 2020 et décembre 2021. Certains patients sont restés uniquement en service conventionnel, tandis que d’autres ont nécessité des unités de soins intensifs (USI) en raison d’une défaillance d’organe ou du besoin de ventilation mécanique. Parmi ces groupes, une minorité — 224 personnes, soit environ 9 % — ont reçu au moins une dose d’un inhibiteur du récepteur de l’IL‑6 (IL‑6Ri), principalement du tocilizumab et, plus rarement, du sarilumab. L’équipe a comparé les patients traités ou non par ces médicaments, en se concentrant sur des effets indésirables graves tels que les infections nosocomiales, les saignements digestifs et les troubles sanguins comme la thrombopénie ou la leucopénie.
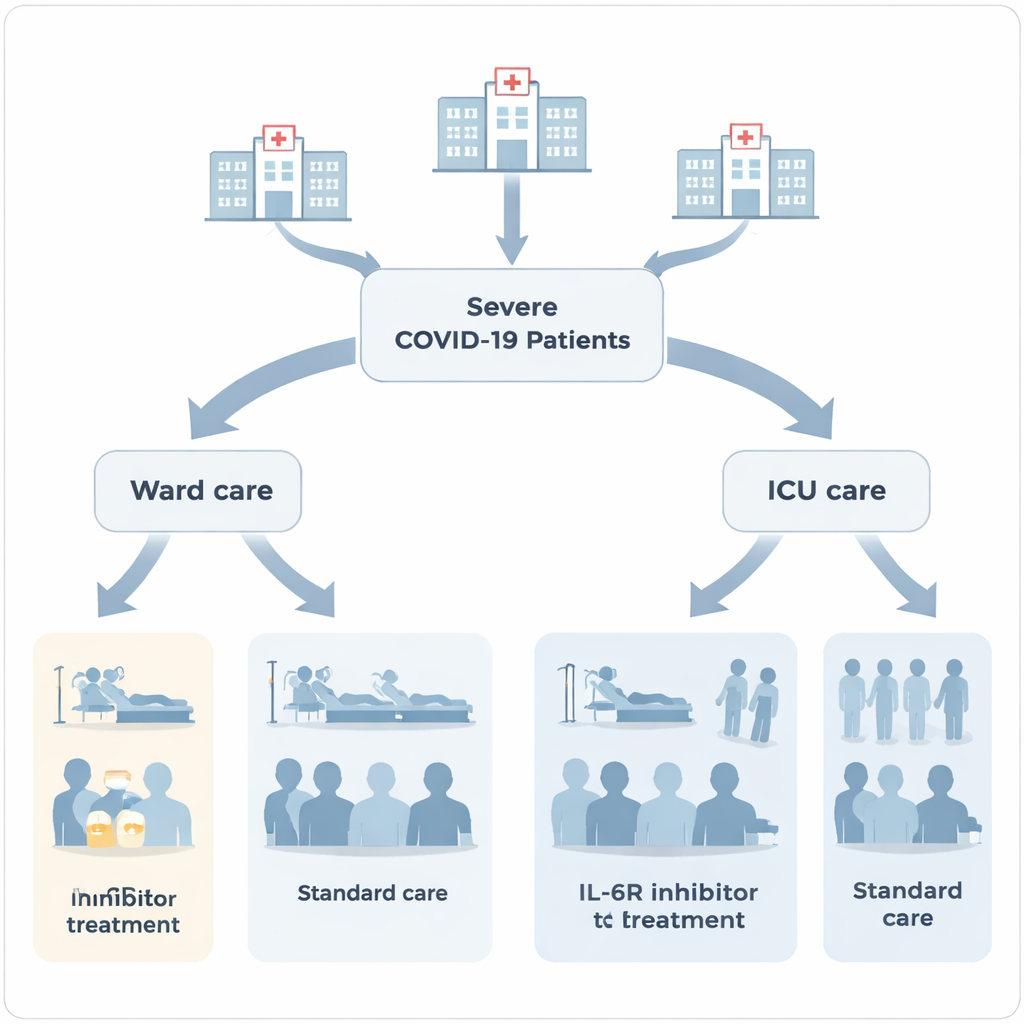
Ce qui est arrivé aux patients en services conventionnels
Parmi les 1 603 patients hospitalisés en service conventionnel, ceux traités par IL‑6Ri avaient tendance à être plus malades : ils avaient plus souvent besoin d’oxygène à haut débit, séjourné plus longtemps et reçu plus fréquemment d’autres traitements comme des corticostéroïdes et des anticoagulants. Dans ce groupe, le risque de décès à l’hôpital était plus élevé pour les patients ayant reçu un IL‑6Ri (environ 19 %) comparé à ceux qui n’en ont pas reçu (environ 10 %). Parallèlement, la durée moyenne d’hospitalisation était plus longue — 10 jours contre 7 jours en moyenne. Si ces différences peuvent en partie refléter le fait que les médecins réservaient les IL‑6Ri aux patients les plus fragiles, elles soulèvent des inquiétudes quant à l’absence d’amélioration nette des résultats en dehors de l’USI.
Ce qui est arrivé en soins intensifs
Chez les 984 patients ayant nécessité des soins en USI, les schémas thérapeutiques étaient quelque peu différents. Ici, 133 patients ont reçu un IL‑6Ri. Les patients en USI, traités ou non, ont nécessité de hauts niveaux de support avancé tels que la ventilation mécanique, la position ventrale et parfois l’oxygénation par membrane extracorporelle (ECMO), une forme de contournement cœur‑poumons. Dans ce groupe plus gravement atteint, les taux de décès hospitaliers étaient similaires, que les patients aient reçu un IL‑6Ri ou non — environ un sur quatre est décédé dans chaque groupe. Les durées de séjour en USI et le temps total d’hospitalisation étaient également à peu près les mêmes. En d’autres termes, dans cette population ICU en conditions réelles, le blocage de l’IL‑6 n’a pas clairement amélioré la survie, mais il ne l’a pas non plus détériorée.
Le risque clé : davantage d’infections
Le constat le plus marquant est apparu lorsque les chercheurs ont examiné les nouvelles infections survenues pendant l’hospitalisation, comme les pneumonies associées à la ventilation, les infections urinaires, les bactériémies et autres maladies nosocomiales. Dans l’ensemble de la population, les patients ayant reçu un IL‑6Ri ont présenté plus d’infections secondaires que ceux qui n’en ont pas reçu. Après ajustement minutieux sur l’âge, le poids, les comorbidités et la sévérité de la maladie, l’utilisation d’IL‑6Ri restait associée à un risque d’infection plus élevé — de l’ordre d’une augmentation relative de 40 % à 100 %, selon la méthode d’analyse. Ce risque supplémentaire n’était pas limité à un type particulier d’agent infectieux ou à un site spécifique d’infection. En revanche, les saignements digestifs graves et les complications sanguines sont survenus à des fréquences similaires avec ou sans IL‑6Ri, ce qui suggère que ces effets redoutés n’étaient pas sensiblement amplifiés par ces médicaments dans ce contexte.
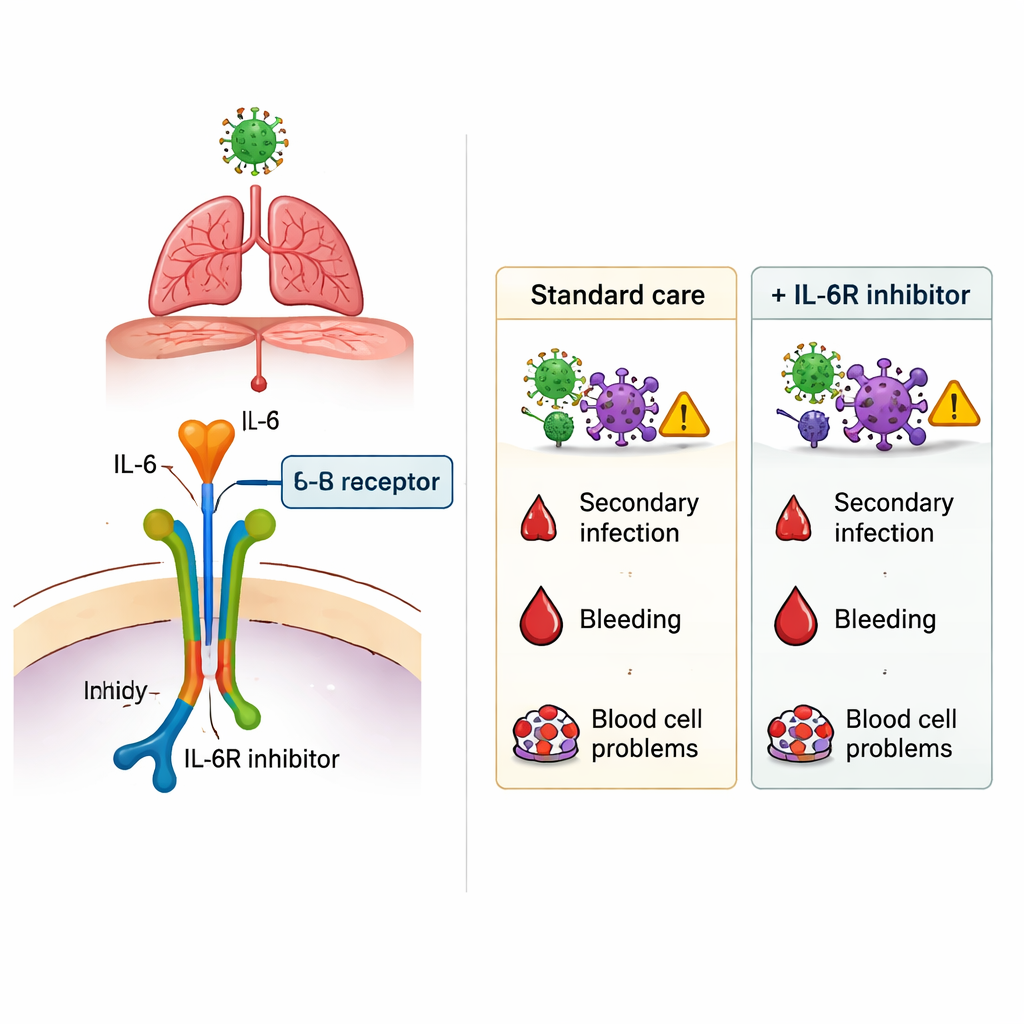
Ce que cela signifie pour l’avenir
Pour le grand public, la conclusion est que des médicaments comme le tocilizumab et le sarilumab peuvent modifier modestement l’évolution d’un COVID‑19 sévère, mais pas sans coût. Dans cette vaste étude française, leur emploi a été lié à une probabilité accrue d’infections nosocomiales, tandis que la survie des patients les plus graves en USI ne s’est pas clairement améliorée et que les patients en service conventionnel qui les ont reçus ont eu un taux de mortalité plus élevé. L’étude ne prouve pas que les bloqueurs de l’IL‑6 aient directement causé ces résultats — les médecins ont pu les choisir pour des patients déjà à haut risque — mais elle renforce la nécessité de décisions individualisées et prudentes. Lors de la considération d’un traitement par inhibiteur de l’IL‑6, les cliniciens doivent peser le bénéfice potentiel d’un ralentissement de l’inflammation dangereuse contre la possibilité réelle d’induire de nouvelles infections, surtout chez les patients vulnérables.
Citation: Lefèvre, C., Funck-Brentano, T., Cachanado, M. et al. Benefit and risk associated with interleukin-6 receptor inhibitor administration during severe COVID-19: a retrospective multicentric study. Sci Rep 16, 5978 (2026). https://doi.org/10.1038/s41598-026-36864-w
Mots-clés: COVID‑19, inhibiteur de l’interleukine‑6, tocilizumab, infections secondaires, soins intensifs