Clear Sky Science · fr
Le 4‑nonylphénol régule la prolifération et l’apoptose cellulaires dans le carcinome du col de l’utérus via la voie de signalisation MEG3/PI3K/AKT
Des produits chimiques quotidiens et le risque de cancer chez les femmes
Nous sommes entourées de substances issues des plastiques, des détergents et des pesticides qui peuvent agir comme des hormones dans l’organisme. Cette étude examine si l’un de ces composés, le 4‑nonylphénol (4‑NP), pourrait favoriser le cancer du col de l’utérus, et comment une molécule protectrice naturelle présente dans nos cellules, appelée MEG3, pourrait s’y opposer. Comprendre cette relation pourrait indiquer de nouvelles façons de réduire le risque lié à la pollution environnementale et de concevoir des traitements plus ciblés contre le cancer du col de l’utérus.
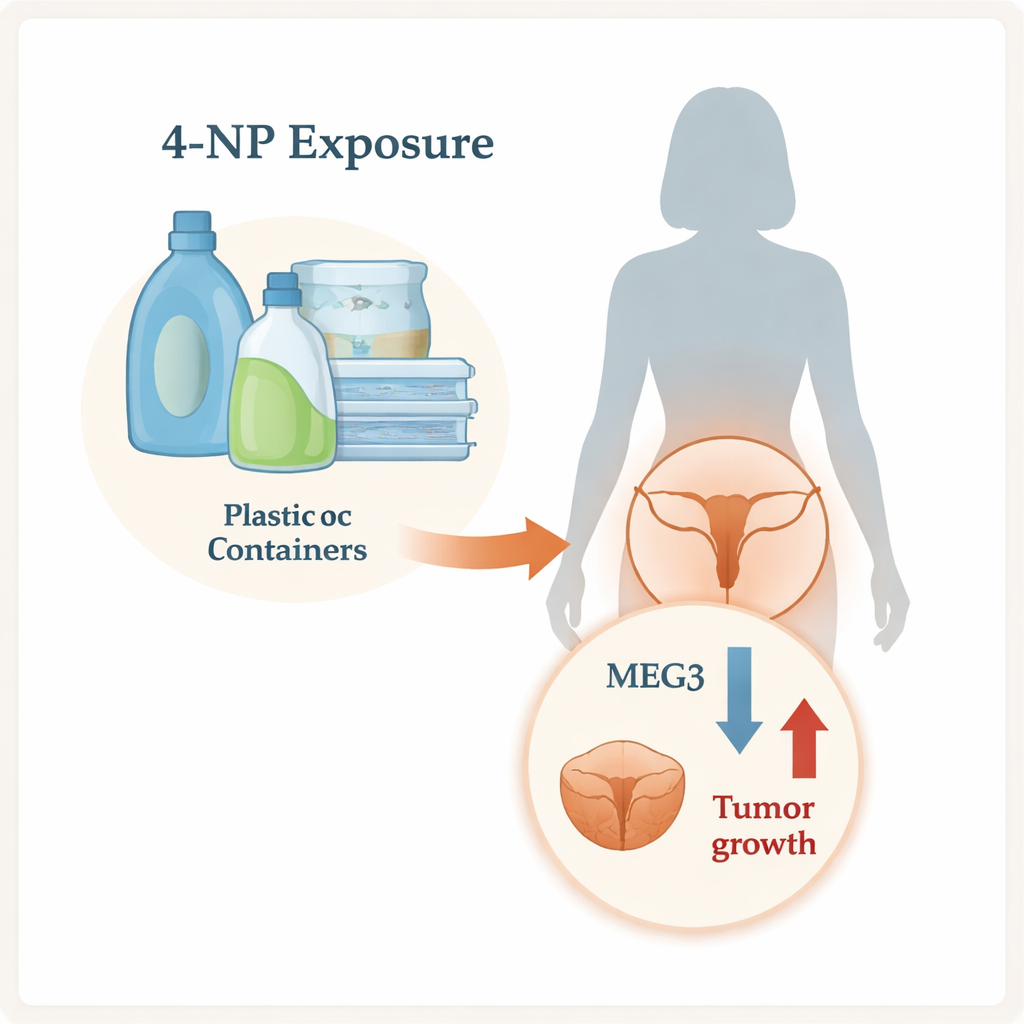
Un polluant courant passé au crible
Le 4‑NP est largement utilisé dans des produits industriels et peut s’infiltrer dans l’eau, le sol et, in fine, l’organisme humain. Il se comporte un peu comme l’œstrogène, une hormone féminine clé, et a été associé à des troubles du système reproducteur. Les chercheurs ont d’abord posé une question simple : les femmes atteintes d’un cancer du col ont‑elles des taux plus élevés de ce produit chimique dans leur organisme ? En mesurant le 4‑NP dans l’urine de 35 femmes atteintes d’un carcinome du col et de 35 femmes en bonne santé, ils ont constaté que les patientes présentaient en moyenne près de six fois plus de 4‑NP. Cela ne prouve pas que le produit chimique cause le cancer, mais montre que les femmes atteintes ont tendance à avoir une exposition interne nettement plus élevée.
Le frein naturel de l’organisme : MEG3
À l’intérieur de nos cellules, de longs brins d’ARN qui ne codent pas pour des protéines peuvent néanmoins contrôler la croissance et la mort cellulaires. L’un d’eux, appelé MEG3, agit normalement comme un frein à la croissance tumorale. L’équipe a comparé des tissus de carcinome du col avec des tissus sains adjacents provenant de 31 patientes et a constaté que les niveaux de MEG3 étaient bien plus faibles dans les tumeurs. Ils ont observé le même schéma en expériences cellulaires : les cellules du cancer du col (HeLa) avaient moins de MEG3 que les cellules cervicales normales, et lorsque les cellules étaient exposées au 4‑NP, MEG3 chutait encore davantage avec le temps. Cela suggère que le cancer lui‑même et l’exposition environnementale au 4‑NP peuvent agir de concert pour réduire l’expression d’un signal naturel suppresseur de tumeur.
Lorsque le frein est rétabli
Ensuite, les scientifiques ont testé ce qui se passait s’ils forçaient les cellules cancéreuses à produire plus de MEG3. En utilisant un vecteur viral pour augmenter MEG3 dans des cellules HeLa, ils ont observé un ralentissement des cellules. Les cellules cancéreuses se divisèrent moins, migrèrent plus lentement sur une plaque (un signe de moindre capacité d’invasion) et furent plus susceptibles de subir l’apoptose. Les tests du cycle cellulaire montrèrent que MEG3 poussait les cellules à faire une pause avant la réplication de l’ADN, une autre manière de limiter la croissance. Chez la souris, les tumeurs issues de cellules HeLa sur‑expressant MEG3 étaient nettement plus petites et plus légères que celles issues de cellules cancéreuses habituelles, confirmant que MEG3 peut freiner la croissance tumorale in vivo.
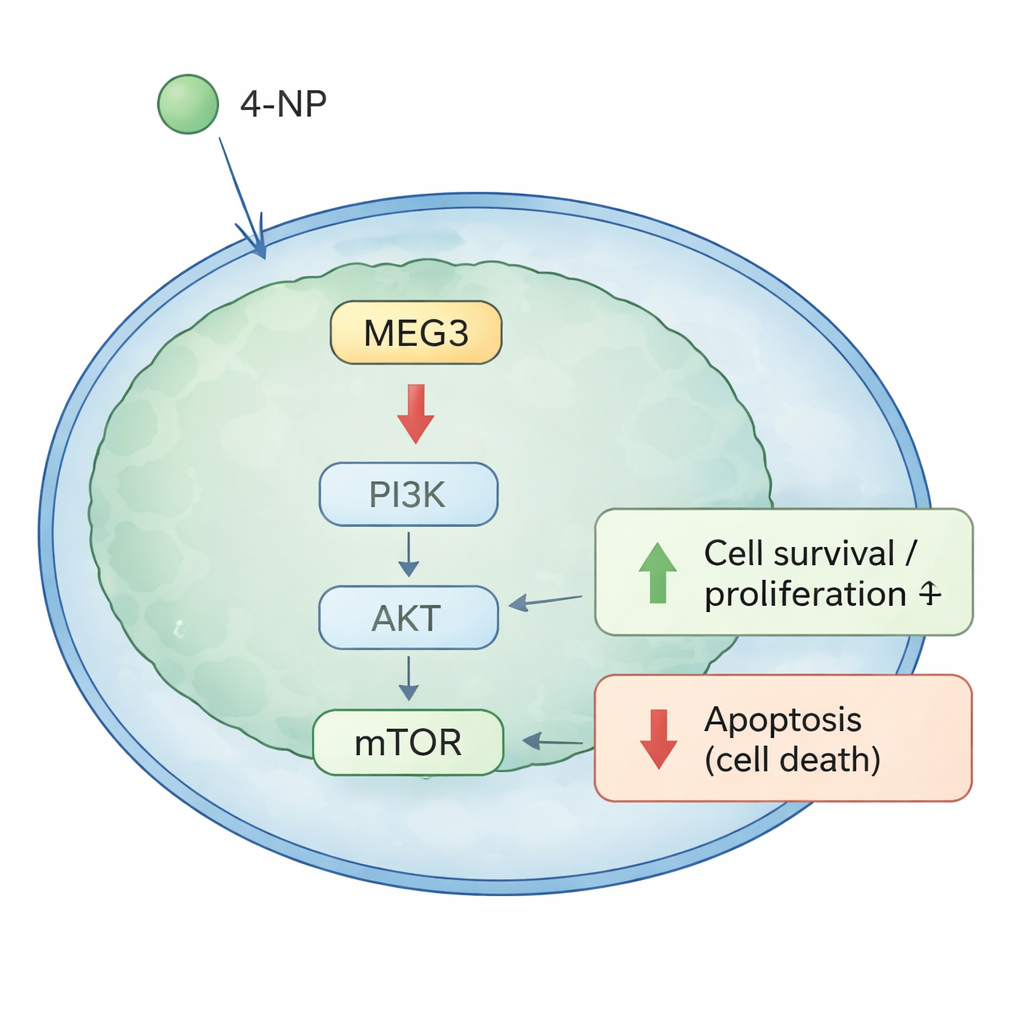
Un interrupteur de croissance à l’intérieur des cellules cancéreuses
Pour comprendre comment MEG3 exerce ce contrôle, les chercheurs se sont concentrés sur un commutateur de croissance bien connu dans les cellules : la voie PI3K/AKT. Lorsque cette voie est active, les cellules ont tendance à croître et à survivre ; lorsqu’elle est atténuée, les cellules sont plus susceptibles de mourir. Tant en culture cellulaire que dans les tumeurs de souris, l’augmentation de MEG3 réduisit les formes actives (phosphorylées) de PI3K, AKT et mTOR, ainsi que BCL‑2, une protéine qui protège les cellules de la mort, tout en favorisant des signaux pro‑mort. En revanche, l’exposition des cellules au 4‑NP eut l’effet opposé : elle augmenta les signaux de croissance et de survie et diminua la mort cellulaire. Fait important, lorsque MEG3 fut restauré, il inversa en grande partie les effets pro‑croissance et anti‑mort du 4‑NP, ce qui laisse penser que cet ARN joue un rôle clé de médiateur entre l’exposition environnementale et le comportement des cellules cancéreuses.
Ce que cela signifie pour les patientes et la prévention
Pour un public non spécialiste, le message est le suivant : un produit chimique environnemental courant semble associé à une exposition interne plus élevée chez les femmes atteintes d’un cancer du col et peut, en laboratoire, pousser les cellules cancéreuses à croître plus vite et à mourir moins souvent. MEG3, une molécule naturelle de nos cellules, fait office de garde‑fou en réduisant l’activité d’une voie de croissance puissante. Bien que l’étude ne puisse pas encore prouver que le 4‑NP provoque le cancer du col, et qu’elle soit limitée par sa taille et ses modèles expérimentaux, elle met en évidence une nouvelle chaîne d’événements : le 4‑NP réduit MEG3, ce qui libère un interrupteur de croissance et favorise le développement tumoral. À l’avenir, la surveillance des niveaux de 4‑NP et de l’activité de MEG3 pourrait aider à évaluer le risque environnemental, et des thérapies visant à restaurer MEG3 ou à bloquer la même voie de croissance pourraient offrir de nouvelles options pour les femmes confrontées au cancer du col de l’utérus.
Citation: Wu, W., Ren, X., Chen, Y. et al. 4-Nonylphenol regulates cell proliferation and apoptosis in cervical carcinoma through the MEG3/PI3K/AKT signaling pathway. Sci Rep 16, 6067 (2026). https://doi.org/10.1038/s41598-026-36863-x
Mots-clés: cancer du col de l’utérus, polluants environnementaux, 4‑nonylphénol, ARN long non codant MEG3, voie PI3K AKT