Clear Sky Science · fr
Mécanismes différenciés d’inactivation du SARS‑CoV‑2 par des tensioactifs anioniques : étude comparative des sels d’acides gras et des tensioactifs synthétiques
Pourquoi le savon que vous utilisez compte encore
La pandémie de COVID‑19 a fait du lavage des mains un rituel quotidien, mais tous les savons n’agissent pas de la même façon contre le virus responsable de la maladie. Cette étude examine au microscope les ingrédients courants des savons pour déterminer lesquels désarment le mieux le SARS‑CoV‑2 et par quels mécanismes. Les résultats peuvent orienter des choix plus judicieux pour les savons et désinfectants de tous les jours, faisant d’un geste routinier comme se laver les mains un outil encore plus efficace pour protéger la santé.
Comment le savon attaque un bouclier gras
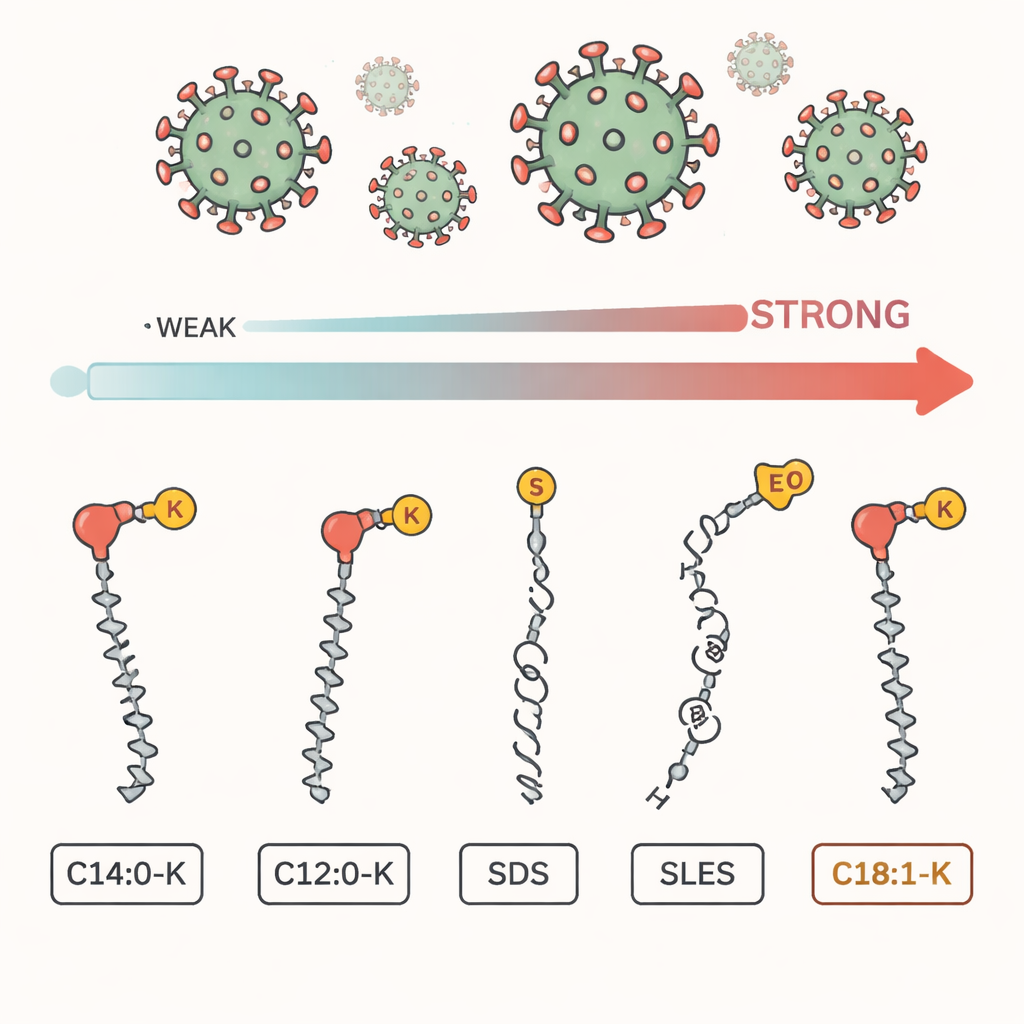
Le SARS‑CoV‑2, comme de nombreux virus dangereux, est entouré d’une coquille huileuse et fragile composée de lipides. Les molécules de savon ont deux visages : une partie aime l’eau, l’autre aime les graisses. Lors du lavage des mains, ces molécules s’insèrent dans cette enveloppe grasse et peuvent la déchirer, rendant le virus incapable d’infecter des cellules. Mais les savons sont constitués d’ingrédients différents ; cette étude a comparé cinq d’entre eux couramment utilisés : trois sels d’acides gras naturels (dont l’oléate de potassium, appelé C18:1‑K) et deux tensioactifs synthétiques fréquents, le SDS et le SLES, présents dans nombre de savons liquides et de shampoings.
Quels ingrédients de savon frappent le plus fort le virus
Quand les chercheurs ont mis le virus en contact avec ces tensioactifs en laboratoire, un ingrédient s’est distingué. Le C18:1‑K, composant naturel du savon avec une longue chaîne légèrement coudée, a réduit l’infectiosité du virus de plus de 100 000 fois à très faible concentration. Le SDS, tensioactif synthétique plus agressif, n’a atteint qu’une réduction d’environ dix fois au même niveau, tandis que le SLES et un ingrédient à chaîne plus courte, le C12:0‑K, n’ont quasiment pas inactivé le virus. Dans l’ensemble, le classement est net : C18:1‑K en tête, suivi par le SDS, puis le SLES, les acides gras plus courts fermant la marche. Des chaînes plus longues et plus lipophiles confèrent une inactivation virale bien plus puissante.
Un coup d’œil sur des batailles invisibles
Pour comprendre pourquoi ces différences étaient si marquées, l’équipe a utilisé une technique mesurant les variations de chaleur pour suivre l’interaction entre tensioactifs et virus. Le C18:1‑K a produit un signal thermique indiquant qu’il enfonce principalement sa queue huileuse dans la membrane lipidique du virus, un processus entraîné par des forces hydrophobes (affinité pour les graisses). Le SDS et le C12:0‑K, en revanche, ont montré un changement thermique opposé, suggérant qu’ils se lient davantage aux parties chargées des protéines à la surface du virus plutôt que de perturber profondément la membrane lipidique. Le SLES semblait se situer entre les deux, ses tendances hydrophobes et hydrophiles se neutralisant en partie. Ces empreintes énergétiques ont révélé que ce n’est pas seulement la puissance, mais aussi le mode d’attaque qui diffère selon les ingrédients.
Ce que le microscope a révélé
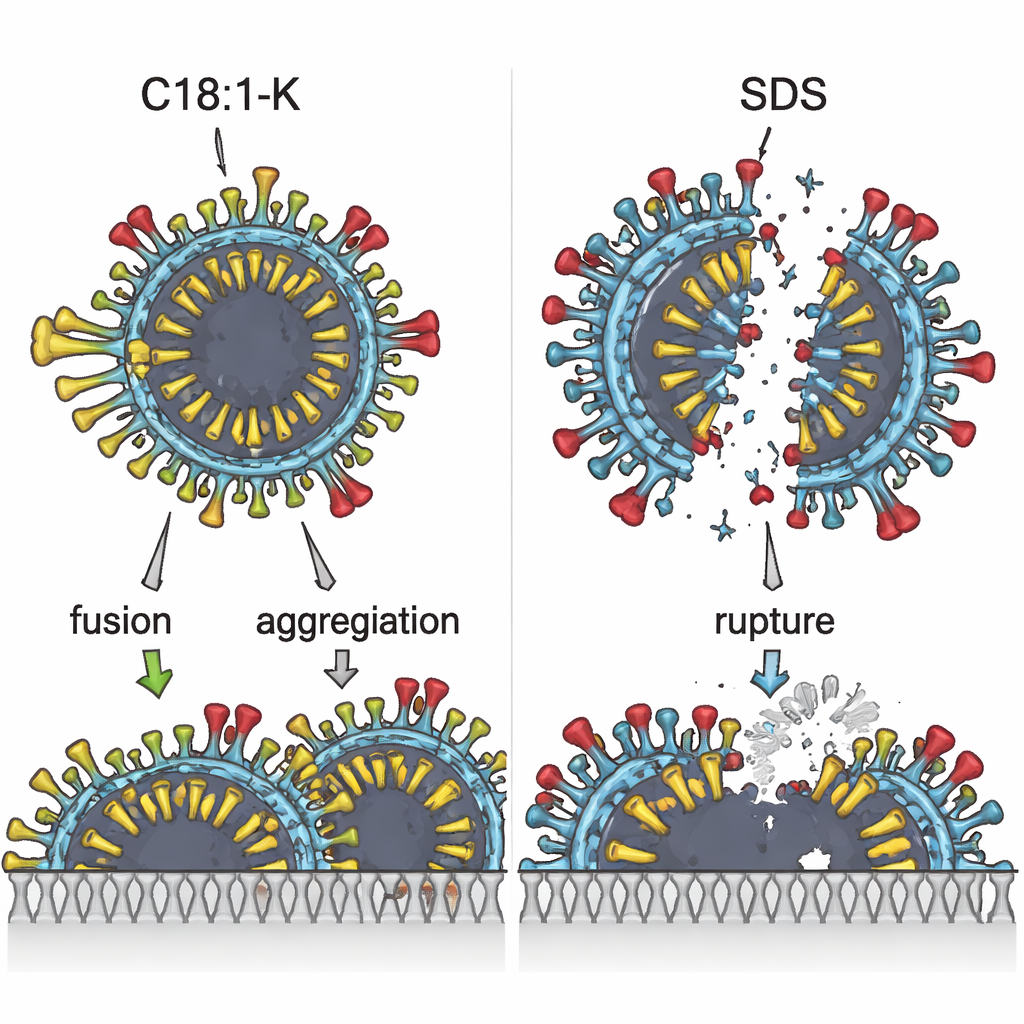
La microscopie électronique a apporté un pendant visuel à ces variations énergétiques invisibles. Lorsque le virus était traité par des tensioactifs agissant principalement par attraction électrostatique aux protéines, comme le SDS ou le C12:0‑K, de nombreuses particules semblaient éventrées ou rompues. Avec le C18:1‑K, en revanche, les particules virales apparaissaient plus souvent fusionnées ou agglomérées, sans éclatement évident. Tous les tensioactifs provoquaient un certain degré d’agrégation virale à des concentrations élevées, mais seul le C18:1‑K produisait des amas étendus de « fusion des membranes », peu susceptibles de rester infectieux. L’ingrédient le plus efficace pour inactiver le virus, le C18:1‑K, présentait aussi la plus faible concentration micellaire critique — un signe que ses queues lipidiques s’assemblent facilement et peuvent perturber fortement l’enveloppe virale une fois un seuil atteint.
Ce que cela signifie pour la protection quotidienne
Pour le grand public, le message est simple : le savon abîme chimiquement le SARS‑CoV‑2, et certains ingrédients d’origine naturelle sont particulièrement efficaces. Les savons riches en sels d’acides gras à longues chaînes, comme l’oléate de potassium, peuvent attaquer l’enveloppe huileuse du virus via de fortes interactions hydrophobes et favoriser la fusion et l’agglomération des particules virales, les rendant inoffensives. Bien que tous les tensioactifs testés contribuent à l’inactivation, ceux conçus ou choisis pour une action hydrophobe prononcée peuvent offrir une protection supérieure. Ces informations peuvent aider les chimistes à formuler des savons et désinfectants plus efficaces et doux pour la peau, non seulement contre le SARS‑CoV‑2, mais aussi contre d’autres virus enveloppés qui dépendent du même manteau lipidique fragile.
Citation: Yamamoto, A., Iseki, Y., Elsayed, A.M.A. et al. Differential mechanisms of SARS-CoV-2 inactivation by anionic surfactants: a comparative study of fatty acid salts and synthetic surfactants. Sci Rep 16, 6394 (2026). https://doi.org/10.1038/s41598-026-36858-8
Mots-clés: lavage des mains, SARS‑CoV‑2, tensioactifs de savon, enveloppe virale, désinfectants