Clear Sky Science · fr
YTHDC1 module le phénotype malin du rétinoblastome via l'autophagie médiée par SQSTM1
Pourquoi c’est important pour le cancer de l’œil chez l’enfant
Le rétinoblastome est le cancer de l’œil le plus fréquent chez les jeunes enfants. Les médecins peuvent souvent le guérir s’il est détecté tôt, mais lorsque la tumeur commence à envahir les tissus autour de l’œil ou à se propager vers le cerveau, sauver à la fois la vie et la vision de l’enfant devient beaucoup plus difficile. Cette étude explore un « frein » moléculaire à l’intérieur des cellules tumorales — deux molécules appelées YTHDC1 et SQSTM1 — qui semblent contribuer à maintenir le rétinoblastome moins agressif. Comprendre comment fonctionne ce frein pourrait ouvrir de nouvelles voies pour des traitements plus ciblés et moins agressifs.
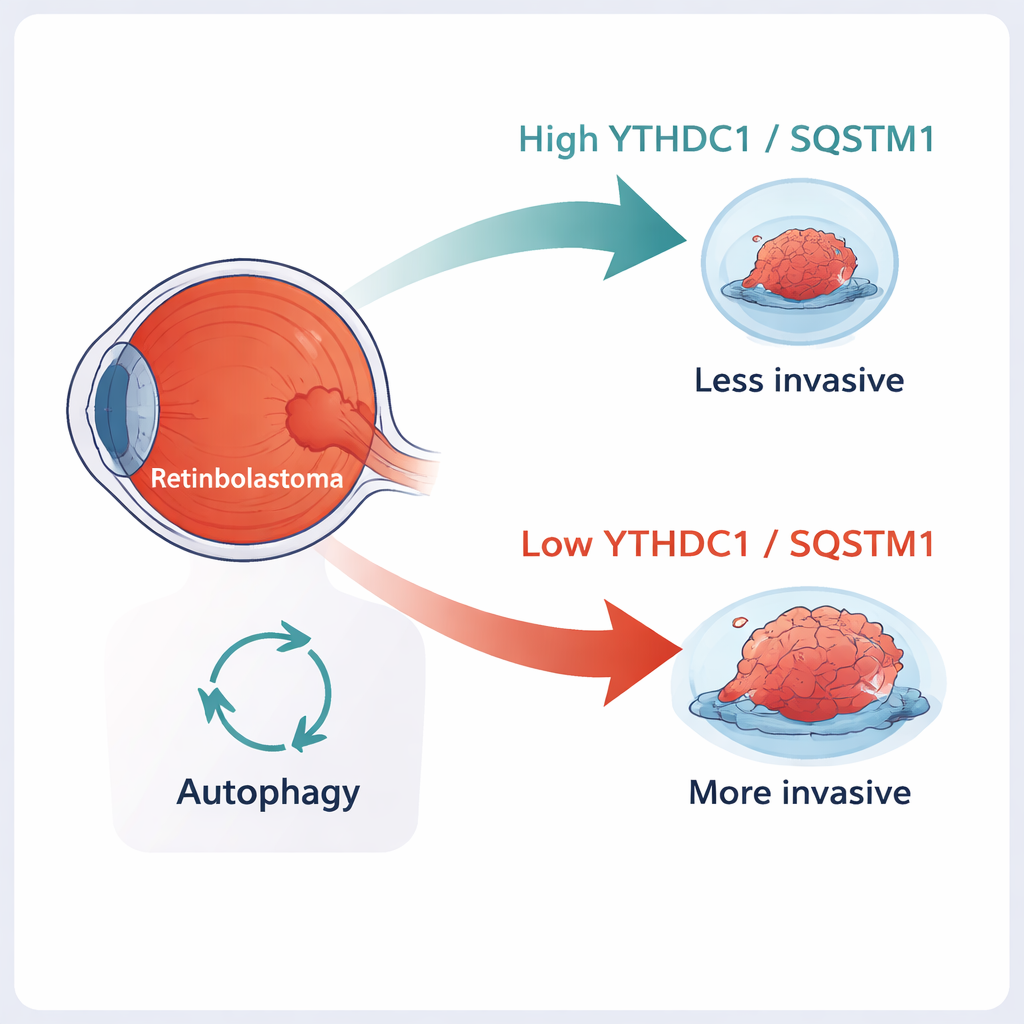
Un examen plus approfondi des tumeurs oculaires infantiles
Le rétinoblastome prend naissance dans la couche sensible à la lumière de l’œil, la rétine, le plus souvent chez les enfants de moins de cinq ans. Classiquement, la maladie débute quand les deux copies d’un gène gardien, RB1, sont perdues. Mais la perte de RB1 à elle seule n’explique pas entièrement pourquoi certaines tumeurs restent confinées dans l’œil tandis que d’autres s’enfoncent dans les tissus voisins ou longent le nerf optique. De plus en plus, les chercheurs réalisent que des marques chimiques apposées sur l’ARN — les messages temporaires qui indiquent à la cellule quelles protéines produire — peuvent influencer fortement le comportement des cancers. L’une des marques les plus communes, appelée m6A, peut modifier la stabilité de ces messages et leur durée de vie dans la cellule.
Découverte d’un frein moléculaire manquant
Les auteurs ont commencé par comparer l’activité génétique dans les tumeurs confinées à l’œil et celles déjà devenues invasives. En utilisant un jeu de données public de séquençage ARN de prélèvements de rétinoblastome, ils ont identifié des milliers de gènes dont l’activité différait entre les deux groupes, puis se sont concentrés sur les « régulateurs » clés de la m6A. Ceux-ci incluent des enzymes qui ajoutent ou retirent la m6A et des protéines « lectrices » qui interprètent cette marque. Parmi dix régulateurs majeurs, ils ont constaté qu’une lectrice, YTHDC1, était de façon constante moins exprimée dans les tumeurs invasives. En examinant des échantillons provenant de 50 enfants et en réalisant des tests en laboratoire sur des tissus tumoraux, ils ont confirmé que les niveaux de YTHDC1 — tant son ARN que sa protéine — étaient réduits dans les cancers les plus agressifs.
Mettre YTHDC1 à l’épreuve
Pour comprendre le rôle réel de YTHDC1, l’équipe a manipulé ses niveaux dans deux lignées cellulaires humaines de rétinoblastome. Lorsqu’ils ont abaissé YTHDC1 à l’aide d’outils génétiques, les cellules se sont multipliées plus rapidement et ont mieux traversé des membranes artificielles mimant des barrières tissulaires — signes d’une tumeur plus invasive. Chez la souris, les cellules dépourvues de YTHDC1 ont formé des tumeurs plus grandes et plus lourdes. L’inverse était également vrai : forcer l’expression de YTHDC1 ralentissait la croissance cellulaire et réduisait leur capacité à migrer et à envahir. Ces expériences suggèrent que YTHDC1 joue un rôle de suppresseur tumoral, aidant à contenir les comportements les plus dangereux du rétinoblastome.
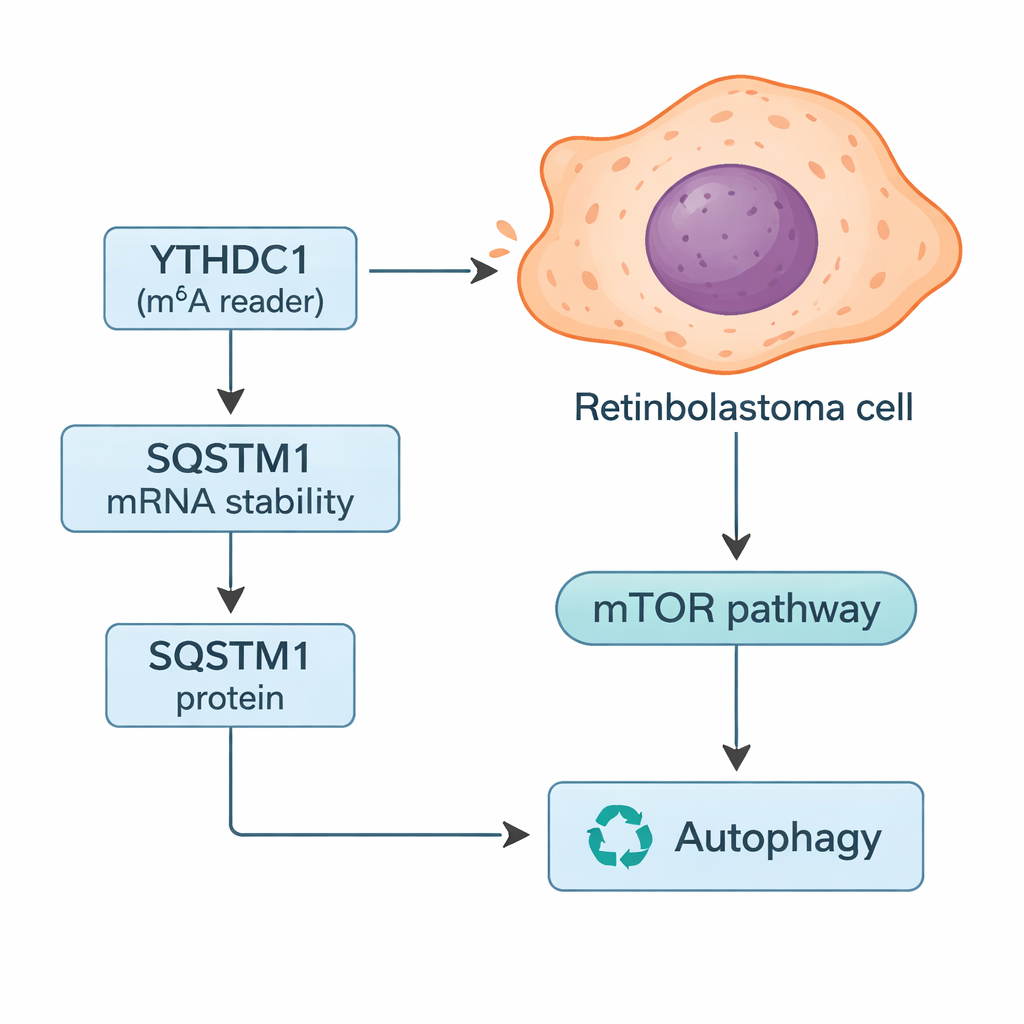
Comment YTHDC1 contrôle le système de recyclage cellulaire
En approfondissant, les chercheurs ont recherché des gènes spécifiques dont les messages pourraient être contrôlés par YTHDC1. En combinant des recherches en bases de données avec leurs données tumorales, ils ont ciblé SQSTM1, une protéine mieux connue sous le nom de p62. SQSTM1 participe à la régulation de l’autophagie, le système de recyclage cellulaire qui dégrade des composants endommagés et peut fournir de l’énergie lorsque les ressources se raréfient. L’étude a montré que YTHDC1 se lie physiquement à l’ARN de SQSTM1 et le stabilise, permettant ainsi une production accrue de protéine SQSTM1. Quand YTHDC1 était réduit, les niveaux de SQSTM1 chutaient et son ARN se dégradait plus rapidement. La suppression de SQSTM1 seule augmentait la croissance et l’invasion des cellules de rétinoblastome, et annulait partiellement les effets protecteurs observés lors de la surexpression de YTHDC1, positionnant SQSTM1 comme un acteur clé intermédiaire de cette voie.
Autophagie, énergie et agressivité tumorale
Parce que SQSTM1 est central pour l’autophagie, l’équipe a testé comment la modification de YTHDC1 et SQSTM1 modifiait ce processus de recyclage. À l’aide d’un ensemble de marqueurs fluorescents et de mesures protéiques, ils ont constaté qu’abaisser YTHDC1 ou SQSTM1 augmentait le « flux » autophagique — davantage de matériel cellulaire était acheminé dans et à travers le système de recyclage. Ils ont aussi observé des changements dans la voie mTOR, un interrupteur majeur de détection des nutriments qui, normalement, freine l’autophagie. Avec moins de SQSTM1, l’activité de mTOR diminuait, ce qui est cohérent avec une activation de l’autophagie. Dans le rétinoblastome invasif, les auteurs proposent que la réduction de YTHDC1 entraîne un affaiblissement du signal SQSTM1, une baisse de l’activité de mTOR et une autophagie accrue qui aide les cellules tumorales à survivre au stress et à se propager.
Ce que cela implique pour les traitements futurs
Pour un non-spécialiste, le message essentiel est que cette étude identifie une chaîne d’événements à l’intérieur des cellules de rétinoblastome — YTHDC1 contrôlant SQSTM1, qui à son tour façonne le système de recyclage cellulaire — et que cette chaîne influence l’agressivité du cancer. Lorsque cette chaîne est affaiblie, les tumeurs croissent plus vite et envahissent davantage. Bien qu’il reste beaucoup de travail avant que ces découvertes puissent parvenir en clinique, cette voie offre de nouvelles idées thérapeutiques : restaurer la fonction de YTHDC1, stabiliser SQSTM1 ou ajuster finement l’autophagie et l’activité de mTOR pourrait un jour compléter les chimiothérapies existantes. Pour les enfants atteints de ce cancer oculaire, de telles stratégies ciblées pourraient aider à limiter la diffusion tumorale tout en préservant davantage la vision et en réduisant les effets secondaires des traitements.
Citation: Ding, J., Sun, J., Wang, J. et al. YTHDC1 modulates the malignant phenotype of retinoblastoma via SQSTM1-mediated autophagy. Sci Rep 16, 6292 (2026). https://doi.org/10.1038/s41598-026-36833-3
Mots-clés: rétinoblastome, YTHDC1, SQSTM1, autophagie, voie mTOR